康方灣區科技園位于中山市翠亨新區,總投資超30億元,占地面積167畝,建筑面積44萬平方米,總規劃產能超過10萬升。康方灣區科技園區集創新抗體藥物研發、原液及制劑生產、銷售于一體,規劃建設成為全球技術水平領先的生物醫藥創新研發和產業化基地。康方灣區科技園分三期項目進行建設,項目一期預計2022年投產。
康方灣區科技園是康方生物全面提升公司一體化研發創新體系、國際化標準的GMP生產體系和先進運作模式的商業化體系能力的重要載體,也是公司繼國家健康科技產業基地中心和中新廣州知識城生物制藥基地之后的第三個產業化基地。基地規劃建設全球領先的生物制藥智能工廠,其工藝自動化項目采用40,000L不銹鋼工藝設備,建成后將成為中國體量最大的抗體藥物生產線之一。
根據協議,西門子將為康方灣區科技園提供全集成的解決方案,包含SIMATIC PCS 7、Batch等在內的工藝過程自動化系統,并在Batch層面對第三方設備進行集成控制,更好地提高工藝流程的柔性化。本次與西門子公司合作,將有助于全面提升康方灣區科技園的自動化、數字化、智能化,進而更好地保障商業化生產階段的產品質量。
康方生物高級副總裁夏羽博士表示:為全世界患者開發可負擔的新一代高品質創新生物藥物,是康方生物作為中國生物藥物創新先行者和推動者的歷史使命。康方灣區科技園數字化智能工廠的建設,有助于進一步快速提升康方生物在國內和國際市場競爭力,包括持續的藥物研發創新能力,以及通過擴大產能、優化工藝和降低管理成本從而降低生物創新藥物生產成本等,為康方生物從Biotech轉變成為Biopharma,乃至進一步發展成為全球具有影響力的Bigpharma提供重要支撐。希望西門子在醫藥行業尖端的自動化解決方案,作為康方生物智能化工廠的“壓艙石”,為康方生物的高質量跨越發展注入更為強勁的動力、提供更為有力的支撐、蓄積更為強大的潛能。
西門子數字化工業集團副總裁兼過程自動化部總經理姚峻博士表示:數據賦能、技術創新將成為單抗乃至生物制藥企業實現降本增效、擴大產能的主要手段,我非常期待能夠將西門子在數字化領域的強勁實力與康方生物在研發和工藝實力相結合,有效保障康方生物后續諸多創新藥物商業化進程,共同推動中國高品質創新生物藥物的發展。
關于康方生物
康方生物(港交所股票代碼:9926.HK)是一家致力于研究、開發、生產及商業化全球病人可負擔的創新抗體新藥的生物制藥公司。自成立以來,公司建立了端對端全方位的藥物開發平臺(ACE平臺),涵蓋了全面一體化的藥物發現和開發功能,包括靶點驗證、抗體發現與開發、CMC生產工藝開發和符合GMP標準的規模化生產。公司也成功建立了雙特異抗體藥物開發平臺(Tetrabody平臺)。公司目前擁有20個以上用于治療腫瘤、自身免疫、炎癥、代謝疾病等重大疾病的創新藥物產品管線,其中13個品種進入臨床研究,包括兩個國際首創的雙特異性抗體新藥(PD-1/CTLA-4以及PD-1/VEGF)。2021年8月,公司首款自主創新研發的差異化PD-1單克隆抗體派安普利單抗注射液(安尼可)已獲批上市。康方生物期望通過高效及突破性的研發創新開發國際首創及同類藥物最佳療法的新藥,成為全球領先的生物制藥企業。
關于西門子中國
西門子股份公司是一家專注于工業、基礎設施、交通和醫療領域的科技公司。從更高效節能的工廠、更具韌性的供應鏈、更智能的樓宇和電網,到更清潔、更舒適的交通以及先進的醫療系統,西門子致力于讓科技有為,為客戶創造價值。通過融合現實與數字世界,西門子賦能客戶推動產業和市場變革,幫助數十億計的人們,共創每一天。2021財年(2020年10月1日至2021年9月30日),西門子在中國的總營收達到82億歐元,擁有超過3萬名員工。西門子已經發展成為中國社會和經濟的一部分,并竭誠與中國攜手合作,共同致力于實現可持續發展。
這意味著,康方生物自主研發并產業化的凱得寧單抗,成為全球第一個遞交上市申請的基于PD-1的雙特異性抗體藥物,也成為中國自主研發的首款雙特異性抗體藥物。
凱得寧單抗在全球率先提交上市并獲得受理,標志著中國生物制藥水平在快速走在世界前列,將有力推動中國生物醫藥產業在全球地位的提升,促進中國從制藥大國走向制藥強國,助力“健康中國2030”戰略的實現。
對康方生物而言,凱得寧單抗是康方生物第二款提交上市申請的自主研發的創新抗體藥物,是康方生物在中國和美國提交的第5個新藥上市申請。
臨床研究數據顯示,凱得寧單抗治療經含鉑化療失敗的復發或轉移性宮頸癌患者的療效顯著,且安全性良好。在目標適應癥人群中,凱得寧單抗與已上市PD-1單抗公開數據相比,顯示了更優療效。相關臨床數據將在有關國際會議及期刊上發表。
復旦大學附屬腫瘤醫院腫瘤婦科主任吳小華教授表示,全球范圍內,雖然有治療宮頸癌適應癥的PD-1單抗獲批上市,但臨床研究結果顯示其僅在2線以上的PD-L1陽性患者中取得不超過15%的客觀緩解率。凱得寧單抗在注冊性II期臨床中表現出來的單藥有效性和安全性數據令人鼓舞,不僅在PD-L1陽性人群中獲得較高的響應率,在PD-L1陰性人群中也看到了不俗的效果,中位無進展生存期也有顯著提升,為中國晚期宮頸癌患者帶來更好的治療手段。2030年是《加速消除宮頸癌全球戰略》和《健康中國2030》綱要的共同關鍵節點,相信凱得寧單抗作為我國第一個自主研發的雙特異性抗體產品,能助力宮頸癌全球和中國健康戰略的順利實現。
中華醫學會婦科腫瘤學分會候任主任委員、山東大學齊魯醫院婦產科孔北華教授表示,子宮頸癌是我國發病率最高的婦科惡性腫瘤,晚期轉移復發患者常規治療難以治愈,是婦科腫瘤醫生面臨的最大挑戰之一,存在重大臨床需求。免疫檢查點抑制劑單藥治療臨床療效不盡滿意,聯合應用雖然有望提高療效但毒副作用嚴重,大大限制了其臨床應用。凱得寧單抗經臨床試驗證明對晚期轉移復發常規治療失敗的子宮頸癌患者有效率高,毒副反應低,安全可控,已進入國家快速審批程序,這是醫生的喜訊,是患者的福音,這將引領我國腫瘤治療在國際上率先進入免疫治療新時代,提升我國子宮頸癌的防治水平,造福廣大患者,可喜可賀。
康方生物創始人、董事長兼職首席執行官夏瑜博士欣喜地指出:凱得寧單抗由康方生物科學家多年潛心研究開發,是具有全球專利的同時靶向PD-1/CTLA-4的單克隆抗體新藥,也是全球首個申請上市的針對PD-1的雙特異性抗體。非常感謝康方團隊、臨床研究中心和醫學專家及各級藥監部門為此做出的卓越努力。康方生物將充分發揮在雙特異性抗體領域的領先優勢,加速推進凱得寧單抗在其他適應癥的臨床研究。我們期待凱得寧單抗在腫瘤雙免疫抗體治療的優勢造福更多的腫瘤患者。
凱得寧單抗治療宮頸癌相關主要里程碑:
2021年7月,凱得寧單抗聯合化療一線治療晚期宮頸癌的III期臨床正式啟動
2021年2月,美國食品藥品監督管理局(FDA)授予凱得寧單抗治療宮頸癌的孤兒藥資格認定
2020年7月,FDA授予凱得寧單抗治療經含鉑化療治療失敗的復發或轉移性宮頸癌的快速審批通道資格
2020年10月,凱得寧單抗用于經標準治療后的復發或轉移性宮頸鱗癌獲得國家藥品監督管理局藥品審評中心(CDE)審核批準納入“突破性治療品種”名單。
目前,凱得寧單抗布局的主要適應癥還包括胃癌、肺癌、肝癌、食管鱗癌及鼻咽癌等。其中,凱得寧單抗治療一線胃癌的III期臨床也已經正式啟動。
關于凱得寧單抗(PD-1/CTLA-4雙抗)
凱得寧單抗 (AK104)是康方生物自主研發的新型的、首創的PD-1/CTLA-4雙特異性腫瘤免疫治療骨干藥物,主要適應癥包括肺癌、肝癌、胃癌、宮頸癌、腎癌、食管鱗癌及鼻咽癌等多種惡性腫瘤,相關腫瘤的研究階段性數據顯示,凱得寧單抗與PD-1聯合CTLA-4的聯合療法相比,毒性顯著降低,具有明顯的安全性和療效優勢。凱得寧單抗是2017年國家衛健委及科技部十三五“重大新藥創制”科技重大專項支持項目,也是2017年廣東省“珠江人才計劃”引進創新創業團隊支持項目。凱得寧單抗的研發被中國醫藥生物技術協會和《中國醫藥生物技術》雜志共同評為“2017年中國醫藥生物技術十大進展”之一。
關于康方生物
康方生物(港交所股票代碼:9926.HK)是一家致力于研究、開發、生產及商業化全球病人可負擔的創新抗體新藥的生物制藥公司。自成立以來,公司建立了端對端全方位的藥物開發平臺(ACE平臺),涵蓋了全面一體化的藥物發現和開發功能,包括靶點驗證、抗體發現與開發、CMC生產工藝開發和符合GMP標準的規模化生產。公司也成功建立了雙特異抗體藥物開發平臺(Tetrabody平臺)。公司目前擁有20個以上用于治療腫瘤、自身免疫、炎癥、代謝疾病等重大疾病的創新藥物產品管線,其中13個品種進入臨床研究,包括兩個國際首創的雙特異性抗體新藥(PD-1/CTLA-4以及PD-1/VEGF)。2021年8月,公司首款自主創新研發的差異化PD-1單克隆抗體派安普利單抗注射液(安尼可)已獲批上市。康方生物期望通過高效及突破性的研發創新開發國際首創及同類藥物最佳療法的新藥,成為全球領先的生物制藥企業。
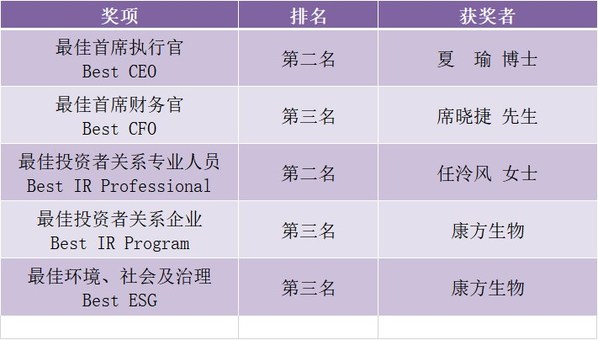
除了獲得“最受尊崇公司”獎項,康方生物還包攬了“醫療健康組別”全部五項獎項的TOP 3:
《Institutional Investor》是全球最具影響力的金融雜志之一,其評選憑借高質量標準聞名業界。本屆評選共有來自18個行業的1,438間公司接受評比,共有3,503位買方投資者及581位賣方分析師參與了投票。
更多關于“2021年亞洲區公司管理團隊”評選信息,請查詢www.institutionalinvestor.com/research/11071/The-All-Asia-Executive-Team
康方生物致力于高效踐行國際標準的公司治理,在資本市場穩健發展。2020年4月上市以來,公司先后被恒生指數公司納入恒生綜合指數(HSCI)、恒生香港上市生物科技指數等恒生系列指數成份股;被上海證券交易所和深圳交易同時納入滬港通下港股通標的和深港通下的港股通股票名單;并于2021年5月納入MSCI中國指數成份股。
2020年度業績公告顯示,康方生物擁有20個以上用于治療腫瘤、自身免疫、炎癥、代謝疾病等重大疾病的創新藥物產品管線,包括6款領先的雙特異性抗體藥物。其中,共有13個產品在中國、美國、澳大利亞等國開展了40多項臨床試驗,9個臨床試驗處于注冊性臨床或III期臨床階段,4個注冊性臨床試驗達到主要終點。公司預期在2021年提交公司全球首創的PD-1/CTLA-4雙特異性抗體新藥Cadonilimab(AK104)治療復發或轉移性宮頸癌的新藥上市申請,該藥物有望成為全球首款基于PD-1的雙特異性抗體藥物,引領腫瘤免疫治療2.0時代。同時還將提交與中國生物制藥(1177.HK)共同開發和商業化的PD-1單抗新藥派安普利Penpulimab(AK105)三線治療轉移性鼻咽癌和派安普利聯合化療一線治療鱗狀非小細胞肺癌的2項新藥上市申請。
聯系方式:
媒體聯系:pr@akesobio.com
投資者聯系:ir@akesobio.com