上海 2025年5月28日 /美通社/ -- 北京時間2025年5月27日,君實生物(1877.HK,688180.SH)宣布,由公司自主研發的昂戈瑞西單抗注射液(重組人源化抗PCSK9單克隆抗體注射液,商品名:君適達®)用于:1)雜合子型家族性高膽固醇血癥(HeFH)的成人患者;2)在他汀類藥物不耐受或禁忌使用的患者中,單獨或與依折麥布聯合用藥用于非家族性高膽固醇血癥和混合型血脂異常的成人患者的兩項新適應癥上市申請近日獲得國家藥品監督管理局(NMPA)批準。此次獲批包括2種規格,分別為150mg(1ml)/支(預充式注射器)、150mg(1ml)/支(預充式自動注射器)。昂戈瑞西單抗成為首個獲批用于他汀不耐受人群的國產PCSK9靶點藥物。
《中國血脂管理指南(2023年)》[1]指出,心血管疾病是我國城鄉居民第一位死因,其中以動脈粥樣硬化性心血管疾病(ASCVD)為主。低密度脂蛋白膽固醇(LDL-C)水平升高是ASCVD的致病性危險因素,通過降低LDL-C水平可顯著減少ASCVD的發病及死亡危險。
HeFH是家族性高膽固醇血癥的常見類型,估測患病率1/250~1/200,主要臨床特征為LDL-C水平顯著升高和早發冠心病[1]。與非家族性高膽固醇血癥患者相比,HeFH患者基礎LDL-C水平更高且指南推薦的控制目標水平更低,若使用他汀類藥物等治療后LDL-C未能達標,將導致患者處于高心血管風險。
此外,盡管目前他汀類藥物已成為降脂治療的基礎,但臨床上約有9.1%的患者存在他汀不耐受,且在亞洲人群中該比例更高[2]。對于他汀不耐受患者,停用或僅使用可耐受劑量的他汀類藥物可能導致LDL-C水平不達標,從而無法達到降低患者ASCVD風險的目的。
PCSK9抑制劑作為強效降低LDL-C水平的新型降脂藥物,已得到國內外血脂管理指南的推薦,并得到臨床醫生的廣泛認可。昂戈瑞西單抗的顯著降脂作用已在多項Ⅲ期臨床研究中獲得證明,并已于2024年10月獲得NMPA批準用于治療原發性高膽固醇血癥(非家族性)和混合型血脂異常的成人患者。
此次兩項新適應癥的獲批主要基于JS002-005(NCT05325203)和JS002-007(NCT05621070)兩項注冊臨床試驗。
其中,JS002-005是在HeFH成人患者中進行的一項隨機、雙盲、安慰劑對照的Ⅲ期臨床研究,由首都醫科大學附屬北京安貞醫院馬長生教授和藺潔教授擔任主要研究者,共入組135例HeFH患者。該研究是首個抗PCSK9單抗用于中國確診HeFH患者(DLCN分值>8分)的Ⅲ期臨床研究。
JS002-005的最新數據已全文發表于《動脈粥樣硬化》(Atherosclerosis),結果顯示[3],與安慰劑相比,昂戈瑞西單抗150mg每2周一次(Q2W)或450mg每4周一次(Q4W)皮下注射治療24周時,可顯著降低LDL-C水平分別達69.4%和80.6%(p?0.0001),且在治療期間維持穩定降幅。同時,昂戈瑞西單抗對其他血脂參數也有明顯的改善作用,非高密度脂蛋白膽固醇(non-HDL-C)、載脂蛋白B(ApoB)、總膽固醇(TC)和脂蛋白(a)[Lp(a)]水平較基線顯著降低,其中Lp(a)較基線降幅達50%。整體安全性良好,治療期間出現的不良事件(TEAE)發生率與安慰劑相當。
JS002-007是在他汀類藥物不耐受的原發性高膽固醇血癥和混合型血脂異常成人患者中完成的一項隨機、雙盲、安慰劑對照的Ⅲ期臨床研究,由北京大學第三醫院唐熠達教授擔任主要研究者。該研究是首個抗PCSK9單抗用于他汀不耐受的中國原發性高膽固醇血癥和混合型血脂異常患者的Ⅲ期臨床研究,研究結果將于近期在國際學術期刊上發表。
君實生物總經理兼首席執行官鄒建軍博士表示:"截至目前,昂戈瑞西單抗已累計獲批3項適應癥,包括雜合子型家族性高膽固醇血癥以及非家族性高膽固醇血癥和混合型血脂異常,同時覆蓋了他汀類藥物不耐受或禁忌使用的非家族性高膽固醇血癥和混合型血脂異常成人患者。這不僅標志著我們在心血管疾病領域取得了重要突破,也代表著中國心血管疾病患者將擁有更多的治療選擇。未來,我們將繼續‘立足中國',圍繞國人臨床未盡之需,致力通過創新藥物探索攻克更多疾病領域并加速創新藥物的可及性。"
| 【參考文獻】 |
| 1. 中國血脂管理指南(2023年). 中國循環雜志. 2023 38;3:237-271. |
| 2. Bytyçi I, et al. Prevalence of statin intolerance: a meta-analysis. Eur Heart J. 2022;43(34):3213-3223. |
| 3. Lin J, Ji Y, Wang G, et al. Efficacy and safety of ongericimab in Chinese patients with heterozygous familial hypercholesterolemia: a randomized, double-blind, placebo-controlled phase 3 trial[J]. Atherosclerosis, 2025: 119120. |
| 1. 本材料旨在傳遞前沿信息,無意向您做任何產品的推廣,不作為臨床用藥指導。 |
| 2. 若您想了解具體疾病診療信息,請遵從醫療衛生專業人士的意見與指導。 |
—— 完 ——
關于昂戈瑞西單抗注射液(君適達 ® )
昂戈瑞西單抗注射液(君適達®)是君實生物自主研發的注射用重組人源化抗PCSK9單克隆抗體注射液,于2024年10月獲NMPA批準上市,目前已在中國內地獲批3項適應癥,用于治療:1)原發性高膽固醇血癥(非家族性)和混合型血脂異常的成人患者;2)雜合子型家族性高膽固醇血癥的成人患者;3)在他汀類藥物不耐受或禁忌使用的患者中,單獨或與依折麥布聯合用藥用于非家族性高膽固醇血癥和混合型血脂異常的成人患者。獲批規格為150mg(1ml)/支(預充式注射器)、150mg(1ml)/支(預充式自動注射器)。
2023年10月,君實生物與重慶博創醫藥有限公司(博創醫藥)達成合作,授予博創醫藥在中國大陸和許可用途內研發、生產、商業化昂戈瑞西單抗的獨占許可。
關于君實生物
君實生物(688180.SH,1877.HK)成立于2012年12月,是一家以創新為驅動,致力于創新療法的發現、開發和商業化的生物制藥公司。依托全球一體化源頭創新研發能力,公司已構建起涵蓋超過50款創新藥物的多層次產品管線,覆蓋惡性腫瘤、自身免疫、慢性代謝類、神經系統、感染性疾病五大治療領域,已有5款產品在國內或海外上市,包括我國首個自主研發、在中美歐等地超過35個國家和地區獲批上市的PD-1抑制劑特瑞普利單抗(拓益®)。疫情期間,君實生物還參與開發了埃特司韋單抗、民得維®等多款預防和治療新冠的創新藥物,積極承擔本土創新藥企的責任。
君實生物以"用世界一流、值得信賴的創新藥普惠患者"為使命,立足中國,布局全球。目前,公司在全球擁有約2500名員工,分布在美國馬里蘭,中國上海、蘇州、北京、廣州等。
官方網站:www.junshipharma.com
官方微信:君實生物
 ]]>
]]>
上海2025年4月25日 /美通社/ -- 北京時間2025年4月25日,君實生物(1877.HK,688180.SH)宣布,由公司自主研發的抗PD-1單抗藥物特瑞普利單抗注射液(拓益®)用于不可切除或轉移性黑色素瘤的一線治療的新適應癥上市申請于近日獲得國家藥品監督管理局(NMPA)批準。這是特瑞普利單抗在中國內地獲批的第12項適應癥。
黑色素瘤是惡性程度最高的皮膚癌類型,2022年全球新發病例約33.2萬,死亡病例約5.9萬[1]。黑色素瘤在我國相對少見,但病死率高(2022年新發病例約0.9萬,而死亡病例達到約0.5萬)[2],發病率也在逐年增加[3]。自2018年起,國內抗PD-1單抗已獲批用于晚期黑色素瘤二線及以上治療并在臨床上得到廣泛使用,但截至目前晚期一線標準治療仍為傳統化療或靶向治療(僅適用于攜帶BRAF V600突變的患者)為主,國內尚無國產抗PD-1單抗獲批該適應癥。因此,國內晚期黑色素瘤患者對于一線免疫治療的臨床需求迫切。
此次新適應癥的獲批主要基于一項多中心、隨機、開放、陽性藥對照的Ⅲ期臨床研究(MELATORCH研究,NCT03430297)的數據結果。MELATORCH是國內首個達成陽性結果的PD-(L)1抑制劑一線治療晚期黑色素瘤的關鍵注冊臨床研究,由北京大學腫瘤醫院郭軍教授擔任主要研究者,在全國11家臨床中心開展。該研究旨在比較特瑞普利單抗對比達卡巴嗪在既往未接受系統抗腫瘤治療的不可切除或轉移性黑色素瘤患者中的有效性和安全性。
此前,MELATORCH的研究成果在第27屆全國臨床腫瘤學大會暨2024年中國臨床腫瘤學會(CSCO)學術年會上首次發布。結果顯示,相較于達卡巴嗪組(N=128),特瑞普利單抗組(N=127)基于盲態獨立中心閱片(BICR)評估的無進展生存期(PFS)顯著延長,兩組中位PFS分別為2.3個月和2.1個月,疾病進展或死亡風險降低29.2%(HR=0.708,95% CI: 0.526-0.954;P=0.0209);矯正后續抗腫瘤治療影響的總生存期(OS)敏感性分析結果顯示,與達卡巴嗪組相比,特瑞普利單抗治療組顯示出明顯的生存獲益趨勢,中位OS分別為15.1個月和9.4個月(HR=0.680,95%CI:0.486-0.951);特瑞普利單抗的安全性良好,與既往研究一致,未發現新的安全信號。
北京大學腫瘤醫院郭軍教授表示:"黑色素瘤是一種惡性程度極高的腫瘤,由于其對傳統放化療的敏感性較低,患者的生存預后往往不夠理想。然而,得益于其較高的免疫原性,近年來以特瑞普利單抗為代表的免疫治療手段顯著改善了患者的生存境遇,尤其在我國,晚期二線及后線患者已可通過國家醫保享受到普惠的治療獲益。如今,特瑞普利單抗進一步拓展至晚期黑色素瘤的一線治療。相較于傳統化療,特瑞普利單抗在無進展生存期(PFS)、客觀緩解率(ORR)和緩解持續時間(DoR)等方面都展現出顯著優勢,總生存期(OS)也呈現出明顯的獲益趨勢。值得一提的是,此次獲批所依據的MELATORCH研究完全納入了中國人群,研究設計更加貼合中國黑色素瘤的臨床實踐,結果對于中國黑色素瘤患者更具參考性。我衷心期待我國自主研發的免疫療法能夠為中國晚期黑色素瘤患者提供覆蓋全人群的系統化解決方案,為更多患者帶來生命的希望與曙光。"
君實生物總經理兼首席執行官鄒建軍博士表示:"僅短短一個月時間,特瑞普利單抗便接連斬獲肝癌和黑色素瘤兩項新適應癥的批準,這一成果無疑是研究者、受試患者以及研發團隊精誠協作、無私奉獻的結晶!回溯到七年前,特瑞普利單抗正是在二線黑色素瘤治療領域率先取得突破,作為首個國產抗PD-1單抗榮耀上市,開啟了國內免疫治療的新紀元;如今,它再續華章,成為首個國產黑色素瘤一線免疫療法,這不僅彰顯了其卓越的臨床價值,更凸顯了我國在腫瘤免疫治療領域的強勁實力與創新活力。未來我們將持續深耕,致力用世界一流、值得信賴的創新藥普惠患者!"
【參考文獻】 |
[1].https://gco.iarc.who.int/media/globocan/factsheets/cancers/16-melanoma-of-skin-fact-sheet.pdf. |
[2].https://gco.iarc.who.int/media/globocan/factsheets/populations/160-china-fact-sheet.pdf. |
[3].中華人民共和國國家衛生健康委員會黑色素瘤診療指南(2022年版). |
1. 本材料旨在傳遞前沿信息,無意向您做任何產品的推廣,不作為臨床用藥指導。
2. 若您想了解具體疾病診療信息,請遵從醫療衛生專業人士的意見與指導。
關于特瑞普利單抗注射液(拓益®)
特瑞普利單抗注射液(拓益®)作為我國批準上市的首個國產以PD-1為靶點的單抗藥物,獲得國家科技重大專項項目支持,并榮膺國家專利領域最高獎項"中國專利金獎"。
特瑞普利單抗至今已在全球(包括中國、美國、歐洲及東南亞等地)開展了覆蓋超過15個適應癥的40多項由公司發起的臨床研究。正在進行或已完成的關鍵注冊臨床研究在多個瘤種范圍內評估特瑞普利單抗的安全性及療效,包括肺癌、鼻咽癌、食管癌、胃癌、膀胱癌、乳腺癌、肝癌、腎癌及皮膚癌等。
截至目前,特瑞普利單抗已在中國內地獲批12項適應癥:【1】用于既往接受全身系統治療失敗的不可切除或轉移性黑色素瘤的治療(2018年12月);【2】用于既往接受過二線及以上系統治療失敗的復發/轉移性鼻咽癌患者的治療(2021年2月);【3】用于含鉑化療失敗包括新輔助或輔助化療12個月內進展的局部晚期或轉移性尿路上皮癌的治療(2021年4月);【4】聯合順鉑和吉西他濱用于局部復發或轉移性鼻咽癌患者的一線治療(2021年11月);【5】聯合紫杉醇和順鉑用于不可切除局部晚期/復發或遠處轉移性食管鱗癌患者的一線治療(2022年5月);【6】聯合培美曲塞和鉑類用于表皮生長因子受體(EGFR)基因突變陰性和間變性淋巴瘤激酶(ALK)陰性、不可手術切除的局部晚期或轉移性非鱗狀非小細胞肺癌的一線治療(2022年9月);【7】聯合化療圍手術期治療,繼之本品單藥作為輔助治療,用于可切除IIIA-IIIB期非小細胞肺癌的成人患者(2023年12月);【8】聯合阿昔替尼用于中高危的不可切除或轉移性腎細胞癌患者的一線治療(2024年4月);【9】聯合依托泊苷和鉑類用于廣泛期小細胞肺癌一線治療(2024年6月);【10】聯合注射用紫杉醇(白蛋白結合型)用于經充分驗證的檢測評估PD-L1陽性(CPS≥1)的復發或轉移性三陰性乳腺癌的一線治療(2024年6月);【11】聯合貝伐珠單抗用于不可切除或轉移性肝細胞癌患者的一線治療(2025年3月);【12】用于不可切除或轉移性黑色素瘤的一線治療(2025年4月)。2020年12月,特瑞普利單抗首次通過國家醫保談判,目前已有10項獲批適應癥納入《國家醫保目錄(2024年)》,是目錄中唯一用于黑色素瘤、非小細胞肺癌圍手術期、腎癌、三陰性乳腺癌治療的抗PD-1單抗藥物。2024年10月,特瑞普利單抗用于復發/轉移性鼻咽癌治療的適應癥在中國香港獲批。
在國際化布局方面,特瑞普利單抗目前已在美國、歐盟、印度、英國、約旦、澳大利亞、新加坡等國家和地區獲得批準上市,并在全球多個國家和地區接受上市審評。
關于君實生物
君實生物(688180.SH,1877.HK)成立于2012年12月,是一家以創新為驅動,致力于創新療法的發現、開發和商業化的生物制藥公司。依托全球一體化源頭創新研發能力,公司已構建起涵蓋超過50款創新藥物的多層次產品管線,覆蓋惡性腫瘤、自身免疫、慢性代謝類、神經系統、感染性疾病五大治療領域,已有5款產品在國內或海外上市,包括我國首個自主研發、在中美歐等地超過35個國家和地區獲批上市的PD-1抑制劑特瑞普利單抗(拓益®)。疫情期間,君實生物還參與開發了埃特司韋單抗、民得維®等多款預防和治療新冠的創新藥物,積極承擔本土創新藥企的責任。
君實生物以"用世界一流、值得信賴的創新藥普惠患者"為使命,立足中國,布局全球。目前,公司在全球擁有約2500名員工,分布在美國馬里蘭,中國上海、蘇州、北京、廣州等。
官方網站:www.junshipharma.com
官方微信:君實生物

上海2025年3月26日 /美通社/ -- 君實生物(1877.HK,688180.SH)宣布,由公司自主研發的抗PD-1單抗藥物特瑞普利單抗(新加坡商品名:LOQTORZI®)聯合順鉑和吉西他濱用于復發、不能手術或放療的,或轉移性鼻咽癌成人患者的一線治療的上市許可申請獲得新加坡衛生科學局(HSA)批準。特瑞普利單抗成為新加坡首個且唯一獲批用于鼻咽癌的腫瘤免疫治療藥物。
鼻咽癌是一種發生于鼻咽部黏膜上皮的惡性腫瘤,是常見的頭頸部惡性腫瘤之一。報告指出,2022年鼻咽癌在全球范圍內確診的新發病例數超過12萬[1]。特瑞普利單抗是《美國國家綜合癌癥網絡(NCCN)頭頸部腫瘤臨床實踐指南2025.V1》中推薦用于復發/轉移性鼻咽癌全線治療的唯一首選藥物[2]。
本次鼻咽癌適應癥的獲批主要基于JUPITER-02(一項針對一線治療鼻咽癌的隨機、雙盲、安慰劑對照、國際多中心Ⅲ期臨床研究,NCT03581786)的研究結果。JUPITER-02研究是鼻咽癌免疫治療領域首個國際多中心、樣本量最大的雙盲、隨機對照III期臨床研究,也是全球首個鼻咽癌一線免疫聯合化療對比單純化療將總生存期(OS)預設有統計學檢驗(一類錯誤控制)并確證具有生存獲益的Ⅲ期臨床研究。該研究結果曾以口頭報告形式亮相2021年美國臨床腫瘤學會(ASCO)年會全體大會(#LBA2),隨后榮登《自然-醫學》(Nature Medicine)雜志封面,并獲得《美國醫學會雜志》(Journal of the American Medical Association,JAMA)全文發表。
研究結果顯示,與單純化療相比,特瑞普利單抗聯合化療使患者的疾病進展風險降低48%,死亡風險降低37%。特瑞普利單抗聯合化療組的中位無進展生存期(PFS)對比單純化療延長了13.2個月,從8.2個月提升至21.4個月。此外,接受該聯合療法治療的患者可獲得更高的客觀緩解率(ORR)和更長的持續緩解時間(DoR),完全緩解(CR)率達到26.7%,且未發現新的安全性信號。長期生存隨訪數據在2024年ASCO年會展示,特瑞普利單抗治療組5年生存率達到52%。
君實生物總經理兼首席執行官鄒建軍博士表示:"特瑞普利單抗在新加坡獲批標志著我們正式登陸東南亞市場。東南亞是鼻咽癌的高發地區之一,我們很高興能夠將鼻咽癌領域具有劃時代意義的創新療法帶給東南亞患者,以改變當地的治療格局。目前,特瑞普利單抗已成功在全球四個大洲的超過35個國家和地區獲批上市。我們將繼續深化‘立足中國,布局全球'的國際化戰略,推動中國創新藥造福世界患者。"
此次上市許可申請的遞交是通過奧比斯項目(Project Orbis)。該項目由美國食品藥品監督管理局(FDA)腫瘤學卓越中心(OCE)發起和倡導,為FDA和其它國家及地區的監管機構搭建合作機制和框架,允許不同監管機構共同審評腫瘤藥品的注冊申請。特瑞普利單抗治療是首個被納入奧比斯項目的國產腫瘤藥,此前君實生物通過奧比斯項目向澳大利亞藥品管理局(TGA)遞交的特瑞普利單抗鼻咽癌適應癥的2項上市許可申請已獲得TGA批準。
【參考文獻】 |
1. https://gco.iarc.who.int/media/globocan/factsheets/cancers/4-nasopharynx-fact-sheet.pdf. |
2. 2025NCCN 臨床實踐指南:頭頸部腫瘤(2025.V1) |
1. 本材料旨在傳遞前沿信息,無意向您做任何產品的推廣,不作為臨床用藥指導。 |
關于特瑞普利單抗注射液(拓益®)
特瑞普利單抗注射液(拓益®)作為我國批準上市的首個國產以PD-1為靶點的單抗藥物,獲得國家科技重大專項項目支持,并榮膺國家專利領域最高獎項"中國專利金獎"。
特瑞普利單抗至今已在全球(包括中國、美國、歐洲及東南亞等地)開展了覆蓋超過15個適應癥的40多項由公司發起的臨床研究。正在進行或已完成的關鍵注冊臨床研究在多個瘤種范圍內評估特瑞普利單抗的安全性及療效,包括肺癌、鼻咽癌、食管癌、胃癌、膀胱癌、乳腺癌、肝癌、腎癌及皮膚癌等。
截至目前,特瑞普利單抗已在中國內地獲批11項適應癥:用于既往接受全身系統治療失敗的不可切除或轉移性黑色素瘤的治療(2018年12月);用于既往接受過二線及以上系統治療失敗的復發/轉移性鼻咽癌患者的治療(2021年2月);用于含鉑化療失敗包括新輔助或輔助化療12個月內進展的局部晚期或轉移性尿路上皮癌的治療(2021年4月);聯合順鉑和吉西他濱用于局部復發或轉移性鼻咽癌患者的一線治療(2021年11月);聯合紫杉醇和順鉑用于不可切除局部晚期/復發或遠處轉移性食管鱗癌患者的一線治療(2022年5月);聯合培美曲塞和鉑類用于表皮生長因子受體(EGFR)基因突變陰性和間變性淋巴瘤激酶(ALK)陰性、不可手術切除的局部晚期或轉移性非鱗狀非小細胞肺癌的一線治療(2022年9月);聯合化療圍手術期治療,繼之本品單藥作為輔助治療,用于可切除IIIA-IIIB期非小細胞肺癌的成人患者(2023年12月);聯合阿昔替尼用于中高危的不可切除或轉移性腎細胞癌患者的一線治療(2024年4月);聯合依托泊苷和鉑類用于廣泛期小細胞肺癌一線治療(2024年6月);聯合注射用紫杉醇(白蛋白結合型)用于經充分驗證的檢測評估PD-L1陽性(CPS≥1)的復發或轉移性三陰性乳腺癌的一線治療(2024年6月);聯合貝伐珠單抗用于不可切除或轉移性肝細胞癌患者的一線治療(2025年3月)。2020年12月,特瑞普利單抗首次通過國家醫保談判,目前已有10項獲批適應癥納入《國家醫保目錄(2024年)》,是目錄中唯一用于黑色素瘤、非小細胞肺癌圍手術期、腎癌、三陰性乳腺癌治療的抗PD-1單抗藥物。2024年10月,特瑞普利單抗用于復發/轉移性鼻咽癌治療的適應癥在中國香港獲批。
在國際化布局方面,特瑞普利單抗目前已在美國、歐盟、印度、英國、約旦、澳大利亞、新加坡等國家和地區獲得批準上市,并在全球多個國家或地區接受上市審評。
關于君實生物
君實生物(688180.SH,1877.HK)成立于2012年12月,是一家以創新為驅動,致力于創新療法的發現、開發和商業化的生物制藥公司。依托全球一體化源頭創新研發能力,公司已構建起涵蓋超過50款創新藥物的多層次產品管線,覆蓋惡性腫瘤、自身免疫、慢性代謝類、神經系統、感染性疾病五大治療領域,已有5款產品在國內或海外上市,包括我國首個自主研發、在中美歐等地超過35個國家和地區獲批上市的PD-1抑制劑特瑞普利單抗(拓益®)。疫情期間,君實生物還參與開發了埃特司韋單抗、民得維®等多款預防和治療新冠的創新藥物,積極承擔本土創新藥企的責任。
君實生物以"用世界一流、值得信賴的創新藥普惠患者"為使命,立足中國,布局全球。目前,公司在全球擁有約2500名員工,分布在美國舊金山和馬里蘭,中國上海、蘇州、北京、廣州等。
官方網站:www.junshipharma.com
官方微信:君實生物

上海2025年3月21日 /美通社/ -- 北京時間2025年3月21日,君實生物(1877.HK,688180.SH)宣布,由公司自主研發的抗PD-1單抗藥物特瑞普利單抗注射液(拓益®)聯合貝伐珠單抗用于不可切除或轉移性肝細胞癌(HCC)患者的一線治療新適應癥的上市申請于近日獲得國家藥品監督管理局(NMPA)批準。這是特瑞普利單抗在中國獲批的第11項適應癥。
肝癌是世界范圍內常見的消化系統惡性腫瘤,病理類型以肝細胞癌(HCC)為主(約占90%)[1]。2022年,全球肝癌的年新發病例數和死亡例數分別為86.6萬和75.9萬[2]。我國是肝癌大國,2022年肝癌新發病例數達到36.8萬(占全球病例的42.4%),居國內惡性腫瘤第4位,死亡31.7萬(占全球病例的41.7%),居國內惡性腫瘤第2位[3]。由于起病隱匿,約70%-80%的中國肝癌患者首次診斷時已是中晚期[4],中位總生存期(OS)僅約10個月,5年生存率約12%[5]。
此次新適應癥的獲批主要基于HEPATORCH研究(NCT04723004)的數據結果。HEPATORCH研究是一項國際多中心、隨機、開放、陽性藥對照的Ⅲ期臨床研究,由中國科學院院士、復旦大學附屬中山醫院樊嘉教授擔任主要研究者,在中國大陸、中國臺灣和新加坡的57家臨床中心開展,共入組326例患者。研究旨在評估與標準治療索拉非尼相比,特瑞普利單抗聯合貝伐珠單抗(TB方案)一線治療不可切除或轉移性HCC的有效性和安全性。
此前,HEPATORCH的研究成果在第27屆全國臨床腫瘤學大會暨2024年中國臨床腫瘤學會(CSCO)學術年會上首次發布,主要研究終點無進展生存期(PFS,基于獨立影像評估)和OS達到"雙終點陽性結果"。與索拉非尼相比,特瑞普利單抗聯合貝伐珠單抗可顯著延長患者的PFS和OS,兩組中位PFS分別為5.8 vs. 4.0個月,疾病進展或死亡風險降低31%(HR=0.69,95% CI:0.525-0.913;P=0.0086),兩組中位OS分別為20.0 vs. 14.5個月,死亡風險降低24%(HR=0.76,95% CI:0.579-0.987;P=0.0394)。特瑞普利單抗聯合貝伐珠單抗組客觀緩解率(ORR)較索拉非尼組顯著提高,兩組ORR分別為25.3% vs. 6.1%。同時,該聯合療法在晚期HCC患者中的安全性良好,毒性譜與已知單藥毒性譜一致,未發現新的安全信號。
復旦大學附屬中山醫院樊嘉院士表示:"免疫聯合抗血管生成治療已成為晚期肝癌一線治療基石。HEPATORCH研究充分驗證了特瑞普利單抗在中國肝癌患者中的臨床療效,聯合貝伐ORR高達25.3%,中位PFS為5.8個月,中位OS達到20.0個月。特瑞普利單抗聯合貝伐珠單抗的TB方案將造福更多中國晚期肝癌患者。"
君實生物總經理兼首席執行官鄒建軍博士表示:"在'十全實美'的基礎上,特瑞普利單抗繼續突破,迎來了其第11個適應癥的正式獲批,這讓我們倍感振奮!作為全球肝癌疾病負擔最重的國家,我國肝癌患者長期面臨治療選擇有限的困境。君實生物長期聚焦全球肝癌治療領域的臨床需求,針對不同病程人群布局了運用多元聯用策略的臨床研究,旨在為肝癌患者提供更精準、更豐富的治療選擇。我們將持續致力于該領域內的藥物創新,為人類抗擊肝癌事業注入更強大的'中國智慧'。"
【參考文獻】 |
1. Hepatocellular carcinoma. Nat Rev Dis Primers. 2021;7(1):7. |
2. Bray F, Laversanne M, Sung H, et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2024;74(3):229-263. |
3. Zheng RS, Chen R, Han BF, et al. Zhonghua Zhong Liu Za Zhi. 2024;46(3):221-231. |
4.《靶免聯合局部治療 中晚期肝細胞癌中國專家共識》, 肝癌電子雜志, 2023, 10(3): 1-11 |
5. Zeng H, Chen W, Zheng R, et al. Changing cancer survival in China during 2003-15: a pooled analysis of 17 population-based cancer registries. Lancet Glob Health. 2018;6(5):e555-e567. |
1. 本材料旨在傳遞前沿信息,無意向您做任何產品的推廣,不作為臨床用藥指導。 |
關于特瑞普利單抗注射液(拓益®)
特瑞普利單抗注射液(拓益®)作為我國批準上市的首個國產以PD-1為靶點的單抗藥物,獲得國家科技重大專項項目支持,并榮膺國家專利領域最高獎項"中國專利金獎"。
特瑞普利單抗至今已在全球(包括中國、美國、歐洲及東南亞等地)開展了覆蓋超過15個適應癥的40多項由公司發起的臨床研究。正在進行或已完成的關鍵注冊臨床研究在多個瘤種范圍內評估特瑞普利單抗的安全性及療效,包括肺癌、鼻咽癌、食管癌、胃癌、膀胱癌、乳腺癌、肝癌、腎癌及皮膚癌等。
截至目前,特瑞普利單抗已在中國內地獲批11項適應癥:用于既往接受全身系統治療失敗的不可切除或轉移性黑色素瘤的治療(2018年12月);用于既往接受過二線及以上系統治療失敗的復發/轉移性鼻咽癌患者的治療(2021年2月);用于含鉑化療失敗包括新輔助或輔助化療12個月內進展的局部晚期或轉移性尿路上皮癌的治療(2021年4月);聯合順鉑和吉西他濱用于局部復發或轉移性鼻咽癌患者的一線治療(2021年11月);聯合紫杉醇和順鉑用于不可切除局部晚期/復發或遠處轉移性食管鱗癌患者的一線治療(2022年5月);聯合培美曲塞和鉑類用于表皮生長因子受體(EGFR)基因突變陰性和間變性淋巴瘤激酶(ALK)陰性、不可手術切除的局部晚期或轉移性非鱗狀非小細胞肺癌的一線治療(2022年9月);聯合化療圍手術期治療,繼之本品單藥作為輔助治療,用于可切除IIIA-IIIB期非小細胞肺癌的成人患者(2023年12月);聯合阿昔替尼用于中高危的不可切除或轉移性腎細胞癌患者的一線治療(2024年4月);聯合依托泊苷和鉑類用于廣泛期小細胞肺癌一線治療(2024年6月);聯合注射用紫杉醇(白蛋白結合型)用于經充分驗證的檢測評估PD-L1陽性(CPS≥1)的復發或轉移性三陰性乳腺癌的一線治療(2024年6月);聯合貝伐珠單抗用于不可切除或轉移性肝細胞癌患者的一線治療(2025年3月)。2020年12月,特瑞普利單抗首次通過國家醫保談判,目前已有10項獲批適應癥納入《國家醫保目錄(2024年)》,是目錄中唯一用于黑色素瘤、非小細胞肺癌圍手術期、腎癌、三陰性乳腺癌治療的抗PD-1單抗藥物。2024年10月,特瑞普利單抗用于復發/轉移性鼻咽癌治療的適應癥在中國香港獲批。
在國際化布局方面,特瑞普利單抗目前已在美國、歐盟、印度、英國、約旦、澳大利亞等國家和地區獲得批準上市,并在全球多個國家或地區接受上市審評。
關于君實生物
君實生物(688180.SH,1877.HK)成立于2012年12月,是一家以創新為驅動,致力于創新療法的發現、開發和商業化的生物制藥公司。依托全球一體化源頭創新研發能力,公司已構建起涵蓋超過50款創新藥物的多層次產品管線,覆蓋惡性腫瘤、自身免疫、慢性代謝類、神經系統、感染性疾病五大治療領域,已有5款產品在國內或海外上市,包括我國首個自主研發、在中美歐等地超過35個國家和地區獲批上市的PD-1抑制劑特瑞普利單抗(拓益®)。疫情期間,君實生物還參與開發了埃特司韋單抗、民得維®等多款預防和治療新冠的創新藥物,積極承擔本土創新藥企的責任。
君實生物以"用世界一流、值得信賴的創新藥普惠患者"為使命,立足中國,布局全球。目前,公司在全球擁有約2500名員工,分布在美國舊金山和馬里蘭,中國上海、蘇州、北京、廣州等。
官方網站:www.junshipharma.com
官方微信:君實生物

上海2025年1月20日 /美通社/ -- 北京時間2025年1月20日,君實生物(1877.HK,688180.SH)宣布全資子公司TopAlliance Biosciences與利奧制藥(LEO Pharma)就特瑞普利單抗在歐洲的分銷與商業化達成合作。通過強強聯合,雙方將攜手提升特瑞普利單抗在歐洲市場的可及性,為歐洲患者提供優質的創新療法。
特瑞普利單抗是一款以PD-1為靶點的單抗藥物,由中國本土創新藥企君實生物自主研發,至今已在全球超過35個國家和地區獲批上市,用于多種惡性腫瘤治療。2024年,特瑞普利單抗分別獲得歐盟委員會(EC)和英國藥品和保健品管理局(MHRA)的批準,用于以下兩項適應癥:1)聯合順鉑和吉西他濱,用于復發、不能手術或放療的,或轉移性鼻咽癌(NPC)成人患者的一線治療;2)聯合順鉑和紫杉醇,用于不可切除的晚期/復發或轉移性食管鱗癌成人患者的一線治療。特瑞普利單抗是歐洲首個且目前唯一獲批用于鼻咽癌治療的藥物,同時也是歐洲唯一用于不限PD-L1表達的晚期或轉移性食管鱗癌一線免疫治療藥物。
根據協議,利奧制藥將負責特瑞普利單抗在歐盟(EU)及歐洲經濟區(EEA)所有成員國,以及瑞士、英國的分銷、推廣、銷售等工作,目前最多可達32個國家。君實生物將作為特瑞普利單抗在歐洲的上市許可持有人(MAH),負責產品的開發、生產、注冊、藥物警戒、質量管理等事務。此外,利奧制藥將向君實生物支付包括首付款、未來可能新增的獲批適應癥的里程款項,以及特瑞普利單抗在合作區域內銷售凈額兩位數百分比的銷售分成。
君實生物高級副總裁、TopAlliance Biosciences首席執行官姚盛博士表示,"與LEO Pharma的合作為君實生物在歐洲市場樹立了一個重要的里程碑,與公司的全球化拓展戰略高度契合。歐洲已被確定為公司業務增長的關鍵戰略區域。作為該產品在歐洲的藥品上市許可持有人(MAH),我們已在當地建立了運營中心,并正在積極與當地衛生部門合作,為特瑞普利單抗在歐洲的成功商業上市做好準備。利奧制藥作為一家總部在歐洲、擁有百年歷史的跨國制藥企業,在歐洲市場構建了成熟的藥品分銷網絡,并積累了豐富的市場推廣經驗。我們相信,雙方將充分發揮各自在研發、生產和商業化方面的優勢,讓特瑞普利單抗能夠精準且高效地覆蓋歐洲市場,及早惠及當地有需求的患者。未來,我們將繼續踐行公司‘立足中國,布局全球'的國際化戰略,攜手合作伙伴為全球患者提供來自中國的高質量創新藥。"
利奧制藥執行副總裁Jean Monin表示:"我們很高興能與君實生物合作,為利奧制藥現有的抗栓塞業務錦上添花,該業務已為癌癥相關血栓患者提供服務。LOQTORZI®(特瑞普利單抗)的分銷和營銷合作為那些存在高度未被滿足的臨床需求的地區帶來了重要的新治療選擇。這項合作專注于專科醫院產品,能夠補充我們現有的針對癌癥相關血栓及其他專科患者的基于肝素的抗凝治療。借助我們的商業平臺,LOQTORZI®將創造有價值的協同效應,并推動持續增長。"
1. 本材料旨在傳遞前沿信息,無意向您做任何產品的推廣,不作為臨床用藥指導。 |
2. 若您想了解具體疾病診療信息,請遵從醫療衛生專業人士的意見與指導。 |
關于特瑞普利單抗注射液(拓益®)
特瑞普利單抗注射液(拓益®)作為我國批準上市的首個國產以PD-1為靶點的單抗藥物,獲得國家科技重大專項項目支持,并榮膺國家專利領域最高獎項"中國專利金獎"。
特瑞普利單抗至今已在全球(包括中國、美國、歐洲及東南亞等地)開展了覆蓋超過15個適應癥的40多項由公司發起的臨床研究。正在進行或已完成的關鍵注冊臨床研究在多個瘤種范圍內評估特瑞普利單抗的安全性及療效,包括肺癌、鼻咽癌、食管癌、胃癌、膀胱癌、乳腺癌、肝癌、腎癌及皮膚癌等。
截至目前,特瑞普利單抗已在中國內地獲批10項適應癥:用于既往接受全身系統治療失敗的不可切除或轉移性黑色素瘤的治療(2018年12月);用于既往接受過二線及以上系統治療失敗的復發/轉移性鼻咽癌患者的治療(2021年2月);用于含鉑化療失敗包括新輔助或輔助化療12個月內進展的局部晚期或轉移性尿路上皮癌的治療(2021年4月);聯合順鉑和吉西他濱用于局部復發或轉移性鼻咽癌患者的一線治療(2021年11月);聯合紫杉醇和順鉑用于不可切除局部晚期/復發或遠處轉移性食管鱗癌患者的一線治療(2022年5月);聯合培美曲塞和鉑類用于表皮生長因子受體(EGFR)基因突變陰性和間變性淋巴瘤激酶(ALK)陰性、不可手術切除的局部晚期或轉移性非鱗狀非小細胞肺癌的一線治療(2022年9月);聯合化療圍手術期治療,繼之本品單藥作為輔助治療,用于可切除IIIA-IIIB期非小細胞肺癌的成人患者(2023年12月);聯合阿昔替尼用于中高危的不可切除或轉移性腎細胞癌患者的一線治療(2024年4月);聯合依托泊苷和鉑類用于廣泛期小細胞肺癌一線治療(2024年6月);聯合注射用紫杉醇(白蛋白結合型)用于經充分驗證的檢測評估PD-L1陽性(CPS≥1)的復發或轉移性三陰性乳腺癌的一線治療(2024年6月)。2020年12月,特瑞普利單抗首次通過國家醫保談判,目前已有10項獲批適應癥納入《國家醫保目錄(2024年)》,是目錄中唯一用于黑色素瘤、非小細胞肺癌圍手術期、腎癌、三陰性乳腺癌治療的抗PD-1單抗藥物。2024年10月,特瑞普利單抗用于復發/轉移性鼻咽癌治療的適應癥在中國香港獲批。
在國際化布局方面,特瑞普利單抗目前已在美國、歐盟、印度、英國、約旦、澳大利亞等國家和地區獲得批準上市。特瑞普利單抗的上市申請正在全球多個國家接受審評,其中包括新加坡衛生科學局(HSA)。
關于利奧制藥
利奧制藥是一家全球性公司,致力于通過創新改善皮膚病患者的標準治療,同時還為癌癥患者和其他專科患者提供抗凝血治療。利奧制藥由主要股東利奧基金會和自2021年起的Nordic Capital共同持有。利奧制藥提供廣泛的治療產品,每年為1億患者服務。公司總部位于丹麥,擁有4000人的全球團隊。2023年,公司的銷售凈額達到16億美元。更多詳情請訪問:https://www.leo-pharma.com。
關于君實生物
君實生物(688180.SH,1877.HK)成立于2012年12月,是一家以創新為驅動,致力于創新療法的發現、開發和商業化的生物制藥公司。依托全球一體化源頭創新研發能力,公司已構建起涵蓋超過50款創新藥物的多層次產品管線,覆蓋惡性腫瘤、自身免疫、慢性代謝類、神經系統、感染性疾病五大治療領域,已有5款產品在國內或海外上市,包括我國首個自主研發、在中美歐等地超過35個國家和地區獲批上市的PD-1抑制劑特瑞普利單抗(拓益®)。疫情期間,君實生物還參與開發了埃特司韋單抗、民得維®等多款預防和治療新冠的創新藥物,積極承擔本土創新藥企的責任。
君實生物以"用世界一流、值得信賴的創新藥普惠患者"為使命,立足中國,布局全球。目前,公司在全球擁有約2500名員工,分布在美國舊金山和馬里蘭,中國上海、蘇州、北京、廣州等。更多關于君實生物的信息,請訪問:www.junshipharma.com
官方網站:www.junshipharma.com
官方微信:君實生物
]]>
上海2025年1月17日 /美通社/ -- 北京時間2025年1月17日,君實生物(1877.HK,688180.SH)宣布,由公司自主研發的抗PD-1單抗藥物特瑞普利單抗的上市許可申請于近日獲得澳大利亞藥品管理局(TGA)批準,用于治療兩項鼻咽癌(NPC)適應癥:1)特瑞普利單抗聯合順鉑/吉西他濱作為轉移性或復發性局部晚期鼻咽癌成人患者的一線治療;2)特瑞普利單抗單藥治療既往含鉑治療過程中或治療后疾病進展的復發性、不可切除或轉移性鼻咽癌的成人患者。特瑞普利單抗成為澳大利亞首個且唯一用于鼻咽癌的腫瘤免疫治療藥物。
值得注意的是,上述上市許可的申請通過奧比斯項目(Project Orbis)遞交。該項目由美國食品藥品監督管理局(FDA)腫瘤學卓越中心(OCE)發起和倡導,為FDA和其它國家及地區的監管機構搭建合作機制和框架,允許不同監管機構共同審評腫瘤藥品的注冊申請。特瑞普利單抗是首個被納入Project Orbis的國產腫瘤藥。此外,特瑞普利單抗用于治療鼻咽癌還獲得TGA授予的孤兒藥資格認定,一定程度上加速了其在當地的審評審批注冊進度。
君實生物總經理兼首席執行官鄒建軍博士表示:"特瑞普利單抗的國際化進展捷報頻傳。截至目前,特瑞普利單抗已在全球四大洲超過35個國家獲得批準,為全球廣大患者帶去希望。此次在澳大利亞獲批,不僅對于澳大利亞鼻咽癌患者而言意義重大,也標志著公司全球化布局的進一步深化。后續我們將攜手合作伙伴全力加快提升特瑞普利單抗在澳大利亞的可及性,以期盡早惠及當地患者。"
瑞迪博士實驗室品牌市場(印度和新興市場)首席執行官M.V. Ramana先生表示:"此次特瑞普利單抗在澳大利亞獲批是我們與君實生物合作的重要里程碑,標志著君實生物的創新療法正在惠及全球患者。特瑞普利單抗是澳大利亞首個也是唯一一個用于治療鼻咽癌的免疫療法,填補了該地區鼻咽癌患者巨大的未被滿足的需求。在腫瘤領域,我們的目標是構建一個端到端的護理生態系統——包括全球各國現有癌癥標準治療藥物的獲取,在制劑上創新,對創新分子開展戰略合作,以及提供超越藥物的支持,如營養建議和數字工具。繼特瑞普利單抗在印度成功上市后,我們非常期待未來能夠為澳大利亞及其他市場的患者帶去這款藥物。"
鼻咽癌是一種發生于鼻咽部黏膜上皮的惡性腫瘤,是常見的頭頸部惡性腫瘤之一。根據GLOBOCAN 2022發布的數據顯示,2022年鼻咽癌在全球范圍內確診的新發病例數超過12萬[1]。特瑞普利單抗是《美國國家綜合癌癥網絡(NCCN)頭頸部腫瘤臨床實踐指南2025.V1》中推薦用于復發/轉移性鼻咽癌全線治療的唯一首選藥物[2]。
本次上市申請的批準主要基于JUPITER-02(一項針對一線治療鼻咽癌的隨機、雙盲、安慰劑對照、國際多中心Ⅲ期臨床研究,NCT03581786)及POLARIS-02(一項針對二線及以上治療的復發或轉移性鼻咽癌的多中心、開放標簽、Ⅱ期關鍵注冊臨床研究,NCT02915432)的研究結果。
其中,JUPITER-02是鼻咽癌免疫治療領域首個國際多中心、樣本量最大的雙盲、隨機對照Ⅲ期臨床研究,也是全球首個鼻咽癌一線免疫聯合化療對比單純化療將總生存期(OS)預設有統計學檢驗(一類錯誤控制)并確證具有生存獲益的Ⅲ期臨床研究。其研究結果曾以口頭報告形式亮相2021年美國臨床腫瘤學會(ASCO)年會全體大會(#LBA2),隨后榮登《自然-醫學》(Nature Medicine,影響因子:58.7)雜志封面,并獲得《美國醫學會雜志》(Journal of the American Medical Association,JAMA,影響因子:63.1)全文發表。研究結果顯示,與單純化療相比,特瑞普利單抗聯合化療使患者的疾病進展風險降低48%,死亡風險降低37%。特瑞普利單抗聯合化療組的中位無進展生存期(PFS)對比單純化療延長了13.2個月,從8.2個月提升到21.4個月。此外,接受該聯合療法治療的患者可獲得更高的客觀緩解率(ORR)和更長的持續緩解時間(DoR),完全緩解(CR)率達到26.7%,且未發現新的安全性信號。長期生存隨訪數據在2024年ASCO年會展示,特瑞普利單抗治療組5年生存率達到52.0%。
POLARIS-02研究結果已于2021年1月在線發表于《臨床腫瘤學雜志》(Journal of Clinical Oncology,影響因子:42.1)。研究結果顯示,特瑞普利單抗在既往化療失敗的復發/轉移性鼻咽癌患者中表現出持久的抗腫瘤活性和可控的安全性,患者ORR為20.5%,DoR為12.8個月,中位OS達17.4個月。
截至目前,特瑞普利單抗已在全球四大洲超過35個國家和地區獲批多項適應癥,包括中國內地、中國香港、美國、歐盟、英國、澳大利亞、印度、約旦等。
1. 本材料旨在傳遞前沿信息,無意向您做任何產品的推廣,不作為臨床用藥指導。
2. 若您想了解具體疾病診療信息,請遵從醫療衛生專業人士的意見與指導。
【參考文獻】
[1]. https://gco.iarc.who.int/media/globocan/factsheets/cancers/4-nasopharynx-fact-sheet.pdf.
[2]. 2025NCCN 臨床實踐指南:頭頸部腫瘤(2025.V1).
關于特瑞普利單抗注射液(拓益®)
特瑞普利單抗注射液(拓益®)作為我國批準上市的首個國產以PD-1為靶點的單抗藥物,獲得國家科技重大專項項目支持,并榮膺國家專利領域最高獎項"中國專利金獎"。
特瑞普利單抗至今已在全球(包括中國、美國、歐洲及東南亞等地)開展了覆蓋超過15個適應癥的40多項由公司發起的臨床研究。正在進行或已完成的關鍵注冊臨床研究在多個瘤種范圍內評估特瑞普利單抗的安全性及療效,包括肺癌、鼻咽癌、食管癌、胃癌、膀胱癌、乳腺癌、肝癌、腎癌及皮膚癌等。
截至目前,特瑞普利單抗已在中國內地獲批10項適應癥:用于既往接受全身系統治療失敗的不可切除或轉移性黑色素瘤的治療(2018年12月);用于既往接受過二線及以上系統治療失敗的復發/轉移性鼻咽癌患者的治療(2021年2月);用于含鉑化療失敗包括新輔助或輔助化療12個月內進展的局部晚期或轉移性尿路上皮癌的治療(2021年4月);聯合順鉑和吉西他濱用于局部復發或轉移性鼻咽癌患者的一線治療(2021年11月);聯合紫杉醇和順鉑用于不可切除局部晚期/復發或遠處轉移性食管鱗癌患者的一線治療(2022年5月);聯合培美曲塞和鉑類用于表皮生長因子受體(EGFR)基因突變陰性和間變性淋巴瘤激酶(ALK)陰性、不可手術切除的局部晚期或轉移性非鱗狀非小細胞肺癌的一線治療(2022年9月);聯合化療圍手術期治療,繼之本品單藥作為輔助治療,用于可切除IIIA-IIIB期非小細胞肺癌的成人患者(2023年12月);聯合阿昔替尼用于中高危的不可切除或轉移性腎細胞癌患者的一線治療(2024年4月);聯合依托泊苷和鉑類用于廣泛期小細胞肺癌一線治療(2024年6月);聯合注射用紫杉醇(白蛋白結合型)用于經充分驗證的檢測評估PD-L1陽性(CPS≥1)的復發或轉移性三陰性乳腺癌的一線治療(2024年6月)。2020年12月,特瑞普利單抗首次通過國家醫保談判,目前已有10項獲批適應癥納入《國家醫保目錄(2024年)》,是目錄中唯一用于黑色素瘤、非小細胞肺癌圍手術期、腎癌、三陰性乳腺癌治療的抗PD-1單抗藥物。2024年10月,特瑞普利單抗用于復發/轉移性鼻咽癌治療的適應癥在中國香港獲批。
在國際化布局方面,特瑞普利單抗目前已在美國、歐盟、印度、英國、約旦、澳大利亞等國家和地區獲得批準上市。此外,特瑞普利單抗的上市申請正在全球多個國家接受審評,其中包括新加坡衛生科學局(HSA)。
關于君實生物
君實生物(688180.SH,1877.HK)成立于2012年12月,是一家以創新為驅動,致力于創新療法的發現、開發和商業化的生物制藥公司。依托全球一體化源頭創新研發能力,公司已構建起涵蓋超過50款創新藥物的多層次產品管線,覆蓋惡性腫瘤、自身免疫、慢性代謝類、神經系統、感染性疾病五大治療領域,已有5款產品在國內或海外上市,包括我國首個自主研發、在中美歐等地超過35個國家和地區獲批上市的PD-1抑制劑特瑞普利單抗(拓益®)。疫情期間,君實生物還參與開發了埃特司韋單抗、民得維®等多款預防和治療新冠的創新藥物,積極承擔本土創新藥企的責任。
君實生物以"用世界一流、值得信賴的創新藥普惠患者"為使命,立足中國,布局全球。目前,公司在全球擁有約2500名員工,分布在美國舊金山和馬里蘭,中國上海、蘇州、北京、廣州等。
官方網站:www.junshipharma.com
官方微信:君實生物
]]>
上海2025年1月10日 /美通社/ -- 北京時間2025年1月10日,君實生物(1877.HK,688180.SH)宣布,公司旗下的口服核苷類抗新型冠狀病毒(SARS-CoV-2)藥物民得維®(氫溴酸氘瑞米德韋片,產品代號:VV116/JT001)用于治療輕中度新型冠狀病毒感染(COVID-19)的成年患者的適應癥正式獲得國家藥品監督管理局(NMPA)同意,由附條件批準轉為常規批準。
2023年1月28日,基于一項在伴或不伴有進展為重癥高風險因素的輕中度COVID-19患者中開展的多中心、雙盲、隨機、安慰劑對照、Ⅲ期臨床研究(JT001-015研究,NCT05582629),民得維®獲得國家藥監局附條件上市批準。
此次民得維®常規批準基于多項臨床及非臨床研究,包括JT001-015研究和一項納入近8000例患者的真實世界研究。研究結果顯示,在輕、中度新冠患者中,民得維®可顯著加速癥狀緩解和消失、縮短病程,加快病毒轉陰,降低重癥COVID-19或全因死亡發生率,對老年和高風險患者效果更顯著。在輕中度肝腎功能不全的患者中,民得維®表現出良好的安全性和耐受性,患者在服藥過程中無需或僅需少量調整用藥劑量。同時,藥理研究顯示民得維®基本無藥物間相互作用,大大減少了用藥禁忌,有效保障患者的合并用藥,為特殊人群提供了更安全、更有效的選擇。
此外,相關研究表明,民得維®可顯著抑制新冠病毒XBB.1.16、EG.5、JN.1變異株,對主要流行株持續有效。
民得維®上市以來,可及性不斷提升,自2024年1月1日起被正式納入國家醫保藥品目錄,每個療程價格為475元,按照乙類醫保報銷,大幅低于同類進口產品。患者可在醫院及互聯網醫院就診購買,顯著提升了抗病毒藥物的可及性和便利性。
1. 本材料旨在傳遞前沿信息,無意向您做任何產品的推廣,不作為臨床用藥指導。
2. 若您想了解具體疾病診療信息,請遵從醫療衛生專業人士的意見與指導。
—— 完 ——
關于氫溴酸氘瑞米德韋片(民得維®,VV116/JT001)
民得維®是一款口服核苷類藥物,可抑制SARS-CoV-2復制。臨床前研究顯示,民得維®對包括奧密克戎在內的新冠病毒原始株和突變株表現出顯著的抗病毒作用,且無遺傳毒性。該產品由中國科學院上海藥物研究所、中國科學院武漢病毒研究所、中國科學院新疆理化技術研究所、中國科學院中亞藥物研發中心/中烏醫藥科技城(科技部"一帶一路"聯合實驗室)、臨港實驗室、蘇州旺山旺水生物醫藥有限公司和君實生物共同研發。
在新冠疫情期間,民得維®在國內外開展了多項臨床研究。一項在伴有進展為重癥高風險因素的輕中度COVID-19患者中對比PAXLOVID用于輕中度COVID-19早期治療的Ⅲ期臨床研究(JT001-010)獲得國際權威期刊《新英格蘭醫學雜志》(The New England Journal of Medicine,IF:96.2)發表[1],另一項在伴或不伴有進展為重癥高風險因素的輕中度COVID-19患者中開展的Ⅲ期臨床研究(JT001-015)獲得國際頂尖感染病學期刊《柳葉刀-感染病學》(The Lancet Infectious Diseases,IF:36.4)發表[2]。
2021年12月,民得維®在烏茲別克斯坦獲得批準用于治療中/重度COVID-19患者。
2023年1月,民得維®在中國獲得批準用于治療輕中度COVID-19的成年患者,并于2023年1月起臨時性納入醫保支付范圍,2024年1月起納入正式國家醫保目錄。
【參考文獻】 |
[1] Cao Z, Gao W, Bao H, et al. VV116 versus Nirmatrelvir–Ritonavir for Oral Treatment of Covid-19. N Engl J Med. DOI: 10.1056/NEJMoa2208822. |
[2] Xiaohong Fan, Xiahong Dai, Yun Ling, et al. Oral VV116 versus placebo in patients with mild-to-moderate COVID-19 in China: a multicentre, double-blind, phase 3, randomised controlled study. The Lancet Infectious Diseases. DOI:10.1016/S1473-3099(23)00577-7. |
關于君實生物
君實生物(688180.SH,1877.HK)成立于2012年12月,是一家以創新為驅動,致力于創新療法的發現、開發和商業化的生物制藥公司。依托全球一體化源頭創新研發能力,公司已構建起涵蓋超過50款創新藥物的多層次產品管線,覆蓋惡性腫瘤、自身免疫、慢性代謝類、神經系統、感染性疾病五大治療領域,已有5款產品在國內或海外上市,包括我國首個自主研發、在中美歐等地超過35個國家和地區獲批上市的PD-1抑制劑特瑞普利單抗(拓益®),臨床開發階段的藥物超過30款。疫情期間,君實生物還參與開發了埃特司韋單抗、民得維®等多款預防和治療新冠的創新藥物,積極承擔本土創新藥企的責任。
君實生物以"用世界一流、值得信賴的創新藥普惠患者"為使命,立足中國,布局全球。目前,公司在全球擁有約2500名員工,分布在美國舊金山和馬里蘭,中國上海、蘇州、北京、廣州等。
官方網站:www.junshipharma.com
官方微信:君實生物
]]>

上海2025年1月6日 /美通社/ -- 北京時間2025年1月6日,君實生物(1877.HK,688180.SH)宣布,由公司自主研發的抗PD-1單抗藥物特瑞普利單抗(商品名:拓益®)用于既往接受全身系統治療失敗的不可切除或轉移性黑色素瘤的治療的適應癥正式獲得國家藥品監督管理局(NMPA)同意,由附條件批準轉為常規批準。
附條件批準上市審評審批政策旨在鼓勵以臨床價值為導向的藥物創新,加快具有突出臨床價值的臨床急需藥品上市。2018年12月,基于一項多中心、單臂、開放標簽的Ⅱ期臨床研究(POLARIS-01研究,NCT03013101),特瑞普利單抗獲得NMPA附條件上市批準,用于既往接受全身系統治療失敗的不可切除或轉移性黑色素瘤的治療,成為我國批準上市的首個國產以PD-1為靶點的單抗藥物。此次獲得常規批準,意味著特瑞普利單抗按監管部門要求完成了必要的驗證性臨床試驗,并證明了其在目標人群中的有效性和安全性。
本次常規批準主要基于一項多中心、隨機、開放、陽性對照的Ⅲ期臨床研究(MELATORCH研究,NCT03430297)。MELATORCH研究旨在比較特瑞普利單抗對比達卡巴嗪在既往未接受系統抗腫瘤治療的不可切除或轉移性黑色素瘤患者中的有效性和安全性,主要研究終點為無進展生存期(PFS,基于獨立影像評估)。北京大學腫瘤醫院郭軍教授擔任該研究的主要研究者,全國11家臨床中心參研。該研究也是目前國內首個且唯一達成陽性結果的PD-(L)1抑制劑一線治療晚期黑色素瘤的關鍵注冊臨床研究。
MELATAORCH研究結果顯示,相較于達卡巴嗪組(N=128),特瑞普利單抗組(N=127)基于獨立影像評估的PFS顯著延長,疾病進展或死亡風險降低29.2%(HR=0.708;95% CI: 0.526-0.954;P=0.0209),其他療效終點(包括研究者評估的PFS、客觀緩解率、緩解持續時間以及總生存期)也顯示出獲益趨勢;安全性良好,與既往研究一致,未發現新的安全信號1。
同時,基于上述研究,NMPA于2024年8月受理了特瑞普利單抗用于不可切除或轉移性黑色素瘤一線治療的新適應癥上市申請。這是特瑞普利單抗在中國內地遞交的第十二項上市申請。
1. 本材料旨在傳遞前沿信息,無意向您做任何產品的推廣,不作為臨床用藥指導。 |
2. 若您想了解具體疾病診療信息,請遵從醫療衛生專業人士的意見與指導。 |
—— 完 ——
關于黑色素瘤
黑色素瘤是惡性程度最高的皮膚癌類型,2022年全球新發病例約33.2萬,死亡病例約5.9萬2。黑色素瘤在我國相對少見,但病死率高(2022年新發病例約0.9萬,而死亡病例達到約0.5萬)3,發病率也在逐年增加4。
【參考文獻】 |
1. 盛錫楠、黃鋼、方美玉等,特瑞普利單抗對比達卡巴嗪一線治療晚期黑色素瘤:一項多中心、隨機、對照、開放標簽的III期臨床研究。2024年中國臨床腫瘤學會學術年會。 |
2. https://gco.iarc.who.int/media/globocan/factsheets/cancers/16-melanoma-of-skin-fact-sheet.pdf. |
3. https://gco.iarc.who.int/media/globocan/factsheets/populations/160-china-fact-sheet.pdf. |
4. 中華人民共和國國家衛生健康委員會黑色素瘤診療指南(2022年版). |
關于特瑞普利單抗注射液(拓益®)
特瑞普利單抗注射液(拓益®)作為我國批準上市的首個國產以PD-1為靶點的單抗藥物,獲得國家科技重大專項項目支持,并榮膺國家專利領域最高獎項"中國專利金獎"。
特瑞普利單抗至今已在全球(包括中國、美國、東南亞及歐洲等地)開展了覆蓋超過15個適應癥的40多項由公司發起的臨床研究。正在進行或已完成的關鍵注冊臨床研究在多個瘤種范圍內評估特瑞普利單抗的安全性及療效,包括肺癌、鼻咽癌、食管癌、胃癌、膀胱癌、乳腺癌、肝癌、腎癌及皮膚癌等。
截至目前,特瑞普利單抗已在中國內地獲批10項適應癥:用于既往接受全身系統治療失敗的不可切除或轉移性黑色素瘤的治療(2018年12月);用于既往接受過二線及以上系統治療失敗的復發/轉移性鼻咽癌患者的治療(2021年2月);用于含鉑化療失敗包括新輔助或輔助化療12個月內進展的局部晚期或轉移性尿路上皮癌的治療(2021年4月);聯合順鉑和吉西他濱用于局部復發或轉移性鼻咽癌患者的一線治療(2021年11月);聯合紫杉醇和順鉑用于不可切除局部晚期/復發或遠處轉移性食管鱗癌患者的一線治療(2022年5月);聯合培美曲塞和鉑類用于表皮生長因子受體(EGFR)基因突變陰性和間變性淋巴瘤激酶(ALK)陰性、不可手術切除的局部晚期或轉移性非鱗狀非小細胞肺癌的一線治療(2022年9月);聯合化療圍手術期治療,繼之本品單藥作為輔助治療,用于可切除IIIA-IIIB期非小細胞肺癌的成人患者(2023年12月);聯合阿昔替尼用于中高危的不可切除或轉移性腎細胞癌患者的一線治療(2024年4月);聯合依托泊苷和鉑類用于廣泛期小細胞肺癌一線治療(2024年6月);聯合注射用紫杉醇(白蛋白結合型)用于經充分驗證的檢測評估PD-L1陽性(CPS≥1)的復發或轉移性三陰性乳腺癌的一線治療(2024年6月)。2020年12月,特瑞普利單抗首次通過國家醫保談判,目前已有10項獲批適應癥納入《國家醫保目錄(2024年)》,是目錄中唯一用于黑色素瘤、非小細胞肺癌圍手術期、腎癌、三陰性乳腺癌治療的抗PD-1單抗藥物。2024年10月,香港藥劑業及毒藥管理局(PPB)批準了特瑞普利單抗的上市申請用于復發/轉移性鼻咽癌的治療。
在國際化布局方面,特瑞普利單抗目前已在美國、歐盟、印度、英國、約旦等國家和地區獲得批準上市。此外,澳大利亞藥品管理局(TGA)和新加坡衛生科學局(HSA)分別受理了特瑞普利單抗聯合順鉑/吉西他濱作為轉移性或復發性局部晚期鼻咽癌成人患者的一線治療,以及作為單藥治療既往含鉑治療過程中或治療后疾病進展的復發性、不可切除或轉移性鼻咽癌的成人患者的上市許可申請。
關于君實生物
君實生物(688180.SH,1877.HK)成立于2012年12月,是一家以創新為驅動,致力于創新療法的發現、開發和商業化的生物制藥公司。依托全球一體化源頭創新研發能力,公司已構建起涵蓋超過50款創新藥物的多層次產品管線,覆蓋惡性腫瘤、自身免疫、慢性代謝類、神經系統、感染性疾病五大治療領域,已有5款產品在國內或海外上市,包括我國首個自主研發、在中美歐等地超過35個國家和地區獲批上市的PD-1抑制劑特瑞普利單抗(拓益®),臨床開發階段的藥物超過30款。疫情期間,君實生物還參與開發了埃特司韋單抗、民得維®等多款預防和治療新冠的創新藥物,積極承擔本土創新藥企的責任。
君實生物以"用世界一流、值得信賴的創新藥普惠患者"為使命,立足中國,布局全球。目前,公司在全球擁有約2500名員工,分布在美國舊金山和馬里蘭,中國上海、蘇州、北京、廣州等。
官方網站:www.junshipharma.com
官方微信:君實生物
]]>
上海2024年11月28日 /美通社/ -- 北京時間11月28日,君實生物(1877.HK,688180.SH)宣布,公司自主研發的抗PD-1單抗產品特瑞普利單抗(商品名:拓益®)新增4項適應癥成功被納入《國家基本醫療保險、工傷保險和生育保險藥品目錄(2024年)》(國家醫保目錄)。新版國家醫保目錄將于2025年1月1日起正式實施。至此,拓益®在國內獲批的10個適應癥已全部納入國家醫保目錄,是目錄中唯一用于黑色素瘤、非小細胞肺癌圍手術期、腎癌和三陰性乳腺癌治療的抗PD-1單抗。
以下為拓益®納入本次新版國家醫保目錄的適應癥:
原有適應癥:
- 既往接受全身系統治療失敗的不可切除或轉移性黑色素瘤的治療;
- 含鉑化療失敗包括新輔助或輔助化療12個月內進展的局部晚期或轉移性尿路上皮癌的治療;
- 既往接受過二線及以上系統治療失敗的復發/轉移性鼻咽癌患者的治療;
- 局部復發或轉移性鼻咽癌患者的一線治療;
- 不可切除局部晚期/復發或轉移性食管鱗癌的一線治療;
- 表皮生長因子受體(EGFR)基因突變陰性和間變性淋巴瘤激酶(ALK)陰性、不可手術切除的局部晚期或轉移性非鱗狀非小細胞肺癌(NSCLC)的一線治療。
新增適應癥:
- 聯合化療圍手術期治療,繼之本品單藥作為輔助治療,用于可切除ⅢA-ⅢB期非小細胞肺癌(NSCLC)的成人患者;
- 聯合阿昔替尼用于中高危的不可切除或轉移性腎細胞癌患者的一線治療;
- 聯合依托泊苷和鉑類用于廣泛期小細胞肺癌(ES-SCLC)的一線治療;
- 聯合注射用紫杉醇(白蛋白結合型)用于經充分驗證的檢測評估PD-L1陽性(CPS≥1)的復發或轉移性三陰性乳腺癌(TNBC)的一線治療。
作為公司的核心產品之一,特瑞普利單抗在開發過程中,即采用差異化的優效策略,其具有獨特的結合位點,高親和力,強勁誘導PD-1受體內吞。2018年,特瑞普利單抗(拓益®)正式在國內獲批上市,成為我國首個批準上市的國產PD-1單抗。2023年10月,特瑞普利單抗的上市申請獲得美國食品藥品監督管理局(FDA)批準,成為美國首個且目前唯一獲批用于鼻咽癌治療的藥物,也是FDA批準上市的首個中國自主研發和生產的創新生物藥。
目前,特瑞普利單抗已在包括中國、美國、歐盟、英國、印度等在內超過35個國家及地區正式獲批上市,累計在全球開展了覆蓋超過15個適應癥的40多項臨床研究,全球商業化網絡布局超過50個國家或地區,是首個獲得中、美、歐三大權威指南(NCCN/ESMO/CSCO)推薦的國產抗PD-1單抗。
君實生物首席商務官王行遠先生表示:"近年來,國家醫保局支持醫藥創新,建立了以新藥為主體的醫保準入和談判續約機制。獲益于此,拓益®累計10項適應癥納入國家醫保,為其2024年成功達成'十全實美'畫上了圓滿的句號。讓我們倍感振奮的是,今年拓益®新納入的4項適應癥均實現了目錄中免疫治療藥物'零的突破',是目錄中首次納入肺癌圍手術期、小細胞肺癌、腎癌以及三陰性乳腺癌免疫療法。我們非常期待在新版醫保落地后,這款已在中、美、歐等地獲批上市的首個國產免疫創新藥,能夠將國際品質和親民價格帶給更廣泛的中國患者。未來,我們也將繼續助力國家醫改,推進解決看病難、看病貴問題,積極踐行公司使命:'打造世界一流、值得信賴的創新藥普惠患者'!"
1. 本材料旨在傳遞前沿信息,無意向您做任何產品的推廣,不作為臨床用藥指導。
2. 若您想了解具體疾病診療信息,請遵從醫療衛生專業人士的意見與指導。
關于特瑞普利單抗注射液(拓益®)
特瑞普利單抗注射液(拓益®)作為我國批準上市的首個國產以PD-1為靶點的單抗藥物,獲得國家科技重大專項項目支持,并榮膺國家專利領域最高獎項"中國專利金獎"。
特瑞普利單抗至今已在全球(包括中國、美國、東南亞及歐洲等地)開展了覆蓋超過15個適應癥的40多項由公司發起的臨床研究。正在進行或已完成的關鍵注冊臨床研究在多個瘤種范圍內評估特瑞普利單抗的安全性及療效,包括肺癌、鼻咽癌、食管癌、胃癌、膀胱癌、乳腺癌、肝癌、腎癌及皮膚癌等。
截至目前,特瑞普利單抗已在中國內地獲批10項適應癥:用于既往接受全身系統治療失敗的不可切除或轉移性黑色素瘤的治療(2018年12月);用于既往接受過二線及以上系統治療失敗的復發/轉移性鼻咽癌患者的治療(2021年2月);用于含鉑化療失敗包括新輔助或輔助化療12個月內進展的局部晚期或轉移性尿路上皮癌的治療(2021年4月);聯合順鉑和吉西他濱用于局部復發或轉移性鼻咽癌患者的一線治療(2021年11月);聯合紫杉醇和順鉑用于不可切除局部晚期/復發或遠處轉移性食管鱗癌患者的一線治療(2022年5月);聯合培美曲塞和鉑類用于表皮生長因子受體(EGFR)基因突變陰性和間變性淋巴瘤激酶(ALK)陰性、不可手術切除的局部晚期或轉移性非鱗狀非小細胞肺癌的一線治療(2022年9月);聯合化療圍手術期治療,繼之本品單藥作為輔助治療,用于可切除IIIA-IIIB期非小細胞肺癌的成人患者(2023年12月);聯合阿昔替尼用于中高危的不可切除或轉移性腎細胞癌患者的一線治療(2024年4月);聯合依托泊苷和鉑類用于廣泛期小細胞肺癌一線治療(2024年6月);聯合注射用紫杉醇(白蛋白結合型)用于經充分驗證的檢測評估PD-L1陽性(CPS≥1)的復發或轉移性三陰性乳腺癌的一線治療(2024年6月)。2020年12月,特瑞普利單抗首次通過國家醫保談判,目前已有10項獲批適應癥納入《國家醫保目錄(2024年)》,是目錄中唯一用于黑色素瘤、非小細胞肺癌圍手術期、腎癌、三陰性乳腺癌治療的抗PD-1單抗藥物。2024年10月,特瑞普利單抗用于復發/轉移性鼻咽癌治療的適應癥在中國香港獲批。
在國際化布局方面,特瑞普利單抗目前已在美國、歐盟、印度、英國、約旦等國家和地區獲得批準上市。此外,澳大利亞藥品管理局(TGA)和新加坡衛生科學局(HSA)分別受理了特瑞普利單抗聯合順鉑/吉西他濱作為轉移性或復發性局部晚期鼻咽癌成人患者的一線治療,以及作為單藥治療既往含鉑治療過程中或治療后疾病進展的復發性、不可切除或轉移性鼻咽癌的成人患者的上市許可申請。
關于君實生物
君實生物(688180.SH,1877.HK)成立于2012年12月,是一家以創新為驅動,致力于創新療法的發現、開發和商業化的生物制藥公司。依托全球一體化源頭創新研發能力,公司已構建起涵蓋超過50款創新藥物的多層次產品管線,覆蓋惡性腫瘤、自身免疫、慢性代謝類、神經系統、感染性疾病五大治療領域,已有5款產品在國內或海外上市,包括我國首個自主研發、在中美歐等地超過35個國家和地區獲批上市的PD-1抑制劑特瑞普利單抗(拓益®),臨床開發階段的藥物超過30款。疫情期間,君實生物還參與開發了埃特司韋單抗、民得維®等多款預防和治療新冠的創新藥物,積極承擔本土創新藥企的責任。
君實生物以"用世界一流、值得信賴的創新藥普惠患者"為使命,立足中國,布局全球。目前,公司在全球擁有約2500名員工,分布在美國舊金山和馬里蘭,中國上海、蘇州、北京、廣州等。
官方網站:www.junshipharma.com
官方微信:君實生物
媒體聯系人:Zhi LI, zhi_li@junshipharma.com
]]>- 特瑞普利單抗聯合順鉑和吉西他濱用于復發、不能手術或放療的,或轉移性鼻咽癌(NPC)成人患者的一線治療;
- 特瑞普利單抗聯合順鉑和紫杉醇用于不可切除的晚期/復發或轉移性食管鱗癌(ESCC)成人患者的一線治療。
君實生物總經理兼首席執行官鄒建軍博士表示:"此次獲得MHRA批準,是特瑞普利單抗在歐洲的又一重要里程碑,不僅使得特瑞普利單抗成為英國首個且唯一用于NPC治療的藥物,也是英國唯一用于不限PD-L1表達的晚期或轉移性食管鱗癌一線治療藥物。能夠將中國創新生物藥帶到英國,解決當地患者長期未被滿足的臨床需求,我們倍感自豪。后續,我們將繼續遵循公司‘立足中國,布局全球’的全球化戰略,推進特瑞普利單抗在全球的商業化落地,讓高質量的中國創新藥惠及更多全球患者。"
本次MHRA對于NPC和ESCC適應癥的批準分別基于JUPITER-02(一項隨機、雙盲、安慰劑對照、國際多中心Ⅲ期臨床研究,NCT03581786)和JUPITER-06(一項隨機、雙盲、安慰劑對照、多中心的Ⅲ期研究,NCT03829969)的研究結果。
其中,JUPITER-02是鼻咽癌免疫治療領域首個國際多中心、樣本量最大的雙盲、隨機對照Ⅲ期臨床研究,也是全球首個鼻咽癌一線免疫聯合化療對比單純化療將總生存期(OS)預設有統計學檢驗(一類錯誤控制)并確證具有生存獲益的Ⅲ期臨床研究。其研究結果曾以口頭報告形式亮相2021年美國臨床腫瘤學會(ASCO)年會全體大會(#LBA2),隨后榮登《自然-醫學》(Nature Medicine,影響因子:58.7)雜志封面,并獲得《美國醫學會雜志》(Journal of the American Medical Association,JAMA,影響因子:63.1)全文發表。研究結果顯示,與單純化療相比,特瑞普利單抗聯合化療使患者的疾病進展風險降低48%,死亡風險降低37%。特瑞普利單抗聯合化療組的中位無進展生存期(PFS)對比單純化療延長了13.2個月,從8.2個月提升到21.4個月。此外,接受該聯合療法治療的患者可獲得更高的客觀緩解率(ORR)和更長的持續緩解時間(DoR),完全緩解(CR)率達到26.7%,且未發現新的安全性信號。長期生存隨訪數據在2024年ASCO年會展示,特瑞普利單抗治療組5年生存率達到52.0%。
基于該項研究,特瑞普利單抗于2021年獲得國家藥品監督管理局(NMPA)批準用于晚期鼻咽癌的治療,是全球首個獲批鼻咽癌治療的免疫檢查點抑制劑(ICI)藥物。同時,特瑞普利單抗還作為首款鼻咽癌藥物在美國、歐洲、印度、約旦、中國香港獲批。此外,特瑞普利單抗用于治療NPC相關適應癥的上市申請正在同步接受澳大利亞藥品管理局(TGA)和新加坡衛生科學局(HSA)的審評。
JUPITER-06是一項隨機、雙盲、安慰劑對照、多中心的Ⅲ期臨床研究(NCT03829969),旨在評估與安慰劑聯合化療相比,特瑞普利單抗聯合紫杉醇/順鉑(TP)用于晚期ESCC一線治療的療效及安全性。該研究結果首次在歐洲腫瘤內科學會年會(ESMO 2021)上以口頭匯報形式報告,隨后在國際頂尖腫瘤學雜志《Cancer Cell》(影響因子:48.8)和《臨床腫瘤學雜志》(Journal of Clinical Oncology,影響因子:42.1)發表。研究結果顯示,特瑞普利單抗聯合化療可使晚期或轉移性ESCC患者獲得更優的PFS和OS,其中中位OS延長6個月,達到17個月,并顯著降低患者的疾病進展或死亡風險達42%,顯著改善生存獲益,且無論PD-L1表達如何均可獲益。
基于該項研究,2022年5月,特瑞普利單抗用于治療ESCC的新適應癥上市申請在中國獲批。今年,特瑞普利單抗作為歐洲唯一用于不限PD-L1表達的晚期或轉移性食管鱗癌一線免疫治療藥物獲批上市。
1. 本材料旨在傳遞前沿信息,無意向您做任何產品的推廣,不作為臨床用藥指導。 |
2. 若您想了解具體疾病診療信息,請遵從醫療衛生專業人士的意見與指導。 |
關于鼻咽癌
鼻咽癌是一種發生于鼻咽部黏膜上皮的惡性腫瘤,是常見的頭頸部惡性腫瘤之一。根據GLOBOCAN 2022發布的數據顯示,2022年鼻咽癌在全球范圍內確診的新發病例數超過12萬1。由于原發腫瘤位置的原因,很少采用手術治療。新近更新的ESMO指南推薦免疫治療聯合化療用于復發或轉移性鼻咽癌的一線治療2。
【參考文獻】 |
1. https://gco.iarc.who.int/media/globocan/factsheets/cancers/4-nasopharynx-fact-sheet.pdf. |
2. Bossi, P; Chan, AT; Even, C; Machiels, JP, et al.ESMO-EURACAN Clinical Practice Guideline update for nasopharyngeal carcinoma: adjuvant therapy and first-line treatment of recurrent/metastatic disease. Ann Oncol, 2023; 34 (3): 247. |
關于食管癌
食管癌是消化道領域最常見的惡性腫瘤之一。根據GLOBOCAN 2022發布的數據顯示,食管癌是2022年全球第十一大常見惡性腫瘤和第七大癌癥死亡原因,新發病例數超過51.1萬,死亡病例數超過44.5萬1。食管鱗癌(ESCC)和腺癌是食管癌的兩種主要組織學亞型。ESMO指南推薦PD-1阻斷性抗體聯合化療用于PD-L1表達陽性的晚期或轉移性ESCC的一線治療2。
【參考文獻】 |
1. https://gco.iarc.fr/today/data/factsheets/cancers/6-Oesophagus-fact-sheet.pdf. |
2. Obermannova R,Alsina M, Cervantes A,Leong T,Lordick F, Nilsson M,van Greeken NCT, Vogel A,Smyth EC; ESMO Guidelines Committee. ESMO Clinical Practice Guidline for diagnosis,treatment and follow-up.Ann Oncol.2022 Oct;33(10):992-1004. |
關于特瑞普利單抗注射液(拓益®,LOQTORZI®)
特瑞普利單抗注射液(拓益®)作為我國批準上市的首個國產以PD-1為靶點的單抗藥物,獲得國家科技重大專項項目支持,并榮膺國家專利領域最高獎項"中國專利金獎"
特瑞普利單抗至今已在全球(包括中國、美國、東南亞及歐洲等地)開展了覆蓋超過15個適應癥的40多項由公司發起的臨床研究。正在進行或已完成的關鍵注冊臨床研究在多個瘤種范圍內評估特瑞普利單抗的安全性及療效,包括肺癌、鼻咽癌、食管癌、胃癌、膀胱癌、乳腺癌、肝癌、腎癌及皮膚癌等。
截至目前,特瑞普利單抗已在中國內地獲批10項適應癥:用于既往接受全身系統治療失敗的不可切除或轉移性黑色素瘤的治療(2018年12月);用于既往接受過二線及以上系統治療失敗的復發/轉移性鼻咽癌患者的治療(2021年2月);用于含鉑化療失敗包括新輔助或輔助化療12個月內進展的局部晚期或轉移性尿路上皮癌的治療(2021年4月);聯合順鉑和吉西他濱用于局部復發或轉移性鼻咽癌患者的一線治療(2021年11月);聯合紫杉醇和順鉑用于不可切除局部晚期/復發或遠處轉移性食管鱗癌患者的一線治療(2022年5月);聯合培美曲塞和鉑類用于表皮生長因子受體(EGFR)基因突變陰性和間變性淋巴瘤激酶(ALK)陰性、不可手術切除的局部晚期或轉移性非鱗狀非小細胞肺癌的一線治療(2022年9月);聯合化療圍手術期治療,繼之本品單藥作為輔助治療,用于可切除IIIA-IIIB期非小細胞肺癌的成人患者(2023年12月);聯合阿昔替尼用于中高危的不可切除或轉移性腎細胞癌患者的一線治療(2024年4月);聯合依托泊苷和鉑類用于廣泛期小細胞肺癌一線治療(2024年6月);聯合注射用紫杉醇(白蛋白結合型)用于經充分驗證的檢測評估PD-L1陽性(CPS≥1)的復發或轉移性三陰性乳腺癌的一線治療(2024年6月)。2020年12月,特瑞普利單抗首次通過國家醫保談判,目前已有6項獲批適應癥納入《國家醫保目錄(2023年)》,是目錄中唯一用于治療黑色素瘤的抗PD-1單抗藥物。2024年10月,特瑞普利單抗用于復發/轉移性鼻咽癌治療的適應癥在中國香港獲批。
在國際化布局方面,特瑞普利單抗目前已在美國、歐盟、印度、英國、約旦等國家和地區獲得批準上市。此外,澳大利亞藥品管理局(TGA)和新加坡衛生科學局(HSA)分別受理了特瑞普利單抗聯合順鉑/吉西他濱作為轉移性或復發性局部晚期鼻咽癌成人患者的一線治療,以及作為單藥治療既往含鉑治療過程中或治療后疾病進展的復發性、不可切除或轉移性鼻咽癌的成人患者的上市許可申請。
關于君實生物
君實生物(688180.SH,1877.HK)成立于2012年12月,是一家以創新為驅動,致力于創新療法的發現、開發和商業化的生物制藥公司。依托全球一體化源頭創新研發能力,公司已構建起涵蓋超過50款創新藥物的多層次產品管線,覆蓋惡性腫瘤、自身免疫、慢性代謝類、神經系統、感染性疾病五大治療領域,已有5款產品在國內或海外上市,包括我國首個自主研發、在中美歐等地超過35個國家和地區獲批上市的PD-1抑制劑特瑞普利單抗(拓益®),臨床開發階段的藥物超過30款。疫情期間,君實生物還參與開發了埃特司韋單抗、民得維®等多款預防和治療新冠的創新藥物,積極承擔本土創新藥企的責任。
君實生物以"用世界一流、值得信賴的創新藥普惠患者"為使命,立足中國,布局全球。目前,公司在全球擁有約2500名員工,分布在美國舊金山和馬里蘭,中國上海、蘇州、北京、廣州等。
官方網站:www.junshipharma.com
官方微信:君實生物
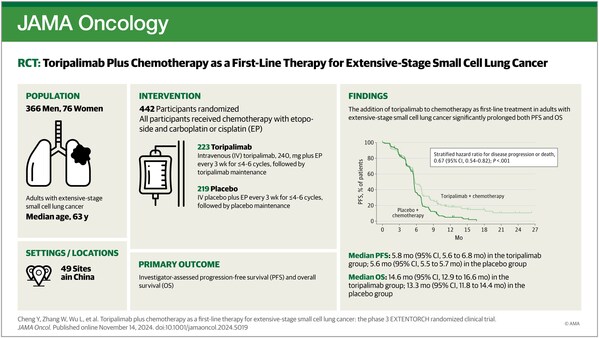
EXTENTORCH研究(NCT04012606)是一項多中心、隨機、雙盲、安慰劑對照的III期臨床研究,旨在比較特瑞普利單抗或安慰劑聯合依托泊苷及鉑類一線治療ES-SCLC的有效性和安全性。
EXTENTORCH研究主要研究者,吉林省腫瘤醫院程穎教授表示:"EXTENTORCH研究作為ES-SCLC領域全球首個成功達到預設雙主要研究終點陽性結果的抗PD-1單抗的Ⅲ期臨床研究,是ES-SCLC治療的又一次關鍵突破。 試驗組1年PFS率提升近4倍,所有亞組患者均有獲益,主要終點之一的OS取得陽性結果,成功通過了臨床‘金標準’的考核,為患者帶來確切生存獲益。本次EXTENTORCH研究見刊不僅公布了特瑞普利單抗聯合化療一線治療ES-SCLC的療效數據,更重要的是,這項研究進行了分子層面的探索,對篩選接受免疫治療的患者具有重要的指導意義。"
2023年5月,EXTENTORCH研究主要終點無進展生存期(PFS)和總生存期(OS)均達到方案預設的優效邊界,特瑞普利單抗由此成為全球首個在ES-SCLC一線治療III期研究中取得預設雙重主要終點陽性結果的PD-1抑制劑。
2024年6月,基于該研究的積極結果,特瑞普利單抗獲國家藥品監督管理局(NMPA)正式批準聯合依托泊苷和鉑類用于ES-SCLC一線治療,并獲中國臨床腫瘤學會(CSCO)兩大指南推薦為ES-SCLC一線治療優選方案,為中國ES-SCLC患者提供了治療新選擇。
此前,EXTENTORCH研究以口頭報告的形式在2023年ESMO大會上首次公布了研究數據,此次全文發表于國際期刊,彰顯了國際學者對這項研究及特瑞普利單抗的肯定,結果顯示:
- 與單純化療相比,特瑞普利單抗聯合化療顯著改善患者PFS和OS,將疾病進展或死亡風險降低33%(HR=0.67;95% CI, 0.54-0.82),死亡風險降低了20%(HR=0.80;95% CI, 0.65-0.98)。亞組分析顯示,所有關鍵亞組均顯示出一致的PFS和OS獲益。
- 生物標志物探索分析顯示,在特瑞普利單抗聯合化療組中,具有低腫瘤內異質性(ITH),HLA-A11+ HLA-B62-單倍型,KMT2D 和COL4A4野生型,或CTNNA2/SCN4A序列變異的患者的臨床獲益更明顯。
- 特瑞普利單抗聯合化療的安全性良好,未發現新的安全信號。兩組在治療期間出現的不良事件(TEAE,99.5%vs100%)和≥3級TEAE(89.6%vs89.4%)的發生率相似。
君實生物總經理兼首席執行官鄒建軍博士表示: “此次EXTENTORCH的重磅研究成果獲得《美國醫學會雜志·腫瘤學》發表,體現了國際學術界對以特瑞普利單抗為代表的免疫治療在ES-SCLC患者一線治療中的價值認可。肺癌一直是公司重點關注的疾病領域,截至目前,特瑞普利單抗已成功獲批包括非小細胞肺癌(NSCLC)和小細胞肺癌(SCLC)在內的3項適應癥,覆蓋了早中期(圍手術期)至晚期人群,管線內也還有其他產品正處于攻關階段,我們會積極推進相關工作,期待能為全球肺癌患者帶來更多更優的創新方案。"
1. 本材料旨在傳遞前沿信息,無意向您做任何產品的推廣,不作為臨床用藥指導。
2. 若您想了解具體疾病診療信息,請遵從醫療衛生專業人士的意見與指導。
關于EXTENTORCH研究
EXTENTORCH研究(NCT04012606)是一項多中心、隨機、雙盲、安慰劑對照的III期臨床研究,旨在比較特瑞普利單抗或安慰劑聯合依托泊苷及鉑類一線治療ES-SCLC的有效性和安全性。研究納入既往未接受系統治療的ES-SCLC患者,以1:1的比例隨機接受特瑞普利單抗(240mg, Q3W)或安慰劑聯合依托泊苷(100mg/m2, Q3W)和鉑類(順鉑 75 mg/m2或卡鉑 AUC 5 mg/mL/min, Q3W)治療4~6個周期,之后接受特瑞普利單抗或安慰劑維持治療,直至疾病進展、出現不可耐受的毒性或完成2年治療。研究分層因素包括性別和基線ECOG體能狀況評分。主要終點為研究者根據RECIST v1.1評估的PFS和OS。次要終點包括盲態獨立中心審查(BICR)評估的PFS、客觀緩解率(ORR)、疾病控制率(DCR)、疾病緩解率(DOR)和安全性等。探索性終點包括PD-L1的表達、腫瘤突變負荷(TMB)和其他基于測序的與臨床療效相關的生物標志物。
自2019年9月至2021年5月,研究共納入442例ES-SCLC患者,隨機分配至特瑞普利單抗聯合化療組(n=223)或安慰劑聯合化療組(n=219)。該研究由程穎教授擔任主要研究者,在全國49家臨床中心聯合開展。
關于特瑞普利單抗注射液(拓益®)
特瑞普利單抗注射液(拓益®)作為我國批準上市的首個國產以PD-1為靶點的單抗藥物,獲得國家科技重大專項項目支持,并榮膺國家專利領域最高獎項"中國專利金獎"。
特瑞普利單抗至今已在全球(包括中國、美國、東南亞及歐洲等地)開展了覆蓋超過15個適應癥的40多項由公司發起的臨床研究。正在進行或已完成的關鍵注冊臨床研究在多個瘤種范圍內評估特瑞普利單抗的安全性及療效,包括肺癌、鼻咽癌、食管癌、胃癌、膀胱癌、乳腺癌、肝癌、腎癌及皮膚癌等。
截至目前,特瑞普利單抗已在中國內地獲批10項適應癥:用于既往接受全身系統治療失敗的不可切除或轉移性黑色素瘤的治療(2018年12月);用于既往接受過二線及以上系統治療失敗的復發/轉移性鼻咽癌患者的治療(2021年2月);用于含鉑化療失敗包括新輔助或輔助化療12個月內進展的局部晚期或轉移性尿路上皮癌的治療(2021年4月);聯合順鉑和吉西他濱用于局部復發或轉移性鼻咽癌患者的一線治療(2021年11月);聯合紫杉醇和順鉑用于不可切除局部晚期/復發或遠處轉移性食管鱗癌患者的一線治療(2022年5月);聯合培美曲塞和鉑類用于表皮生長因子受體(EGFR)基因突變陰性和間變性淋巴瘤激酶(ALK)陰性、不可手術切除的局部晚期或轉移性非鱗狀非小細胞肺癌的一線治療(2022年9月);聯合化療圍手術期治療,繼之本品單藥作為輔助治療,用于可切除IIIA-IIIB期非小細胞肺癌的成人患者(2023年12月);聯合阿昔替尼用于中高危的不可切除或轉移性腎細胞癌患者的一線治療(2024年4月);聯合依托泊苷和鉑類用于廣泛期小細胞肺癌一線治療(2024年6月);聯合注射用紫杉醇(白蛋白結合型)用于經充分驗證的檢測評估PD-L1陽性(CPS≥1)的復發或轉移性三陰性乳腺癌的一線治療(2024年6月)。2020年12月,特瑞普利單抗首次通過國家醫保談判,目前已有6項獲批適應癥納入《國家醫保目錄(2023年)》,是目錄中唯一用于治療黑色素瘤的抗PD-1單抗藥物。2024年10月,特瑞普利單抗用于復發/轉移性鼻咽癌治療的適應癥在中國香港獲批。
在國際化布局方面,特瑞普利單抗已作為首款鼻咽癌藥物在美國和印度獲批上市,其用于晚期鼻咽癌和食管鱗癌的一線治療獲得歐盟委員會批準上市。此外,英國藥品和保健品管理局(MHRA)受理了特瑞普利單抗聯合順鉑和吉西他濱用于局部復發或轉移性鼻咽癌患者的一線治療以及聯合紫杉醇和順鉑用于不可切除局部晚期/復發或轉移性食管鱗癌患者的一線治療的上市許可申請,澳大利亞藥品管理局(TGA)和新加坡衛生科學局(HSA)分別受理了特瑞普利單抗聯合順鉑/吉西他濱作為轉移性或復發性局部晚期鼻咽癌成人患者的一線治療,以及作為單藥治療既往含鉑治療過程中或治療后疾病進展的復發性、不可切除或轉移性鼻咽癌的成人患者的上市許可申請。
關于君實生物
君實生物(688180.SH, 1877.HK)成立于2012年12月,是一家以創新為驅動,致力于創新療法的發現、開發和商業化的生物制藥公司。依托全球一體化源頭創新研發能力,公司已構建起涵蓋超過50款創新藥物的多層次產品管線,覆蓋惡性腫瘤、自身免疫、慢性代謝類、神經系統、感染性疾病五大治療領域,已有5款產品在國內或海外上市,包括我國首個自主研發、在中美歐等地超過30個國家和地區獲批上市的PD-1抑制劑特瑞普利單抗(拓益®),臨床開發階段的藥物超過30款。疫情期間,君實生物還參與開發了埃特司韋單抗、民得維®等多款預防和治療新冠的創新藥物,積極承擔本土創新藥企的責任。
君實生物以"用世界一流、值得信賴的創新藥普惠患者"為使命,立足中國,布局全球。目前,公司在全球擁有約2500名員工,分布在美國舊金山和馬里蘭,中國上海、蘇州、北京、廣州等。
官方網站:www.junshipharma.com
官方微信:君實生物
《中國血脂管理指南(2023年)》[1]指出,心血管疾病是我國城鄉居民第一位死因,其中以動脈粥樣硬化性心血管疾病(ASCVD)為主。低密度脂蛋白膽固醇(LDL-C)水平升高是ASCVD的致病性危險因素,通過降低LDL-C水平可顯著減少ASCVD的發病及死亡危險。雖然現有的以他汀類藥物為基礎的降脂治療可顯著降低LDL-C水平及ASCVD風險,但ASCVD高風險人群的LDL-C降脂達標率現狀仍然堪憂,尤其是ASCVD超高危/極高危患者,LDL-C達標率更低,臨床上仍存在較大的未滿足的降脂治療需求。
本次獲批主要基于兩項多中心、隨機、雙盲、安慰劑對照的Ⅲ期臨床研究JS002-003(NCT04781114)和JS002-006(NCT05532800)。
其中,JS002-003研究由中國人民解放軍北部戰區總醫院韓雅玲院士擔任主要研究者,旨在中國原發性高膽固醇血癥和混合型血脂異常患者中評估昂戈瑞西單抗皮下注射治療的療效和安全性,共入組806例患者。其研究成果在2023年美國心臟協會科學會議(AHA)首次公布,并于2024年5月獲得AHA官方雜志《美國心臟協會雜志》(Journal of the American Heart Association,JAHA,影響因子:6.106)全文發表。JS002-003研究結果顯示[2],相較安慰劑,昂戈瑞西單抗150mg每2周一次(Q2W)或300mg每4周一次(Q4W)皮下注射,可顯著降低LDL-C水平達60%以上,且在52周的治療期間始終維持穩定的降幅,同時對其他血脂參數,如非高密度脂蛋白膽固醇(non-HDL-C)、載脂蛋白B(Apo B)和總膽固醇(TC)也有明顯的改善作用;安全性良好,未發現新的安全信號。
JS002-006研究由中南大學湘雅二醫院趙水平教授擔任主要研究者,旨在原發性高膽固醇血癥和混合型高脂血癥患者中評價使用兩種給藥裝置【預充式注射器(PFS)和預充式自動注射器(AI)】皮下注射昂戈瑞西單抗的有效性和安全性,共入組255例患者。其研究成果于2024年5月獲得內分泌學與代謝領域國際學術期刊《營養代謝與心血管疾病雜志》(Nutrition Metabolism And Cardiovascular Diseases,NMCD)全文發表。結果顯示[3],無論昂戈瑞西單抗PFS還是AI給藥,均表現出相當的顯著降脂作用,與安慰劑相比,患者接受昂戈瑞西單抗150mg Q2W治療12周時,LDL-C水平顯著降低70%以上(PFS組72.7%,AI組71.1%),且安全性良好。
目前,昂戈瑞西單抗另有兩項新適應癥上市申請正在接受NMPA審評,分別為:1)雜合子型家族性高膽固醇血癥;2)他汀類藥物不耐受或禁忌使用的原發性高膽固醇血癥和混合型血脂異常(單藥)。
中南大學湘雅二醫院趙水平教授表示:"昂戈瑞西單抗正式獲批是個令人振奮的消息,這將為他汀類等藥物降脂效果不佳的原發性高膽固醇血癥和混合型高脂血癥患者提供一種全新的治療選擇,為了兼顧患者給藥的易用性和便利性,除通過PFS給藥外,還開發了AI給藥方式,可省去由醫護人員進行注射給藥的過程,以實現居家給藥等可能增加患者便利性的用藥場景。結果顯示,無論昂戈瑞西單抗PFS還是AI給藥,昂戈瑞西單抗均表現出相當的顯著降脂作用,希望其能夠盡快到達患者手中早日惠及更多患者。"
君實生物總經理兼首席執行官鄒建軍博士表示:"君適達®是君實生物的第5款商業化產品,成功將我們的治療領域從腫瘤、自身免疫、感染性疾病拓寬到了慢性代謝類疾病,這在進一步豐富公司產品矩陣的同時,無感染性疾病拓寬到了慢性代謝類疾病,這在進一步豐富公司產品矩陣的同時,無疑是對公司全鏈條新質生產力的又一有力背書。ASCVD是人類健康的頭號殺手,昂戈瑞西單抗的獲批上市,勢必將成為ASCVD患者對抗疾病的有力手段。同時,關于昂戈瑞西單抗還有另外2項適應癥正在審評中,期待后續能夠為更廣泛的ASCVD患者群體帶來更多的治療選擇。"
【參考文獻】 |
[1] 中國血脂管理指南(2023年). 中國循環雜志. 2023 38;3:237-271. |
[2] Wang X, Qiu M, Cheng Z, et al. Efficacy and Safety of Ongericimab in Chinese Patients With Primary Hypercholesterolemia and Mixed Dyslipidemia. J Am Heart Assoc. 2024 May 31:e033669. |
[3] Zhao W et al., Efficacy and safety of ongericimab given by prefilled syringe or autoinjector in primaryl hypercholesterolemia and mixed hyperlipidemia, Nutrition, Metabolism & Cardiovascular Diseases, https://doi.org/10.1016/j.numecd.2024.04.011 |
*完整適應癥名稱為:在控制飲食的基礎上,與他汀類藥物、或者與他汀類藥物和依折麥布聯合用藥,用于在接受中等劑量或中等劑量以上他汀類藥物治療,仍無法達到低密度脂蛋白膽固醇(LDL-C)目標的原發性高膽固醇血癥(非家族性)和混合型血脂異常的成人患者 |
1. 本材料旨在傳遞前沿信息,無意向您做任何產品的推廣,不作為臨床用藥指導。 |
2. 若您想了解具體疾病診療信息,請遵從醫療衛生專業人士的意見與指導。 |
關于昂戈瑞西單抗注射液(君適達®)
昂戈瑞西單抗注射液(君適達®)是君實生物自主研發的注射用重組人源化抗PCSK9單克隆抗體,于2024年10月獲批上市,用于治療原發性高膽固醇血癥(非家族性)和混合型血脂異常的成人患者,規格為150mg(1ml)/支(預充式注射器)、150mg(1ml)/支(預充式自動注射器)。君實生物是國內首家獲得該靶點藥物臨床試驗批件的中國企業。
2023年10月,君實生物與重慶博創醫藥有限公司(博創醫藥)達成合作,授予博創醫藥在中國大陸和許可用途內研發、生產、商業化昂戈瑞西單抗的獨占許可。
2024年4月,國家藥品監督管理局(NMPA)受理了昂戈瑞西單抗的2項新適應癥上市申請,用于治療:1)雜合子型家族性高膽固醇血癥;2)他汀類藥物不耐受或禁忌使用的原發性高膽固醇血癥和混合型血脂異常(單藥)。
關于君實生物
君實生物(688180.SH,1877.HK)成立于2012年12月,是一家以創新為驅動,致力于創新療法的發現、開發和商業化的生物制藥公司。依托全球一體化源頭創新研發能力,公司已構建起涵蓋超過50款創新藥物的多層次產品管線,覆蓋惡性腫瘤、自身免疫、慢性代謝類、神經系統、感染性疾病五大治療領域,已有4款產品在國內或海外上市,包括我國首個自主研發、在中美歐三地獲批上市的PD-1抑制劑特瑞普利單抗(拓益®),臨床開發階段的藥物超過30款。疫情期間,君實生物還參與開發了埃特司韋單抗、民得維®等多款預防和治療新冠的創新藥物,積極承擔本土創新藥企的責任。
君實生物以"用世界一流、值得信賴的創新藥普惠患者"為使命,立足中國,布局全球。目前,公司在全球擁有約2500名員工,分布在美國舊金山和馬里蘭,中國上海、蘇州、北京、廣州等。
官方網站:www.junshipharma.com
官方微信:君實生物
值得注意的是,針對晚期黑色素瘤和肝癌一線治療的兩項Ⅲ期注冊臨床研究,在本屆CSCO學術年會上進行了首次數據分享,研究取得了可喜的成果。這是君實生物在一線治療領域又一令人振奮的進展。
CSCO學術年會由中國臨床腫瘤學會(CSCO)主辦,是中國臨床腫瘤學界最活躍的專業學術組織,也是我國知名度最高、最權威的醫學科技學術性團體之一。今年的大會主題為"以患為本,共享未來",旨在進一步促進國內臨床腫瘤學領域的學術交流和科技合作,鼓勵支持臨床研究和創新,提倡多學科規范化綜合治療基礎上的精準腫瘤學,積極推動學科大發展。
MELATORCH結果首發 有望成為晚期黑色素瘤一線免疫治療新選擇
黑色素瘤是惡性程度最高的皮膚癌類型,2022年全球新發病例約33.2萬,死亡病例約5.9萬[1]。黑色素瘤在我國相對少見,但病死率高(2022年新發病例約0.9萬,而死亡病例達到0.5萬)[2],且發病率還在逐年增加[3]。2018年抗PD-1單抗在國內首次獲批用于晚期黑色素瘤二線及以上治療,但傳統化療或靶向治療(僅適用于攜帶BRAF V600突變的患者)仍然長期作為晚期一線的標準治療。因此,國內晚期黑色素瘤患者對于一線免疫治療的臨床需求較為迫切。
MELATORCH研究(NCT03430297)是一項多中心、隨機、開放、陽性藥對照的Ⅲ期臨床研究,也是目前國內首個達成陽性結果的PD-(L)1抑制劑一線治療晚期黑色素瘤的關鍵注冊臨床研究。該研究旨在比較特瑞普利單抗對比達卡巴嗪在既往未接受系統抗腫瘤治療的不可切除或轉移性黑色素瘤患者中的有效性和安全性,由北京大學腫瘤醫院郭軍教授擔任主要研究者,在全國11家臨床中心開展,共納入255例患者并進入全分析集(特瑞普利單抗組127例,達卡巴嗪組128例)。
9月26日下午,郭軍教授在大會創新藥物臨床研究數據專場作口頭報告了MELATORCH的研究結果:
- 研究達到主要終點,與達卡巴嗪相比,特瑞普利單抗治療顯著延長患者無進展生存期(PFS),盲態獨立中心閱片(BICR)評估的中位PFS分別為2.3 vs. 2.1個月,疾病進展或死亡風險降低29.2%(HR=0.708;95% CI: 0.526-0.954),P=0.0209。
- 特瑞普利單抗組的客觀緩解率(ORR)高于達卡巴嗪組,兩組BICR和研究者評估的ORR分別為11.0% vs. 8.6%、12.6% vs. 9.4%,且緩解持續時間(DoR)較達卡巴嗪組顯示出明顯的延長趨勢,BICR和研究者評估的中位DoR分別為13.8 vs. 6.9個月、16.1 vs. 8.0個月。
- 矯正后續抗腫瘤治療影響的OS敏感性分析結果顯示,與達卡巴嗪組相比,特瑞普利單抗治療組顯示出明顯的生存獲益趨勢,中位OS分別為15.1 vs. 9.4個月(HR=0.680,95%CI:0.486-0.951)。
特瑞普利單抗的安全性良好,與既往研究一致,未發現新的安全信號。
MELATORCH研究的主要研究者、CSCO黑色素瘤專委會主任委員、北京大學腫瘤醫院郭軍教授表示:"黑色素瘤的惡性程度較高且治療效果受到人種差異的影響,因此,找到適合國人的藥物和治療方案尤為重要。此次發表的MELATORCH為本土黑色素瘤患者接受一線免疫治療提供了扎實的循證證據,結果表明,免疫治療相對標準化療能夠顯著提升PFS、ORR和DoR,且OS的獲益趨勢明顯。目前,特瑞普利單抗已在晚期黑色素瘤的全線治療中顯示出巨大的臨床價值,這不僅為我國黑色素瘤患者點燃了希望,同時也為適合本土的藥物方案探索之路指明了方向,期待更多中國黑色素瘤患者能夠通過免疫治療獲益。"
2024年8月,基于MELATORCH研究結果,國家藥品監督管理局(NMPA)受理了特瑞普利單抗用于不可切除或轉移性黑色素瘤一線治療的新適應癥上市申請。
HEPATORCH重磅發布 靶免聯合助力晚期肝癌患者更長生存
肝癌是世界范圍內常見的消化系統惡性腫瘤,病理類型以肝細胞癌(HCC)為主(約占90%)[4]。根據GLOBOCAN 2022報告,2022年全球肝癌的年新發病例數和死亡例數分別為86.6萬和75.9萬[5]。
我國是肝癌大國,2022年肝癌新發病例數達到36.8萬(占全球病例的42.4%),居國內惡性腫瘤第4位,死亡31.7萬(占全球病例的41.7%),居國內惡性腫瘤第2位[6]。由于起病隱匿,約70%-80%的中國肝癌患者首次診斷時已是中晚期[7],中位OS僅約10個月,5年生存率約12%[8]。
9月27日下午,復旦大學附屬中山醫院史穎弘教授在大會上首次口頭報告了特瑞普利單抗聯合貝伐珠單抗一線治療晚期肝細胞癌(HCC)的Ⅲ期HEPATORCH研究結果。
HEPATORCH是一項多中心、隨機、開放、陽性藥對照的Ⅲ期臨床研究,在中國大陸、中國臺灣和新加坡的57家臨床中心開展,共入組326例患者。研究旨在評估與標準治療索拉非尼相比,特瑞普利單抗聯合貝伐珠單抗一線治療不可切除或轉移性HCC的有效性和安全性。
史穎弘教授指出,HEPATORCH研究的主要研究終點基于獨立影像評估的PFS和總生存期(OS)達到"雙終點陽性結果"。
- 與索拉非尼相比,特瑞普利單抗聯合貝伐珠單抗可顯著延長PFS和OS,兩組中位PFS分別為5.8 vs. 4.0個月,疾病進展或死亡風險降低31%(HR=0.69,95% CI:0.525-0.913;P=0.0086);兩組中位OS分別為20.0 vs. 14.5個月,死亡風險降低24%(HR=0.76,95% CI:0.579-0.987;P=0.0394)。
- 特瑞普利單抗聯合貝伐珠單抗組客觀緩解率(ORR)較索拉非尼組明顯提高,兩組ORR分別為25.3% vs. 6.1%。
- 特瑞普利單抗聯合貝伐珠單抗在晚期HCC患者中的安全性良好,毒性譜與已知單藥毒性譜一致,未發現新的安全信號。
HEPATORCH研究主要研究者、中國科學院院士、復旦大學附屬中山醫院樊嘉教授表示:"近年來,晚期肝癌一線治療策略發生了顯著變化,特別是免疫治療的引入以及以免疫治療藥物為基礎的聯合方案的出現徹底顛覆了傳統的治療格局,為晚期肝癌患者帶來全新的治療選擇。此次公布的HEPATORCH研究結果令人欣慰且讓我們備受鼓舞,相對靶向藥物單藥,特瑞普利單抗聯合貝伐珠單抗一線治療晚期HCC顯示出更優PFS、ORR和OS,這一成果不僅能為晚期肝癌患者提供新的治療選擇,也可進一步推動靶免聯合治療方案在肝癌領域中的推廣應用,為提升我國肝癌患者的生存率和生活質量貢獻力量!"
2024年7月,基于HEPATORCH研究結果,國家藥品監督管理局(NMPA)正式受理了特瑞普利單抗聯合貝伐珠單抗用于不可切除或轉移性HCC患者一線治療的新適應癥上市申請。
"星光益熠 十全實美"攜手奔赴新征程
9月27日下午,以"星光益熠,十全實美"為主題的我和CSCO君實生物專場會議成功舉辦。大會主席由中山大學腫瘤防治中心徐瑞華教授、山東省腫瘤醫院于金明院士、中國藥科大學附屬南京天印山醫院秦叔逵教授、復旦大學附屬中山醫院樊嘉院士聯合擔任。解放軍總醫院江澤飛教授、北京大學腫瘤醫院郭軍教授、吉林省腫瘤醫院程穎教授、中國醫學科學院腫瘤醫院王潔教授、復旦大學附屬中山醫院周儉教授、同濟大學附屬東方醫院周彩存教授、上海交通大學附屬胸科醫院陸舜教授、北京大學腫瘤醫院沈琳教授共同出席。
會議匯聚了國內頂尖的腫瘤學專家、學者及行業領袖,共同探討了以特瑞普利單抗為代表的腫瘤免疫治療的最新進展與未來方向。同時各位專家對特瑞普利單抗作為首款國產PD-1抗體藥物已獲批了十項適應癥表達了祝賀,一致認為這一歷程不僅是數字上的增長,也是患者生存時間和生命質量的顯著提升,更是中國醫學進步的重要見證。
在談及特瑞普利單抗在美歐相繼獲批時,現場專家一致認為國產創新藥在腫瘤領域具備很大優勢,對未來中國創新、中國方案走向全球充滿信心。
君實生物總經理兼首席執行官鄒建軍博士表示:"每年的CSCO學術年會都是一場盛大的學術盛宴,非常榮幸能夠見證特瑞普利單抗的多項重磅成果在大會發布。迄今為止,特瑞普利單抗已在國際大會上報告超300次,發表文章400篇以上,影響因子累計2900+分,是首個且目前唯一同時被NCCN、ESMO和CSCO三大權威指南推薦的中國抗PD-1單抗藥物。同時,該產品已在中、美、歐三地獲批上市,覆蓋10大適應癥,另有多個適應癥正在接受多國審評。取得如此成績,要非常感謝各位研究者在研究全程中的辛勤付出。未來,君實生物將繼續聚焦優勢領域,強化研發創新,以期開發更多更新的產品及適應癥惠及廣大患者。"
【參考文獻】
1. 《靶免聯合局部治療 中晚期肝細胞癌中國專家共識》, 肝癌電子雜志, 2023, 10(3): 1-11. |
2. Zeng H, Chen W, Zheng R, et al. Changing cancer survival in China during 2003-15: a pooled analysis of 17 population-based cancer registries. Lancet Glob Health. 2018;6(5):e555-e567. |
3. 中華人民共和國國家衛生健康委員會黑色素瘤診療指南(2022年版). |
4. Hepatocellular carcinoma. Nat Rev Dis Primers. 2021;7(1):7. |
5. Bray F, Laversanne M, Sung H, et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2024;74(3):229-263. |
6. Zheng RS, Chen R, Han BF, et al. Zhonghua Zhong Liu Za Zhi. 2024;46(3):221-231. |
7. https://gco.iarc.who.int/media/globocan/factsheets/cancers/16-melanoma-of-skin-fact-sheet.pdf. |
8. https://gco.iarc.who.int/media/globocan/factsheets/populations/160-china-fact-sheet.pdf. |
1. 本材料旨在傳遞前沿信息,無意向您做任何產品的推廣,不作為臨床用藥指導。
2. 若您想了解具體疾病診療信息,請遵從醫療衛生專業人士的意見與指導。
關于特瑞普利單抗注射液(拓益®)
特瑞普利單抗注射液(拓益®)作為我國批準上市的首個國產以PD-1為靶點的單抗藥物,獲得國家科技重大專項項目支持,并榮膺國家專利領域最高獎項"中國專利金獎"。
特瑞普利單抗至今已在全球(包括中國、美國、東南亞及歐洲等地)開展了覆蓋超過15個適應癥的40多項由公司發起的臨床研究。正在進行或已完成的關鍵注冊臨床研究在多個瘤種范圍內評估特瑞普利單抗的安全性及療效,包括肺癌、鼻咽癌、食管癌、胃癌、膀胱癌、乳腺癌、肝癌、腎癌及皮膚癌等。
截至目前,特瑞普利單抗已在中國內地獲批10項適應癥:用于既往接受全身系統治療失敗的不可切除或轉移性黑色素瘤的治療(2018年12月);用于既往接受過二線及以上系統治療失敗的復發/轉移性鼻咽癌患者的治療(2021年2月);用于含鉑化療失敗包括新輔助或輔助化療12個月內進展的局部晚期或轉移性尿路上皮癌的治療(2021年4月);聯合順鉑和吉西他濱用于局部復發或轉移性鼻咽癌患者的一線治療(2021年11月);聯合紫杉醇和順鉑用于不可切除局部晚期/復發或遠處轉移性食管鱗癌患者的一線治療(2022年5月);聯合培美曲塞和鉑類用于表皮生長因子受體(EGFR)基因突變陰性和間變性淋巴瘤激酶(ALK)陰性、不可手術切除的局部晚期或轉移性非鱗狀非小細胞肺癌的一線治療(2022年9月);聯合化療圍手術期治療,繼之本品單藥作為輔助治療,用于可切除IIIA-IIIB期非小細胞肺癌的成人患者(2023年12月);聯合阿昔替尼用于中高危的不可切除或轉移性腎細胞癌患者的一線治療(2024年4月);聯合依托泊苷和鉑類用于廣泛期小細胞肺癌一線治療(2024年6月);聯合注射用紫杉醇(白蛋白結合型)用于經充分驗證的檢測評估PD-L1陽性(CPS≥1)的復發或轉移性三陰性乳腺癌的一線治療(2024年6月)。2020年12月,特瑞普利單抗首次通過國家醫保談判,目前已有6項獲批適應癥納入《國家醫保目錄(2023年)》,是目錄中唯一用于治療黑色素瘤的抗PD-1單抗藥物。2024年4月,香港衛生署藥物辦公室受理了特瑞普利單抗聯合順鉑/吉西他濱作為轉移性或復發性局部晚期鼻咽癌成人患者的一線治療,以及作為單藥治療既往含鉑治療過程中或治療后疾病進展的復發性、不可切除或轉移性鼻咽癌的成人患者的上市許可申請。
在國際化布局方面,2023年10月,特瑞普利單抗已作為首款鼻咽癌藥物在美國獲批上市。2024年9月,特瑞普利單抗用于晚期鼻咽癌和食管鱗癌的一線治療獲得歐盟委員會批準上市。此外,英國藥品和保健品管理局(MHRA)受理了特瑞普利單抗聯合順鉑和吉西他濱用于局部復發或轉移性鼻咽癌患者的一線治療以及聯合紫杉醇和順鉑用于不可切除局部晚期/復發或轉移性食管鱗癌患者的一線治療的上市許可申請,澳大利亞藥品管理局(TGA)和新加坡衛生科學局(HSA)分別受理了特瑞普利單抗聯合順鉑/吉西他濱作為轉移性或復發性局部晚期鼻咽癌成人患者的一線治療,以及作為單藥治療既往含鉑治療過程中或治療后疾病進展的復發性、不可切除或轉移性鼻咽癌的成人患者的上市許可申請。
關于君實生物
君實生物(688180.SH,1877.HK)成立于2012年12月,是一家以創新為驅動,致力于創新療法的發現、開發和商業化的生物制藥公司。依托全球一體化源頭創新研發能力,公司已構建起涵蓋超過50款創新藥物的多層次產品管線,覆蓋惡性腫瘤、自身免疫、慢性代謝類、神經系統、感染性疾病五大治療領域,已有4款產品在國內或海外上市,包括我國首個自主研發、在中美兩國獲批上市的PD-1抑制劑特瑞普利單抗(拓益®),臨床開發階段的藥物超過30款。疫情期間,君實生物還參與開發了埃特司韋單抗、民得維®等多款預防和治療新冠的創新藥物,積極承擔本土創新藥企的責任。
君實生物以"用世界一流、值得信賴的創新藥普惠患者"為使命,立足中國,布局全球。目前,公司在全球擁有約2500名員工,分布在美國舊金山和馬里蘭,中國上海、蘇州、北京、廣州等。
官方網站:www.junshipharma.com
官方微信:君實生物
上海2024年9月24日 /美通社/ -- 北京時間2024年9月24日,君實生物(1877.HK,688180.SH)宣布,由公司自主研發的抗PD-1單抗藥物特瑞普利單抗(歐洲商品名:LOQTORZI®)于近日獲得歐盟委員會(EC)批準用于治療兩項適應癥:
- 特瑞普利單抗聯合順鉑和吉西他濱用于復發、不能手術或放療的,或轉移性鼻咽癌(NPC)成人患者的一線治療;
- 特瑞普利單抗聯合順鉑和紫杉醇用于不可切除的晚期/復發或轉移性食管鱗癌(ESCC)成人患者的一線治療。
2024年7月,歐洲藥品管理局(EMA)人用醫藥產品委員會(CHMP)發布積極審評意見,建議批準特瑞普利單抗用于以上兩項適應癥。此次獲批適用于歐盟全部27個成員國以及冰島、挪威和列支敦士登,使得特瑞普利單抗成為歐洲首個且唯一用于NPC治療的藥物,也是歐洲唯一用于不限PD-L1表達的晚期或轉移性ESCC一線免疫治療藥物。
本次EC對于NPC和ESCC適應癥的批準分別基于JUPITER-02(一項隨機、雙盲、安慰劑對照、國際多中心Ⅲ期臨床研究,NCT03581786)和JUPITER-06(一項隨機、雙盲、安慰劑對照、多中心的Ⅲ期研究,NCT03829969)的研究結果。
其中,JUPITER-02是鼻咽癌免疫治療領域首個國際多中心、樣本量最大的雙盲、隨機對照Ⅲ期臨床研究,也是全球首個鼻咽癌一線免疫聯合化療對比單純化療將總生存期(OS)預設有統計學檢驗(一類錯誤控制)并確證具有生存獲益的Ⅲ期臨床研究。其研究結果曾以口頭報告形式亮相2021年美國臨床腫瘤學會(ASCO)年會全體大會(#LBA2),隨后榮登《自然-醫學》(Nature Medicine,影響因子:58.7)雜志封面,并獲得《美國醫學會雜志》(Journal of the American Medical Association,JAMA,影響因子:63.1)全文發表。研究結果顯示,與單純化療相比,特瑞普利單抗聯合化療使患者的疾病進展風險降低48%,死亡風險降低37%。特瑞普利單抗聯合化療組的中位無進展生存期(PFS)對比單純化療延長了13.2個月,從8.2個月提升到21.4個月。此外,接受該聯合療法治療的患者可獲得更高的客觀緩解率(ORR),更長的持續緩解時間(DoR)和更高的疾病控制率(DCR),且未發現新的安全性信號。長期生存隨訪數據在2024年ASCO年會展示,特瑞普利單抗治療組5年生存率達到52.0%。
基于該項研究,特瑞普利單抗分別于2021年和2023年獲得國家藥品監督管理局(NMPA)和美國食品藥品監督管理局(FDA)批準用于晚期鼻咽癌的治療,是全球首個獲批鼻咽癌治療的免疫檢查點抑制劑(ICI)藥物,也是美國首個且唯一用于鼻咽癌治療的藥物。此外,特瑞普利單抗用于治療NPC相關適應癥的上市申請正在同步接受英國藥品和保健品管理局(MHRA)、澳大利亞藥品管理局(TGA)、新加坡衛生科學局(HSA)以及中國香港衛生署藥物辦公室(DO)等國家和地區監管機構的審評。
JUPITER-06是一項隨機、雙盲、安慰劑對照、多中心的Ⅲ期臨床研究(NCT03829969),旨在評估與安慰劑聯合化療相比,特瑞普利單抗聯合紫杉醇/順鉑(TP)用于晚期ESCC一線治療的療效及安全性。該研究結果首次在歐洲腫瘤內科學會年會(ESMO 2021)上以口頭匯報形式報告,隨后在國際頂尖腫瘤學雜志《Cancer Cell》(影響因子:48.8)和《臨床腫瘤學雜志》(Journal of Clinical Oncology,影響因子:42.1)發表。研究結果顯示,特瑞普利單抗聯合化療可使晚期或轉移性ESCC患者獲得更優的PFS和OS,其中中位OS延長6個月,達到17個月,并顯著降低患者的疾病進展或死亡風險達42%,顯著改善生存獲益,且無論PD-L1表達如何均可獲益。
基于該項研究,2022年5月,特瑞普利單抗用于治療ESCC的新適應癥上市申請在中國獲批。目前,特瑞普利單抗用于一線治療ESCC的上市申請正在接受MHRA的審評。
JUPITER-02、JUPITER-06主要研究者、中山大學腫瘤防治中心徐瑞華教授表示:"鼻咽癌和食管癌都具有亞洲區域高發的特點,歐美國家在此類瘤種領域的創新療法開發方面較為緩慢。JUPITER-02和JUPITER-06研究的出色的研究成果證明了在鼻咽癌和食管癌領域,中國學者的診療能力和臨床科研水平已經位列全球領先,期待這項‘中國方案'能夠切實改變國際上罹患這兩類瘤種且缺乏有效治療手段的患者境遇,為他們帶來更好的生存希望!"
君實生物總經理兼首席執行官鄒建軍博士表示:"‘立足中國,布局全球'是君實生物創立之初即確立的戰略發展目標,此次特瑞普利單抗獲得EC批準,意味著繼中國、美國之后,我們全球商業化布局的腳步正式邁向歐洲,也標志著我們在創新藥的研發和生產質量再次獲得國際權威監管機構的認可。未來,我們將繼續攜手合作伙伴,全力推動特瑞普利單抗在歐洲地區的商業化落地,為更多海外患者提供來自中國的高質量創新藥物。"
1. 本材料旨在傳遞前沿信息,無意向您做任何產品的推廣,不作為臨床用藥指導。 |
2. 若您想了解具體疾病診療信息,請遵從醫療衛生專業人士的意見與指導。 |
—— 完 ——
關于鼻咽癌
鼻咽癌是一種發生于鼻咽部黏膜上皮的惡性腫瘤,是常見的頭頸部惡性腫瘤之一。根據GLOBOCAN 2022發布的數據顯示,2022年鼻咽癌在全球范圍內確診的新發病例數超過12萬[1]。由于原發腫瘤位置的原因,很少采用手術治療。新近更新的ESMO指南推薦免疫治療聯合化療用于復發或轉移性鼻咽癌的一線治療[2]。
【參考文獻】 |
[1]. https://gco.iarc.who.int/media/globocan/factsheets/populations/160-china-fact-sheet.pdf. |
[2]. Bossi, P; Chan, AT; Even, C; Machiels, JP, et al.ESMO-EURACAN Clinical Practice Guideline update for nasopharyngeal carcinoma: adjuvant therapy and first-line treatment of recurrent/metastatic disease. Ann Oncol, 2023; 34 (3): 247. |
關于食管癌
食管癌是消化道領域最常見的惡性腫瘤之一。根據GLOBOCAN 2022發布的數據顯示,食管癌是2022年全球第十一大常見惡性腫瘤和第七大癌癥死亡原因,新發病例數超過51.1萬,死亡病例數超過44.5萬[1]。食管鱗癌(ESCC)和腺癌是食管癌的兩種主要組織學亞型。ESMO指南推薦PD-1阻斷性抗體聯合化療用于PD-L1表達陽性的晚期或轉移性ESCC的一線治療[2]。
【參考文獻】 |
[1]. https://gco.iarc.who.int/media/globocan/factsheets/populations/160-china-fact-sheet.pdf. |
[2]. Obermannova R,Alsina M, Cervantes A,Leong T,Lordick F, Nilsson M,van Greeken NCT, Vogel A,Smyth EC; ESMO Guidelines Committee. ESMO Clinical Practice Guidline for diagnosis,treatment and follow-up.Ann Oncol.2022 Oct;33(10):992-1004. |
關于特瑞普利單抗注射液(拓益®,LOQTORZI®)
特瑞普利單抗注射液(拓益®)作為我國批準上市的首個國產以PD-1為靶點的單抗藥物,獲得國家科技重大專項項目支持,并榮膺國家專利領域最高獎項"中國專利金獎"。
特瑞普利單抗至今已在全球(包括中國、美國、東南亞及歐洲等地)開展了覆蓋超過15個適應癥的40多項由公司發起的臨床研究。正在進行或已完成的關鍵注冊臨床研究在多個瘤種范圍內評估特瑞普利單抗的安全性及療效,包括肺癌、鼻咽癌、食管癌、胃癌、膀胱癌、乳腺癌、肝癌、腎癌及皮膚癌等。
截至目前,特瑞普利單抗已在中國內地獲批10項適應癥:用于既往接受全身系統治療失敗的不可切除或轉移性黑色素瘤的治療(2018年12月);用于既往接受過二線及以上系統治療失敗的復發/轉移性鼻咽癌患者的治療(2021年2月);用于含鉑化療失敗包括新輔助或輔助化療12個月內進展的局部晚期或轉移性尿路上皮癌的治療(2021年4月);聯合順鉑和吉西他濱用于局部復發或轉移性鼻咽癌患者的一線治療(2021年11月);聯合紫杉醇和順鉑用于不可切除局部晚期/復發或遠處轉移性食管鱗癌患者的一線治療(2022年5月);聯合培美曲塞和鉑類用于表皮生長因子受體(EGFR)基因突變陰性和間變性淋巴瘤激酶(ALK)陰性、不可手術切除的局部晚期或轉移性非鱗狀非小細胞肺癌的一線治療(2022年9月);聯合化療圍手術期治療,繼之本品單藥作為輔助治療,用于可切除IIIA-IIIB期非小細胞肺癌的成人患者(2023年12月);聯合阿昔替尼用于中高危的不可切除或轉移性腎細胞癌患者的一線治療(2024年4月);聯合依托泊苷和鉑類用于廣泛期小細胞肺癌一線治療(2024年6月);聯合注射用紫杉醇(白蛋白結合型)用于經充分驗證的檢測評估PD-L1陽性(CPS≥1)的復發或轉移性三陰性乳腺癌的一線治療(2024年6月)。2020年12月,特瑞普利單抗首次通過國家醫保談判,目前已有6項獲批適應癥納入《國家醫保目錄(2023年)》,是目錄中唯一用于治療黑色素瘤的抗PD-1單抗藥物。2024年4月,香港衛生署藥物辦公室受理了特瑞普利單抗聯合順鉑/吉西他濱作為轉移性或復發性局部晚期鼻咽癌成人患者的一線治療,以及作為單藥治療既往含鉑治療過程中或治療后疾病進展的復發性、不可切除或轉移性鼻咽癌的成人患者的上市許可申請。
在國際化布局方面,2023年10月,特瑞普利單抗已作為首款鼻咽癌藥物在美國獲批上市。2024年9月,特瑞普利單抗用于晚期鼻咽癌和食管鱗癌的一線治療獲得歐盟委員會批準上市。此外,英國藥品和保健品管理局(MHRA)受理了特瑞普利單抗聯合順鉑和吉西他濱用于局部復發或轉移性鼻咽癌患者的一線治療以及聯合紫杉醇和順鉑用于不可切除局部晚期/復發或轉移性食管鱗癌患者的一線治療的上市許可申請,澳大利亞藥品管理局(TGA)和新加坡衛生科學局(HSA)分別受理了特瑞普利單抗聯合順鉑/吉西他濱作為轉移性或復發性局部晚期鼻咽癌成人患者的一線治療,以及作為單藥治療既往含鉑治療過程中或治療后疾病進展的復發性、不可切除或轉移性鼻咽癌的成人患者的上市許可申請。
關于君實生物
君實生物(688180.SH,1877.HK)成立于2012年12月,是一家以創新為驅動,致力于創新療法的發現、開發和商業化的生物制藥公司。依托全球一體化源頭創新研發能力,公司已構建起涵蓋超過50款創新藥物的多層次產品管線,覆蓋惡性腫瘤、自身免疫、慢性代謝類、神經系統、感染性疾病五大治療領域,已有4款產品在國內或海外上市,包括我國首個自主研發、在中美兩國獲批上市的PD-1抑制劑特瑞普利單抗(拓益®),臨床開發階段的藥物超過30款。疫情期間,君實生物還參與開發了埃特司韋單抗、民得維®等多款預防和治療新冠的創新藥物,積極承擔本土創新藥企的責任。
君實生物以"用世界一流、值得信賴的創新藥普惠患者"為使命,立足中國,布局全球。目前,公司在全球擁有約2500名員工,分布在美國舊金山和馬里蘭,中國上海、蘇州、北京、廣州等。
官方網站:www.junshipharma.com
官方微信:君實生物
填補空白,院士領銜20+專家加盟
肺癌是我國發病率和死亡率均排名首位的惡性腫瘤,其中SCLC約占所有肺癌病例的15%,是肺癌中侵襲性最強的亞型,具有疾病進展快速和早期轉移的特點。大多數患者在確診時已處于晚期疾病階段,這使得SCLC治療變得更加復雜和具有挑戰性。
當前,SCLC患者的真實世界研究數據相對匱乏,不僅限制了臨床醫生對治療方案的優化,也影響了患者個體化治療需求的精準性和有效性。因此,國內首部針對SCLC患者生存現狀的白皮書應運而生。
在專家顧問團的指導下,《白皮書》項目在覓健患者平臺順利啟動。包括山東省腫瘤醫院院長于金明院士在內的全國頂尖三甲醫院共22位肺癌領域專家教授組成的專家顧問團在肺癌篩查、早期診斷與治療、個性化醫療方案及腫瘤相關癥狀管理與支持治療等方向皆擁有深厚的積累,全程為《白皮書》項目提供專業指導。
在項目推進過程中,專家顧問團將共同設計患者診療路徑、治療情況、生存質量及隨訪患教等章節問卷并展開討論,并針對報告分析和成稿重點給予指導與建議,為《白皮書》的科學性和有效性提供堅實支撐。
山東省腫瘤醫院院長于金明院士在項目啟動會上表示:"SCLC惡性度高、生長快、轉移早使患者的治療選擇相對有限,而患者除了面對上述挑戰還需面對包括心理健康、生活質量、以及社會角色回歸等困擾。《白皮書》項目是中國首個針對小細胞肺癌患者生存現狀的調研,它不僅提供了一個全面了解患者群體的窗口,也為改善患者生存狀況提供了一個指引。當然,白皮書不僅僅是一份書面文件,相信在制作的過程中,我們可以依靠不同領域的專家的力量,充分落實患者的教育活動讓《白皮書》的結論及規范治療的觀念扎根全國造福廣大腫瘤患者。"
患者傾聽,大量樣本多維度分析
超大樣本數量和豐富的數據維度將全方位地反映我國SCLC患者的生存現狀:分析診療路徑識別治療瓶頸有助于診療流程優化,從而為患者提供更好的醫療服務;分析治療情況有助于提高患者后續臨床用藥的依從性;分析生存質量則可以為政府和相關機構制定公共健康政策提供科學依據。
君實生物總經理兼首席執行官鄒建軍博士表示:"作為全球和中國新發及死亡病例數最高的癌癥,肺癌的防控與治療是一項長期而艱巨的任務,需要政府、醫療機構、科研機構、企業以及社會各界的共同努力。君實生物一直以"用世界一流、值得信賴的生物源創藥普惠患者"為使命,持續深耕肺癌新藥研發,為生命續航注入不竭動力。期待《2024中國小細胞肺癌患者生存現狀白皮書》早日成稿發布,為我們揭示小細胞肺癌患者的真實生存狀況,提供科學權威的治療指導與建議,成為企業研發新藥的強勁動力,為患者生存質量帶來革命性飛躍,點亮生命的希望之光。"
—— 完 ——
1. 本材料旨在傳遞前沿信息,無意向您做任何產品的推廣,不作為臨床用藥指導。
2. 若您想了解具體疾病診療信息,請遵從醫療衛生專業人士的意見與指導。
關于君實生物
君實生物(688180.SH,1877.HK)成立于2012年12月,是一家以創新為驅動,致力于創新療法的發現、開發和商業化的生物制藥公司。依托全球一體化源頭創新研發能力,公司已構建起涵蓋超過50款創新藥物的多層次產品管線,覆蓋惡性腫瘤、自身免疫、慢性代謝類、神經系統、感染性疾病五大治療領域,已有4款產品在國內或海外上市,包括我國首個自主研發、在中美兩國獲批上市的PD-1抑制劑特瑞普利單抗(拓益®),臨床開發階段的藥物超過30款。疫情期間,君實生物還參與開發了埃特司韋單抗、民得維®等多款預防和治療新冠的創新藥物,積極承擔本土創新藥企的責任。
君實生物以"打造世界一流、值得信賴的生物源創藥普惠患者"為使命,立足中國,布局全球。目前,公司在全球擁有約3000名員工,分布在美國舊金山和馬里蘭,中國上海、蘇州、北京、廣州等。
官方網站:www.junshipharma.com
官方微信:君實生物
黑色素瘤是惡性程度最高的皮膚癌類型,2022年全球新發病例約33.2萬,死亡病例約5.9萬[1]。黑色素瘤在我國相對少見,但病死率高(2022年新發病例約0.9萬,而死亡病例達到0.5萬)[2],發病率也在逐年增加[3]。截至目前,國內抗PD-1單抗已獲批用于晚期黑色素瘤二線及以上治療,但晚期一線標準治療仍為傳統化療或靶向治療(僅適用于攜帶BRAF V600突變的患者)。因此,國內晚期黑色素瘤患者對于一線免疫治療的臨床需求迫切。
本次新適應癥的上市申請主要基于MELATORCH研究(NCT03430297)。MELATORCH研究(NCT03430297)是一項多中心、隨機、開放、陽性藥對照的Ⅲ期臨床研究,也是目前國內首個且唯一達成陽性結果的PD-(L)1抑制劑一線治療晚期黑色素瘤的關鍵注冊臨床研究,該研究旨在比較特瑞普利單抗對比達卡巴嗪在既往未接受系統抗腫瘤治療的不可切除或轉移性黑色素瘤患者中的有效性和安全性。該研究由北京大學腫瘤醫院郭軍教授擔任主要研究者,在全國11家臨床中心開展。
2023年9月,MELATORCH研究的主要研究終點無進展生存期(PFS,基于獨立影像評估)達到方案預設的優效邊界。研究結果表明,相較于達卡巴嗪,特瑞普利單抗一線治療不可切除或轉移性黑色素瘤可顯著延長患者的PFS。特瑞普利單抗安全性數據與既往研究相似,未發現新的安全性信號。關于詳細的研究數據,君實生物將在近期國際學術大會上公布。
作為MELATORCH研究的主要研究者,CSCO黑色素瘤專委會主任委員、北京大學腫瘤醫院郭軍教授表示:"過去5年間,特瑞普利單抗作為我國晚期黑色素瘤二線及以上挽救治療的標準療法,改變了中國晚期黑色素瘤治療的格局,為眾多中國患者帶來了突破性的生存獲益。但我們也知道,中國黑色素瘤患者相對白種人更加難治。因此,雖然國際上PD-1抑制劑早已獲批用于黑色素瘤一線治療,甚至更早期患者的輔助治療,但截止目前我國還尚未有免疫檢查點抑制劑在上述人群中獲批。此次特瑞普利單抗的新適應癥上市申請獲得受理,證明了其在更早線治療中的價值,意義重大。期待其能夠早日獲得正式批準,讓我國黑色素瘤患者有機會更早地從免疫治療中獲益。"
君實生物總經理兼首席執行官鄒建軍博士表示:"2018年,特瑞普利單抗作為首個國產抗PD-1單抗獲批上市用于晚期黑色素瘤的二線及以上治療,在中國醫藥生物發展史上留下輝煌的一筆。如今,我們行而不輟,特瑞普利單抗第‘十二項’上市申請獲得NMPA受理,有望成為我國首個黑色素瘤一線免疫療法。我們將與監管部門積極合作,以期盡早為患者提供更優的臨床治療選擇。"
【參考文獻】
- https://gco.iarc.who.int/media/globocan/factsheets/cancers/16-melanoma-of-skin-fact-sheet.pdf.
- https://gco.iarc.who.int/media/globocan/factsheets/populations/160-china-fact-sheet.pdf.
- 中華人民共和國國家衛生健康委員會黑色素瘤診療指南(2022年版)
—— 完 ——
1. 本材料旨在傳遞前沿信息,無意向您做任何產品的推廣,不作為臨床用藥指導。
2. 若您想了解具體疾病診療信息,請遵從醫療衛生專業人士的意見與指導。
關于特瑞普利單抗注射液(拓益®)
特瑞普利單抗注射液(拓益®)作為我國批準上市的首個國產以PD-1為靶點的單抗藥物,獲得國家科技重大專項項目支持,并榮膺國家專利領域最高獎項"中國專利金獎"。
特瑞普利單抗至今已在全球(包括中國、美國、東南亞及歐洲等地)開展了覆蓋超過15個適應癥的40多項由公司發起的臨床研究。正在進行或已完成的關鍵注冊臨床研究在多個瘤種范圍內評估特瑞普利單抗的安全性及療效,包括肺癌、鼻咽癌、食管癌、胃癌、膀胱癌、乳腺癌、肝癌、腎癌及皮膚癌等。
截至目前,特瑞普利單抗已在中國內地獲批10項適應癥:用于既往接受全身系統治療失敗的不可切除或轉移性黑色素瘤的治療(2018年12月);用于既往接受過二線及以上系統治療失敗的復發/轉移性鼻咽癌患者的治療(2021年2月);用于含鉑化療失敗包括新輔助或輔助化療12個月內進展的局部晚期或轉移性尿路上皮癌的治療(2021年4月);聯合順鉑和吉西他濱用于局部復發或轉移性鼻咽癌患者的一線治療(2021年11月);聯合紫杉醇和順鉑用于不可切除局部晚期/復發或遠處轉移性食管鱗癌患者的一線治療(2022年5月);聯合培美曲塞和鉑類用于表皮生長因子受體(EGFR)基因突變陰性和間變性淋巴瘤激酶(ALK)陰性、不可手術切除的局部晚期或轉移性非鱗狀非小細胞肺癌的一線治療(2022年9月);聯合化療圍手術期治療,繼之本品單藥作為輔助治療,用于可切除IIIA-IIIB期非小細胞肺癌的成人患者(2023年12月);聯合阿昔替尼用于中高危的不可切除或轉移性腎細胞癌患者的一線治療(2024年4月);聯合依托泊苷和鉑類用于廣泛期小細胞肺癌一線治療(2024年6月);聯合注射用紫杉醇(白蛋白結合型)用于經充分驗證的檢測評估PD-L1陽性(CPS≥1)的復發或轉移性三陰性乳腺癌的一線治療(2024年6月)。2020年12月,特瑞普利單抗首次通過國家醫保談判,目前已有6項獲批適應癥納入《國家醫保目錄(2023年)》,是目錄中唯一用于治療黑色素瘤的抗PD-1單抗藥物。2024年4月,香港衛生署藥物辦公室受理了特瑞普利單抗聯合順鉑/吉西他濱作為轉移性或復發性局部晚期鼻咽癌成人患者的一線治療,以及作為單藥治療既往含鉑治療過程中或治療后疾病進展的復發性、不可切除或轉移性鼻咽癌的成人患者的上市許可申請。
在國際化布局方面,特瑞普利單抗已作為首款鼻咽癌藥物在美國獲得批準,其在黏膜黑色素瘤、鼻咽癌、軟組織肉瘤、食管癌、小細胞肺癌領域獲得美國食品藥品監督管理局(FDA)授予2項突破性療法認定、1項快速通道認定、1項優先審評認定和5項孤兒藥資格認定。
2022年12月和2023年2月,歐洲藥品管理局(EMA)和英國藥品和保健品管理局(MHRA)分別受理了特瑞普利單抗聯合順鉑和吉西他濱用于局部復發或轉移性鼻咽癌患者的一線治療以及聯合紫杉醇和順鉑用于不可切除局部晚期/復發或轉移性食管鱗癌患者的一線治療的上市許可申請(MAA)。2023年11月和2024年1月,澳大利亞藥品管理局(TGA)和新加坡衛生科學局(HSA)分別受理了特瑞普利單抗聯合順鉑/吉西他濱作為轉移性或復發性局部晚期鼻咽癌成人患者的一線治療,以及作為單藥治療既往含鉑治療過程中或治療后疾病進展的復發性、不可切除或轉移性鼻咽癌的成人患者的上市許可申請,其中TGA授予1項孤兒藥資格認定,HSA授予1項優先審評認定。
關于君實生物
君實生物(688180.SH,1877.HK)成立于2012年12月,是一家以創新為驅動,致力于創新療法的發現、開發和商業化的生物制藥公司。依托全球一體化源頭創新研發能力,公司已構建起涵蓋超過50款創新藥物的多層次產品管線,覆蓋惡性腫瘤、自身免疫、慢性代謝類、神經系統、感染性疾病五大治療領域,已有4款產品在國內或海外上市,包括我國首個自主研發、在中美兩國獲批上市的PD-1抑制劑特瑞普利單抗(拓益®),臨床開發階段的藥物超過30款。疫情期間,君實生物還參與開發了埃特司韋單抗、民得維®等多款預防和治療新冠的創新藥物,積極承擔本土創新藥企的責任。
君實生物以"打造世界一流、值得信賴的生物源創藥普惠患者"為使命,立足中國,布局全球。目前,公司在全球擁有約3000名員工,分布在美國舊金山和馬里蘭,中國上海、蘇州、北京、廣州等。
官方網站:www.junshipharma.com
官方微信:君實生物
- 特瑞普利單抗聯合順鉑和吉西他濱用于復發、不能手術或放療的,或轉移性鼻咽癌(NPC)成人患者的一線治療;
- 特瑞普利單抗聯合順鉑和紫杉醇用于不可切除的晚期/復發或轉移性食管鱗癌(ESCC)成人患者的一線治療。
歐盟委員會(EC)將把CHMP的積極意見納入考慮,以便對特瑞普利單抗的上市申請做出最終審評決議。該決議將適用于歐盟全部27個成員國以及冰島和挪威。如若獲得批準,特瑞普利單抗將成為歐洲首個且唯一用于NPC治療的藥物,也是歐洲唯一用于不限PD-L1表達的晚期或轉移性ESCC一線治療藥物。
君實生物總經理兼首席執行官鄒建軍博士表示:"作為中國創新藥企的先行者,君實生物在持續關注本土患者臨床需求的同時,也致力為全球的患者提供能夠帶來生存獲益的創新療法。歐洲的NPC和ESCC患者通過現有治療臨床獲益有限,而特瑞普利單抗有望改善他們的境遇,此次獲得CHMP的積極意見,意味著我們向這一目標再進一步。我們將繼續與當地監管機構密切溝通,以期積極促成我們的創新療法能夠盡早惠及更多歐洲患者。"
本次CHMP對于NPC適應癥的積極意見主要基于JUPITER-02(一項隨機、雙盲、安慰劑對照、國際多中心III期臨床研究,NCT03581786)。該研究結果曾以口頭報告形式亮相2021年美國臨床腫瘤學會(ASCO)年會全體大會(#LBA2),隨后榮登《自然-醫學》(Nature Medicine,影響因子:58.7)雜志封面,并獲得《美國醫學會雜志》(Journal of the American Medical Association,JAMA,影響因子:63.1)全文發表。
基于上述研究,特瑞普利單抗分別于2021年和2023年獲得國家藥品監督管理局(NMPA)和美國食品藥品監督管理局(FDA)批準用于晚期鼻咽癌的治療,是全球首個獲批鼻咽癌治療的免疫檢查點抑制劑(ICI)藥物,也是美國首個且唯一用于鼻咽癌治療的藥物。此外,特瑞普利單抗用于治療鼻咽癌相關適應癥的上市申請正在同步接受英國藥品和保健品管理局(MHRA)、澳大利亞藥品管理局(TGA)、新加坡衛生科學局(HSA)以及中國香港衛生署藥物辦公室(DO)的審評。
此次CHMP對于ESCC適應癥的積極意見主要基于JUPITER-06(一項隨機、雙盲、安慰劑對照、多中心的Ⅲ期研究,NCT03829969)。該研究結果首次在歐洲腫瘤內科學會年會(ESMO 2021)上以口頭匯報形式報告,隨后在國際頂尖腫瘤學雜志《Cancer Cell》(影響因子:48.8)和《臨床腫瘤學雜志》(Journal of Clinical Oncology,影響因子:42.1)發表。2022年5月,特瑞普利單抗用于治療ESCC的新適應癥上市申請在中國獲批。目前,特瑞普利單抗用于一線治療食管癌的MAA正在接受MHRA的審評。
關于鼻咽癌
鼻咽癌是一種發生于鼻咽部上皮的惡性腫瘤,是全球范圍內常見的頭頸部惡性腫瘤之一。根據GLOBOCAN 2022發布的數據顯示,2022年鼻咽癌在全球范圍內確診的新發病例數超過12萬1。由于原發腫瘤位置的原因,很少采用手術治療。新近更新的ESMO指南推薦免疫治療聯合化療用于復發或轉移性鼻咽癌的一線治療2。
【參考文獻】
1. https://gco.iarc.who.int/media/globocan/factsheets/populations/160-china-fact-sheet.pdf.
2. Bossi, P; Chan, AT; Even, C; Machiels, JP, et al. ESMO-EURACAN Clinical Practice Guideline update for nasopharyngeal carcinoma: adjuvant therapy and first-line treatment of recurrent/metastatic disease. Ann Oncol, 2023; 34 (3): 247.
關于食管癌
食管癌是消化道領域最常見的惡性腫瘤之一。根據GLOBOCAN 2022發布的數據顯示,食管癌是2022年全球第十一大常見惡性腫瘤和第七大癌癥死亡原因,新發病例數超過51.1萬,死亡病例數超過44.5萬1。食管鱗癌(ESCC)和腺癌是食管癌的兩種主要組織學亞型。ESMO指南推薦PD-1阻斷性抗體聯合化療用于PD-L1表達陽性的晚期或轉移性ESCC的一線治療2。
【參考文獻】
1. https://gco.iarc.who.int/media/globocan/factsheets/populations/160-china-fact-sheet.pdf.
2. Obermannova R,Alsina M, Cervantes A,Leong T,Lordick F, Nilsson M,van Greeken NCT, Vogel A,Smyth EC; ESMO Guidelines Committee. ESMO Clinical Practice Guidline for diagnosis, treatment and follow-up. Ann Oncol.2022 Oct;33(10):992-1004.
關于特瑞普利單抗注射液(拓益®)
特瑞普利單抗注射液(拓益®)作為我國批準上市的首個國產以PD-1為靶點的單抗藥物,獲得國家科技重大專項項目支持,并榮膺國家專利領域最高獎項"中國專利金獎"。
特瑞普利單抗至今已在全球(包括中國、美國、東南亞及歐洲等地)開展了覆蓋超過15個適應癥的40多項由公司發起的臨床研究。正在進行或已完成的關鍵注冊臨床研究在多個瘤種范圍內評估特瑞普利單抗的安全性及療效,包括肺癌、鼻咽癌、食管癌、胃癌、膀胱癌、乳腺癌、肝癌、腎癌及皮膚癌等。
截至目前,特瑞普利單抗已在中國內地獲批10項適應癥:用于既往接受全身系統治療失敗的不可切除或轉移性黑色素瘤的治療(2018年12月);用于既往接受過二線及以上系統治療失敗的復發/轉移性鼻咽癌患者的治療(2021年2月);用于含鉑化療失敗包括新輔助或輔助化療12個月內進展的局部晚期或轉移性尿路上皮癌的治療(2021年4月);聯合順鉑和吉西他濱用于局部復發或轉移性鼻咽癌患者的一線治療(2021年11月);聯合紫杉醇和順鉑用于不可切除局部晚期/復發或遠處轉移性食管鱗癌患者的一線治療(2022年5月);聯合培美曲塞和鉑類用于表皮生長因子受體(EGFR)基因突變陰性和間變性淋巴瘤激酶(ALK)陰性、不可手術切除的局部晚期或轉移性非鱗狀非小細胞肺癌的一線治療(2022年9月);聯合化療圍手術期治療,繼之本品單藥作為輔助治療,用于可切除IIIA-IIIB期非小細胞肺癌的成人患者(2023年12月);聯合阿昔替尼用于中高危的不可切除或轉移性腎細胞癌患者的一線治療(2024年4月);聯合依托泊苷和鉑類用于廣泛期小細胞肺癌一線治療(2024年6月);聯合注射用紫杉醇(白蛋白結合型)用于經充分驗證的檢測評估PD-L1陽性(CPS≥1)的復發或轉移性三陰性乳腺癌的一線治療(2024年6月)。2020年12月,特瑞普利單抗首次通過國家醫保談判,目前已有6項獲批適應癥納入《國家醫保目錄(2023年)》,是目錄中唯一用于治療黑色素瘤的抗PD-1單抗藥物。2024年4月,香港衛生署藥物辦公室受理了特瑞普利單抗聯合順鉑/吉西他濱作為轉移性或復發性局部晚期鼻咽癌成人患者的一線治療,以及作為單藥治療既往含鉑治療過程中或治療后疾病進展的復發性、不可切除或轉移性鼻咽癌的成人患者的上市許可申請。
在國際化布局方面,特瑞普利單抗已作為首款鼻咽癌藥物在美國獲得批準,其在黏膜黑色素瘤、鼻咽癌、軟組織肉瘤、食管癌、小細胞肺癌領域獲得美國食品藥品監督管理局(FDA)授予2項突破性療法認定、1項快速通道認定、1項優先審評認定和5項孤兒藥資格認定。
2022年12月和2023年2月,歐洲藥品管理局(EMA)和英國藥品和保健品管理局(MHRA)分別受理了特瑞普利單抗聯合順鉑和吉西他濱用于局部復發或轉移性鼻咽癌患者的一線治療以及聯合紫杉醇和順鉑用于不可切除局部晚期/復發或轉移性食管鱗癌患者的一線治療的上市許可申請(MAA)。2023年11月和2024年1月,澳大利亞藥品管理局(TGA)和新加坡衛生科學局(HSA)分別受理了特瑞普利單抗聯合順鉑/吉西他濱作為轉移性或復發性局部晚期鼻咽癌成人患者的一線治療,以及作為單藥治療既往含鉑治療過程中或治療后疾病進展的復發性、不可切除或轉移性鼻咽癌的成人患者的上市許可申請,其中TGA授予1項孤兒藥資格認定,HSA授予1項優先審評認定。
關于君實生物
君實生物(688180.SH,1877.HK)成立于2012年12月,是一家以創新為驅動,致力于創新療法的發現、開發和商業化的生物制藥公司。依托全球一體化源頭創新研發能力,公司已構建起涵蓋超過50款創新藥物的多層次產品管線,覆蓋惡性腫瘤、自身免疫、慢性代謝類、神經系統、感染性疾病五大治療領域,已有4款產品在國內或海外上市,包括我國首個自主研發、在中美兩國獲批上市的PD-1抑制劑特瑞普利單抗(拓益®),臨床開發階段的藥物超過30款。疫情期間,君實生物還參與開發了埃特司韋單抗、民得維®等多款預防和治療新冠的創新藥物,積極承擔本土創新藥企的責任。
君實生物以"打造世界一流、值得信賴的生物源創藥普惠患者"為使命,立足中國,布局全球。目前,公司在全球擁有約3000名員工,分布在美國舊金山和馬里蘭,中國上海、蘇州、北京、廣州等。
官方網站:www.junshipharma.com
官方微信:君實生物
肝癌是全世界范圍內常見的消化系統惡性腫瘤,病理類型以HCC為主(約占90%)[1]。根據GLOBOCAN 2022報告,2022年全球肝癌的年新發病例數和死亡例數分別為86.6萬和75.9萬[2]。我國是肝癌大國,2022年肝癌新發病例數達到36.8萬(占全球病例的42.4%),居國內惡性腫瘤第4位,死亡31.7萬(占全球病例的41.7%),居國內惡性腫瘤第2位[3]。由于起病隱匿,約70%-80%的中國肝癌患者首次診斷時已是中晚期[4],中位OS僅約10個月,5年生存率約12%[5]。近些年來,隨著以免疫治療藥物為基礎的聯合方案的不斷涌現,晚期HCC的治療格局已經發生了轉變,轉化降期后獲得根治逐漸變成可能。
本次新適應癥的上市申請主要基于HEPATORCH研究(NCT04723004)。該研究是一項多中心、隨機、開放、陽性藥對照的III期臨床研究,旨在評估與標準治療索拉非尼相比,特瑞普利單抗聯合貝伐珠單抗一線治療不可切除或轉移性HCC的有效性和安全性。該研究由中國科學院院士、復旦大學附屬中山醫院樊嘉教授擔任主要研究者,在全國57家臨床中心開展。
2024年6月,HEPATORCH研究的主要研究終點無進展生存期(PFS,基于獨立影像評估)和總生存期(OS)均達到方案預設的優效邊界。研究結果顯示,特瑞普利單抗聯合貝伐珠單抗一線治療晚期HCC患者,相較于索拉非尼,可顯著延長患者的PFS和OS,同時改善客觀緩解率和至疾病進展時間等次要終點。特瑞普利單抗安全性數據與已知風險相符,未發現新的安全性信號。關于詳細的研究數據,君實生物將在近期國際學術大會上公布。
HEPATORCH研究主要研究者、中國科學院院士、復旦大學附屬中山醫院樊嘉教授表示:"由于HCC起病隱匿,大部分國內患者初診時已失去根治性手術的機會。HEPATORCH研究結果顯示出特瑞普利單抗聯合貝伐珠單抗一線治療晚期HCC的顯著生存獲益,也再次證明了免疫檢查點抑制劑聯合抗血管生成靶向藥物對于晚期HCC的療效。期待特瑞普利單抗聯合治療方案能夠盡早獲得批準,為我國晚期HCC患者帶來全新的治療選擇!"
君實生物總經理兼首席執行官鄒建軍博士表示:"非常高興能夠見證特瑞普利單抗第十一項適應癥的成功申報。自2018年獲批成為首個上市的國產抗PD-1單抗以來,特瑞普利單抗瞄準中國乃至全球腫瘤患者的未盡之需,目前已連續在7個瘤種領域獲批10項適應癥,其中包含多個獨家適應癥。此次申報是特瑞普利單抗在肝癌領域申報的首個適應癥,再次顯示出了其強大的‘廣譜'抗癌能力。后續,我們將與監管部門積極溝通,推動這項適應癥的盡快落地,讓更多晚期肝癌患者受益于我們的創新療法。"
【參考文獻】
- Hepatocellular carcinoma. Nat Rev Dis Primers. 2021;7(1):7.
- Bray F, Laversanne M, Sung H, et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2024;74(3):229-263.
- Zheng RS, Chen R, Han BF, et al. Zhonghua Zhong Liu Za Zhi. 2024;46(3):221-231.
- 《靶免聯合局部治療 中晚期肝細胞癌中國專家共識》, 肝癌電子雜志, 2023, 10(3): 1-11
- Zeng H, Chen W, Zheng R, et al. Changing cancer survival in China during 2003-15: a pooled analysis of 17 population-based cancer registries. Lancet Glob Health. 2018;6(5):e555-e567.
關于特瑞普利單抗注射液(拓益®)
特瑞普利單抗注射液(拓益®)作為我國批準上市的首個國產以PD-1為靶點的單抗藥物,獲得國家科技重大專項項目支持,并榮膺國家專利領域最高獎項"中國專利金獎"。
特瑞普利單抗至今已在全球(包括中國、美國、東南亞及歐洲等地)開展了覆蓋超過15個適應癥的40多項由公司發起的臨床研究。正在進行或已完成的關鍵注冊臨床研究在多個瘤種范圍內評估特瑞普利單抗的安全性及療效,包括肺癌、鼻咽癌、食管癌、胃癌、膀胱癌、乳腺癌、肝癌、腎癌及皮膚癌等。
截至目前,特瑞普利單抗已在中國內地獲批10項適應癥:用于既往接受全身系統治療失敗的不可切除或轉移性黑色素瘤的治療(2018年12月);用于既往接受過二線及以上系統治療失敗的復發/轉移性鼻咽癌患者的治療(2021年2月);用于含鉑化療失敗包括新輔助或輔助化療12個月內進展的局部晚期或轉移性尿路上皮癌的治療(2021年4月);聯合順鉑和吉西他濱用于局部復發或轉移性鼻咽癌患者的一線治療(2021年11月);聯合紫杉醇和順鉑用于不可切除局部晚期/復發或遠處轉移性食管鱗癌患者的一線治療(2022年5月);聯合培美曲塞和鉑類用于表皮生長因子受體(EGFR)基因突變陰性和間變性淋巴瘤激酶(ALK)陰性、不可手術切除的局部晚期或轉移性非鱗狀非小細胞肺癌的一線治療(2022年9月);聯合化療圍手術期治療,繼之本品單藥作為輔助治療,用于可切除IIIA-IIIB期非小細胞肺癌的成人患者(2023年12月);聯合阿昔替尼用于中高危的不可切除或轉移性腎細胞癌患者的一線治療(2024年4月);聯合依托泊苷和鉑類用于廣泛期小細胞肺癌一線治療(2024年6月);聯合注射用紫杉醇(白蛋白結合型)用于經充分驗證的檢測評估PD-L1陽性(CPS≥1)的復發或轉移性三陰性乳腺癌的一線治療(2024年6月)。2020年12月,特瑞普利單抗首次通過國家醫保談判,目前已有6項獲批適應癥納入《國家醫保目錄(2023年)》,是目錄中唯一用于治療黑色素瘤的抗PD-1單抗藥物。2024年4月,香港衛生署藥物辦公室受理了特瑞普利單抗聯合順鉑/吉西他濱作為轉移性或復發性局部晚期鼻咽癌成人患者的一線治療,以及作為單藥治療既往含鉑治療過程中或治療后疾病進展的復發性、不可切除或轉移性鼻咽癌的成人患者的上市許可申請。
在國際化布局方面,特瑞普利單抗已作為首款鼻咽癌藥物在美國獲得批準,其在黏膜黑色素瘤、鼻咽癌、軟組織肉瘤、食管癌、小細胞肺癌領域獲得美國食品藥品監督管理局(FDA)授予2項突破性療法認定、1項快速通道認定、1項優先審評認定和5項孤兒藥資格認定。
2022年12月和2023年2月,歐洲藥品管理局(EMA)和英國藥品和保健品管理局(MHRA)分別受理了特瑞普利單抗聯合順鉑和吉西他濱用于局部復發或轉移性鼻咽癌患者的一線治療以及聯合紫杉醇和順鉑用于不可切除局部晚期/復發或轉移性食管鱗癌患者的一線治療的上市許可申請(MAA)。2023年11月和2024年1月,澳大利亞藥品管理局(TGA)和新加坡衛生科學局(HSA)分別受理了特瑞普利單抗聯合順鉑/吉西他濱作為轉移性或復發性局部晚期鼻咽癌成人患者的一線治療,以及作為單藥治療既往含鉑治療過程中或治療后疾病進展的復發性、不可切除或轉移性鼻咽癌的成人患者的上市許可申請,其中TGA授予1項孤兒藥資格認定,HSA授予1項優先審評認定。
關于君實生物
君實生物(688180.SH,1877.HK)成立于2012年12月,是一家以創新為驅動,致力于創新療法的發現、開發和商業化的生物制藥公司。依托全球一體化源頭創新研發能力,公司已構建起涵蓋超過50款創新藥物的多層次產品管線,覆蓋惡性腫瘤、自身免疫、慢性代謝類、神經系統、感染性疾病五大治療領域,已有4款產品在國內或海外上市,包括我國首個自主研發、在中美兩國獲批上市的PD-1抑制劑特瑞普利單抗(拓益®),臨床開發階段的藥物超過30款。疫情期間,君實生物還參與開發了埃特司韋單抗、民得維®等多款預防和治療新冠的創新藥物,積極承擔本土創新藥企的責任。
君實生物以"打造世界一流、值得信賴的生物源創藥普惠患者"為使命,立足中國,布局全球。目前,公司在全球擁有約3000名員工,分布在美國舊金山和馬里蘭,中國上海、蘇州、北京、廣州等。
官方網站:www.junshipharma.com
官方微信:君實生物
]]>據統計,全球乳腺癌的年新發病例數達231萬,死亡病例數達67萬[1],是全球女性發病率最高的癌癥。在我國,乳腺癌年新發病例數達35.7萬,死亡病例數達7.5萬,分別占全球病例數的15.5%和11.2%[2]。其中,三陰性乳腺癌(TNBC)約占所有乳腺癌的10-15%,具有侵襲性強、復發率高和預后較差的特點[3]。晚期TNBC對靶向治療和內分泌治療不敏感,缺乏特異性的治療方法。中國目前的TNBC治療仍以化療為主,但無論單藥或是聯合化療均療效欠佳,中位生存期約9~12個月,5年生存率不足30%[4,5]。
本次新適應癥的獲批主要基于TORCHLIGHT研究(NCT04085276)的數據結果。TORCHLIGHT研究是一項隨機、雙盲、安慰劑對照、多中心的III期臨床研究,由中國臨床腫瘤學會(CSCO)副理事長兼秘書長、解放軍總醫院腫瘤醫學部江澤飛教授擔任主要研究者,在全國56家中心聯合開展。
2023年2月,獨立數據監查委員會(IDMC)在期中分析時判定TORCHLIGHT研究的主要終點達到方案預設的優效界值,成為國內首個在晚期TNBC免疫治療領域取得陽性結果的III期注冊研究。
2024年1月,國際頂尖醫學期刊《自然-醫學》(Nature Medicine,影響因子:58.7)發表了TORCHLIGHT研究期中分析數據。結果顯示,與注射用紫杉醇(白蛋白結合型)相比,特瑞普利單抗聯合注射用紫杉醇(白蛋白結合型)用于首診IV期或復發轉移性TNBC患者可顯著延長PD-L1陽性人群的無進展生存期(PFS),總生存期(OS)也達到了獲益趨勢,實現了中國晚期TNBC免疫治療零的突破。其中,特瑞普利單抗組的中位PFS達8.4個月,疾病進展或死亡風險降低35%(P=0.0102);特瑞普利單抗組的中位OS延長了13.3個月(32.8個月 vs 19.5個月),死亡風險降低了38%(P=0.0148),特瑞普利單抗安全性數據與已知風險相符,未發現新的安全性信號。
解放軍總醫院腫瘤醫學部江澤飛教授表示:"免疫治療已成為三陰性乳腺癌最重要的治療手段,TORCHLIGHT研究在傳統化療基礎上加入免疫檢查點抑制劑,不僅顯著延長晚期TNBC患者的mPFS,且顯示出顯著的生存獲益趨勢,提高TNBC患者總生存超30月。特瑞普利單抗作為國內首個在TNBC領域獲批的免疫療法,將成為TNBC一線治療新標準。"
君實生物總經理兼首席執行官鄒建軍博士表示:"長期以來,晚期三陰性乳腺癌領域一直缺乏有效的治療手段,此次新適應癥的獲批是我們又一次成功嘗試,為中國晚期三陰性乳腺癌患者帶來了新的希望。目前,除了特瑞普利單抗,我們在乳腺癌領域還有更多創新藥在積極布局和開展臨床研究,希望未來能繼續為乳腺癌患者提供更多治療選擇。"
【參考文獻】 |
1. Bray F, Laversanne M, Sung H, Ferlay J, Siegel RL, Soerjomataram I, Jemal A. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2024 May-Jun;74(3):229-263. doi: 10.3322/caac.21834. Epub 2024 Apr 4. PMID: 38572751. |
2. Https://gco.iarc.fr/today/data/factsheets/populations/160-china-fact-sheets.pdf. |
3. Dass, S.A., et al. Medicina. 2021; 57, 62. |
4. De Laurentiis M, et al. Cancer Treat Rev. 2010;36 Suppl 3:S80-6. |
5. Zeichner SB, et al. Breast Cancer (Auckl). 2016;10:25-36. |
6. Zefei J, et al. Toripalimab plus nab-paclitaxel in metastatic or recurrent triple-negative breast cancer: a randomized phase 3 trial. Nat Med 30, 249–256 (2024). |
—— 完 ——
關于特瑞普利單抗注射液(拓益®)
特瑞普利單抗注射液(拓益®)作為我國批準上市的首個國產以PD-1為靶點的單抗藥物,獲得國家科技重大專項項目支持,并榮膺國家專利領域最高獎項"中國專利金獎"。
特瑞普利單抗至今已在全球(包括中國、美國、東南亞及歐洲等地)開展了覆蓋超過15個適應癥的40多項由公司發起的臨床研究。正在進行或已完成的關鍵注冊臨床研究在多個瘤種范圍內評估特瑞普利單抗的安全性及療效,包括肺癌、鼻咽癌、食管癌、胃癌、膀胱癌、乳腺癌、肝癌、腎癌及皮膚癌等。
截至目前,特瑞普利單抗已在中國內地獲批10項適應癥:用于既往接受全身系統治療失敗的不可切除或轉移性黑色素瘤的治療(2018年12月);用于既往接受過二線及以上系統治療失敗的復發/轉移性鼻咽癌患者的治療(2021年2月);用于含鉑化療失敗包括新輔助或輔助化療12個月內進展的局部晚期或轉移性尿路上皮癌的治療(2021年4月);聯合順鉑和吉西他濱用于局部復發或轉移性鼻咽癌患者的一線治療(2021年11月);聯合紫杉醇和順鉑用于不可切除局部晚期/復發或遠處轉移性食管鱗癌患者的一線治療(2022年5月);聯合培美曲塞和鉑類用于表皮生長因子受體(EGFR)基因突變陰性和間變性淋巴瘤激酶(ALK)陰性、不可手術切除的局部晚期或轉移性非鱗狀非小細胞肺癌的一線治療(2022年9月);聯合化療圍手術期治療,繼之本品單藥作為輔助治療,用于可切除IIIA-IIIB期非小細胞肺癌的成人患者(2023年12月);聯合阿昔替尼用于中高危的不可切除或轉移性腎細胞癌患者的一線治療(2024年4月);聯合依托泊苷和鉑類用于廣泛期小細胞肺癌一線治療(2024年6月);聯合注射用紫杉醇(白蛋白結合型)用于經充分驗證的檢測評估PD-L1陽性(CPS≥1)的復發或轉移性三陰性乳腺癌的一線治療(2024年6月)。2020年12月,特瑞普利單抗首次通過國家醫保談判,目前已有6項獲批適應癥納入《國家醫保目錄(2023年)》,是目錄中唯一用于治療黑色素瘤的抗PD-1單抗藥物。2024年4月,香港衛生署藥物辦公室受理了特瑞普利單抗聯合順鉑/吉西他濱作為轉移性或復發性局部晚期鼻咽癌成人患者的一線治療,以及作為單藥治療既往含鉑治療過程中或治療后疾病進展的復發性、不可切除或轉移性鼻咽癌的成人患者的上市許可申請。
在國際化布局方面,特瑞普利單抗已作為首款鼻咽癌藥物在美國獲得批準,其在黏膜黑色素瘤、鼻咽癌、軟組織肉瘤、食管癌、小細胞肺癌領域獲得美國食品藥品監督管理局(FDA)授予2項突破性療法認定、1項快速通道認定、1項優先審評認定和5項孤兒藥資格認定。
2022年12月和2023年2月,歐洲藥品管理局(EMA)和英國藥品和保健品管理局(MHRA)分別受理了特瑞普利單抗聯合順鉑和吉西他濱用于局部復發或轉移性鼻咽癌患者的一線治療以及聯合紫杉醇和順鉑用于不可切除局部晚期/復發或轉移性食管鱗癌患者的一線治療的上市許可申請(MAA)。2023年11月和2024年1月,澳大利亞藥品管理局(TGA)和新加坡衛生科學局(HSA)分別受理了特瑞普利單抗聯合順鉑/吉西他濱作為轉移性或復發性局部晚期鼻咽癌成人患者的一線治療,以及作為單藥治療既往含鉑治療過程中或治療后疾病進展的復發性、不可切除或轉移性鼻咽癌的成人患者的上市許可申請,其中TGA授予1項孤兒藥資格認定,HSA授予1項優先審評認定。
關于君實生物
君實生物(688180.SH,1877.HK)成立于2012年12月,是一家以創新為驅動,致力于創新療法的發現、開發和商業化的生物制藥公司。依托全球一體化源頭創新研發能力,公司已構建起涵蓋超過50款創新藥物的多層次產品管線,覆蓋惡性腫瘤、自身免疫、慢性代謝類、神經系統、感染性疾病五大治療領域,已有4款產品在國內或海外上市,包括我國首個自主研發、在中美兩國獲批上市的PD-1抑制劑特瑞普利單抗(拓益®),臨床開發階段的藥物超過30款。疫情期間,君實生物還參與開發了埃特司韋單抗、民得維®等多款預防和治療新冠的創新藥物,積極承擔本土創新藥企的責任。
君實生物以"打造世界一流、值得信賴的生物源創藥普惠患者"為使命,立足中國,布局全球。目前,公司在全球擁有約3000名員工,分布在美國舊金山和馬里蘭,中國上海、蘇州、北京、廣州等。
官方網站:www.junshipharma.com
官方微信:君實生物
肺癌是目前我國發病率和死亡率均排名首位的惡性腫瘤[1]。小細胞肺癌(SCLC)是肺癌中侵襲性最強的亞型[2],約占所有肺癌病例的15%-20%[3],具有進展迅速、早期轉移、預后差等特點[4]。SCLC分為局限期(LS-SCLC)和廣泛期(ES-SCLC)。對于LS-SCLC患者,通過標準化療和放療,目前已可達到約90%的客觀緩解率和約25%的5年生存率[5,6]。然而,大部分患者在就診時,已被診斷為ES-SCLC,中位生存期不足1年[7],2年生存率不到10%[8],仍是臨床未解決的一大難題。
此次新適應癥的獲批主要基于EXTENTORCH研究(NCT04012606)的數據結果。EXTENTORCH研究是一項隨機、雙盲、安慰劑對照、多中心III期臨床研究,旨在比較特瑞普利單抗或安慰劑聯合依托泊苷及鉑類在一線治療廣泛期小細胞肺癌中的有效性和安全性,由吉林省腫瘤醫院程穎教授擔任主要研究者,在全國51家臨床中心聯合開展。
2023年5月,EXTENTORCH研究的主要終點達到方案預設的優效邊界,特瑞普利單抗由此成為全球首個在ES-SCLC一線治療III期研究中達成總生存期(OS)和無進展生存期(PFS)雙重主要終點的PD-1抑制劑。
2023年10月舉行的歐洲腫瘤內科學會(ESMO)大會上,EXTENTORCH以口頭報告形式首次公布數據。研究結果顯示,相較單純化療,特瑞普利單抗聯合化療可顯著延長患者的PFS和OS,且安全性良好,有望成為ES-SCLC免疫治療的優選方案。其中,特瑞普利單抗組的中位PFS達5.8個月,疾病進展或死亡風險降低33.3%(P=0.0002),1年PFS率較化療組提升近4倍(18.1% vs. 4.9%);特瑞普利單抗組的中位OS達14.6個月,死亡風險降低20.2%(P=0.0327),1年OS率高達63.1%。
吉林省腫瘤醫院程穎教授表示:"SCLC侵襲性強、早期轉移和較差的預后。長期以來,ES-SCLC都以含鉑化療作為標準治療方案,盡管患者用藥初期較敏感,但易出現耐藥,而免疫治療的加入打開了新的局面。EXTENTORCH研究的PFS和OS雙重主要終點設計遵循了更高的統計學標準,并最終取得了雙終點陽性結果,這意味著相較單純化療,特瑞普利單抗聯合化療可顯著改善患者的PFS和OS。特瑞普利單抗獲批ES-SCLC一線治療適應癥,為中國SCLC增添了新的、有效的、安全性的、經濟的治療選擇!"
君實生物總經理兼首席執行官鄒建軍博士表示:"作為全球新發和死亡病例數最高的癌癥,肺癌一直是腫瘤治療的'頭號敵人'。君實生物在肺癌新藥研發上持續投入,截至目前特瑞普利單抗已成功獲批3項肺癌適應癥,包括非鱗非小細胞肺癌(NSCLC)和SCLC,并覆蓋了早中期(圍手術期)至晚期人群,還有更多產品和適應癥仍處于攻關階段。我們也期待能夠不斷為肺癌患者帶來更多更好的治療選擇。"
【參考文獻】 |
1. https://gco.iarc.who.int/media/globocan/factsheets/populations/160-china-fact-sheet.pdf. |
2. 張爽等.小細胞肺癌個體化治療進展[J].中國腫瘤臨床,2017,44(12):571-576. |
3. Gaspar LE, et al. Small-cell lung cancer: prognostic factors and changing treatment over 15 years. Clin Lung Cancer. 2012 Mar;13(2):115-22. |
4. Pesch B, et al. Cigarette smoking and lung cancer--relative risk estimates for the major histological types from a pooled analysis of case-control studies. Int J Cancer. 2012 Sep 1;131(5):1210-9. |
5. Kalemkerian GP. Small Cell Lung Cancer. Semin Respir Crit Care Med. 2016 Oct;37(5):783-796. |
6. Stinchcombe TE, et al. Limited-stage small cell lung cancer: current chemoradiotherapy treatment paradigms. Oncologist. 2010;15(2):187-95. |
7. Lally BE, et al. Small cell lung cancer: have we made any progress over the last 25 years? Oncologist. 2007 Sep;12(9):1096-104. |
8. Socinski MA, et al. Phase III study of pemetrexed plus carboplatin compared with etoposide plus carboplatin in chemotherapy-naive patients with extensive-stage small-cell lung cancer. J Clin Oncol. 2009 Oct 1;27(28):4787-92. |
關于特瑞普利單抗注射液(拓益®)
特瑞普利單抗注射液(拓益®)作為我國批準上市的首個國產以PD-1為靶點的單抗藥物,獲得國家科技重大專項項目支持,并榮膺國家專利領域最高獎項"中國專利金獎"。
特瑞普利單抗至今已在全球(包括中國、美國、東南亞及歐洲等地)開展了覆蓋超過15個適應癥的40多項由公司發起的臨床研究。正在進行或已完成的關鍵注冊臨床研究在多個瘤種范圍內評估特瑞普利單抗的安全性及療效,包括肺癌、鼻咽癌、食管癌、胃癌、膀胱癌、乳腺癌、肝癌、腎癌及皮膚癌等。
截至目前,特瑞普利單抗已在中國內地獲批9項適應癥:用于既往接受全身系統治療失敗的不可切除或轉移性黑色素瘤的治療(2018年12月);用于既往接受過二線及以上系統治療失敗的復發/轉移性鼻咽癌患者的治療(2021年2月);用于含鉑化療失敗包括新輔助或輔助化療12個月內進展的局部晚期或轉移性尿路上皮癌的治療(2021年4月);聯合順鉑和吉西他濱用于局部復發或轉移性鼻咽癌患者的一線治療(2021年11月);聯合紫杉醇和順鉑用于不可切除局部晚期/復發或遠處轉移性食管鱗癌患者的一線治療(2022年5月);聯合培美曲塞和鉑類用于表皮生長因子受體(EGFR)基因突變陰性和間變性淋巴瘤激酶(ALK)陰性、不可手術切除的局部晚期或轉移性非鱗狀非小細胞肺癌的一線治療(2022年9月);聯合化療圍手術期治療,繼之本品單藥作為輔助治療,用于可切除IIIA-IIIB期非小細胞肺癌的成人患者(2023年12月);聯合阿昔替尼用于中高危的不可切除或轉移性腎細胞癌患者的一線治療(2024年4月);聯合依托泊苷和鉑類用于廣泛期小細胞肺癌一線治療(2024年6月)。2020年12月,特瑞普利單抗首次通過國家醫保談判,目前已有6項獲批適應癥納入《國家醫保目錄(2023年)》,是目錄中唯一用于治療黑色素瘤的抗PD-1單抗藥物。2024年4月,香港衛生署藥物辦公室受理了特瑞普利單抗聯合順鉑/吉西他濱作為轉移性或復發性局部晚期鼻咽癌成人患者的一線治療,以及作為單藥治療既往含鉑治療過程中或治療后疾病進展的復發性、不可切除或轉移性鼻咽癌的成人患者的上市許可申請。
在國際化布局方面,特瑞普利單抗已作為首款鼻咽癌藥物在美國獲得批準,其在黏膜黑色素瘤、鼻咽癌、軟組織肉瘤、食管癌、小細胞肺癌領域獲得美國食品藥品監督管理局(FDA)授予2項突破性療法認定、1項快速通道認定、1項優先審評認定和5項孤兒藥資格認定。
2022年12月和2023年2月,歐洲藥品管理局(EMA)和英國藥品和保健品管理局(MHRA)分別受理了特瑞普利單抗聯合順鉑和吉西他濱用于局部復發或轉移性鼻咽癌患者的一線治療以及聯合紫杉醇和順鉑用于不可切除局部晚期/復發或轉移性食管鱗癌患者的一線治療的上市許可申請(MAA)。2023年11月和2024年1月,澳大利亞藥品管理局(TGA)和新加坡衛生科學局(HSA)分別受理了特瑞普利單抗聯合順鉑/吉西他濱作為轉移性或復發性局部晚期鼻咽癌成人患者的一線治療,以及作為單藥治療既往含鉑治療過程中或治療后疾病進展的復發性、不可切除或轉移性鼻咽癌的成人患者的上市許可申請,其中TGA授予1項孤兒藥資格認定,HSA授予1項優先審評認定。
關于君實生物
君實生物(688180.SH,1877.HK)成立于2012年12月,是一家以創新為驅動,致力于創新療法的發現、開發和商業化的生物制藥公司。依托全球一體化源頭創新研發能力,公司已構建起涵蓋超過50款創新藥物的多層次產品管線,覆蓋惡性腫瘤、自身免疫、慢性代謝類、神經系統、感染性疾病五大治療領域,已有4款產品在國內或海外上市,包括我國首個自主研發、在中美兩國獲批上市的PD-1抑制劑特瑞普利單抗(拓益®),臨床開發階段的藥物超過30款。疫情期間,君實生物還參與開發了埃特司韋單抗、民得維®等多款預防和治療新冠的創新藥物,積極承擔本土創新藥企的責任。
君實生物以"打造世界一流、值得信賴的生物源創藥普惠患者"為使命,立足中國,布局全球。目前,公司在全球擁有約3000名員工,分布在美國舊金山和馬里蘭,中國上海、蘇州、北京、廣州等。
官方網站:www.junshipharma.com
官方微信:君實生物