創新引領,驅動健康未來核心競爭力
作為中國大健康產業領軍企業之一的濟民可信集團始終秉持創新驅動發展的理念,將社會責任深植于創新研發的每一個環節,已建立涵蓋基礎研發、臨床前研究、臨床研究、新藥注冊上市全流程的研發體系,匯聚了海內外藥物研發、臨床醫學等領域的近800名優秀專業型人才。
《報告》顯示,濟民可信借助并融合AI技術加速新藥研發,通過AI技術迭代打造5大研發平臺,并以6大工藝平臺為基礎,濟民可信現有70余個在研新藥項目,13個新藥完成臨床研究并獲批上市,34項臨床試驗許可覆蓋腫瘤、腎病、疼痛等疾病領域,持續為公眾提供"療效顯著、安全可靠、價格可及"的藥物以及多元化、專業化的健康產品。
濟民可信以"振興中藥"為使命,他們認為在中醫藥行業發展浪潮中,創新是傳承的根本。近年來,濟民可信中藥類創新研發已累計獲國家及省級科技獎項12項,2大智造基地入選省級數字化轉型標桿,構建"研發-生產"全鏈質控體系,推動中藥產業向新質生產力升級,讓千年智慧綻放新質光輝。
濟民可信將"捍衛產品的質量就是捍衛患者的生命"作為其質量管理的核心理念,主動對標國際先進標準,部分產品已獲得FDA及歐盟認證,集團下屬多家公司通過了多個國家監管部門的質量安全檢查,歷年藥品抽檢合格率均為100%。同時,他們還通過員工培訓、合規管理等方式,讓安全意識與合規意識深深根植于每一個員工心中。
逐綠而行,構建可持續發展新范式
響應國家"雙碳"戰略,濟民可信將可持續發展融入運營全鏈條。他們通過開展分層分類培訓,有效幫助員工提升了環境風險識別能力與生態責任意識;通過倡導無紙化辦公、安裝太陽能路燈、綠色能源充電樁等清潔能源設施,全面推行綠色辦公場景升級。
濟民可信引入大量機器人和自動化設備,實現了對設備運行情況和能源消耗狀態的實時監控,以及各個環節的可追溯和數據化管理,有效提高藥材資源利用率,形成了"源頭減量-過程優化-末端治理"的綠色生產閉環。
在"兩山"理論和循環經濟理念引領下,濟民可信還建成了"中國首創、亞洲第一、全球最大"的煤制清潔燃氣生產基地,并投資建設"中國東部首個現代化石材產業基地",促進全球綠色發展,助力"雙碳"目標達成。
善澤四方,織就公益共生網絡
為響應國家鄉村振興戰略,濟民可信將中藥材種植與現代制藥產業深度融合,在云南省曲靖市富源縣黃泥河鎮打造薏苡種植基地,并與當地企業合作建立了薏苡烘干廠,有效提高了當地農戶的收入。
為推動基層醫療服務從"可及"向"優質"升級,縮小城鄉地區醫療條件差距,濟民可信還主導或參與了許多藥品捐贈、公益知識科普等活動。
二十余年來,濟民可信已累計捐贈逾7億元,獲得中華慈善總會"中華慈善突出貢獻獎"。2014年濟民可信發起成立了"濟民可信醫藥公益慈善基金會",并以此為基礎構建起了涵蓋醫療救助、科研創新、人才培養、學術交流、健康科普等領域的立體化公益體系。
濟民可信將員工視為核心資產,建立分層培訓體系、提供全場景福利保障,賦能職業成長;同時,他們還不斷完善合規架構與文化建設,確保決策透明、運營規范,持續提升企業治理水平,讓企業成為員工的精神家園。
在企業合規管理方面,濟民可信構建起了符合企業發展需求的多層次治理架構,設有專門的合規管理機構并長期開展合規文化的持續宣導,以強化決策透明、運營順暢,持續維護企業聲譽并獲得市場認可。
《報告》從環境、社會與治理三大維度清晰地勾勒出濟民可信如何將時代責任內化為發展動力,并闡述了其長期堅持的戰略:"濟民可信將致力于實現身心有所‘醫'、空氣有所‘益'、環境有所‘宜'、人人有所‘依'的品牌理想,為健康中國建設和全球綠色轉型貢獻‘可信'力量。"
如需更多信息
請聯系:PR@jemincare.com
 ]]>
]]>南昌2025年5月23日 /美通社/ -- 2025 年 5 月 22日,濟民可信集團宣布,公司自主研發的化藥 4 類抗腫瘤藥物濟立安 ®(鹽酸伊立替康脂質體注射液)已獲國家藥品監督管理局批準上市。該產品為國內第二家批準上市并視同通過一致性評價的仿制藥,將為晚期胰腺癌患者帶來新的治療選擇。
胰腺癌素以"三高三低"著稱——發病率高,復發率高,死亡率高,早期診斷率低,手術切除率低,藥物有效率低,被稱為"癌中之王"。傳統伊立替康注射液具備胰腺癌的確切療效,但患者長期使用易出現骨髓抑制、嚴重腹瀉及肝腎毒性等副作用,嚴重影響治療依從性。濟立安®采用的脂質體技術憑借其生物相容性高、靶向性強、毒副作用低等優勢,可顯著提升藥物安全性及耐受性。國際研究顯示,伊立替康脂質體聯合5-FU/LV方案治療吉西他濱化療失敗的轉移性胰腺癌患者,中位無進展生存期(PFS)與總生存期(OS)均有顯著改善[1]。
2022年4月,原研施維雅易安達®獲得國家藥品監督管理局正式批準,與5-氟尿嘧啶和亞葉酸聯合用于接受吉西他濱治療后進展的轉移性胰腺癌患者 [2]。濟民可信研發的仿制藥濟立安®(鹽酸伊立替康脂質體注射液)在臨床實驗中表現出色,臨床試驗結果顯示,該產品與原研制劑對比人體生物等效性完全一致。值得一提的是,濟立安®(鹽酸伊立替康脂質體注射液)是濟民可信今年內第二個獲批上市的脂質體產品,充分彰顯了濟民可信在高端創新制劑研發領域的實力和積累。
濟立安®(鹽酸伊立替康脂質體注射液)由濟民可信集團創新技術藥物研究院研發,由無錫濟煜山禾藥業股份有限公司落地生產。創新技術藥物研究院聚焦國際領先的高端創新制劑研發,擁有高端制劑、特色原料藥、創新中藥三大平臺,涵蓋脂質體、微球、吸入劑、口服固體、創新中藥、特色原料藥等技術研發,覆蓋腫瘤、鎮痛、呼吸、關節炎、抗感染、心腦血管、腎病、肝病等多個領域。
參考資料
[1]. Bang YJ,Li CP,Lee KH,et al.Liposomal irinotecan in metastatic pancreatic adenocarcinoma in Asian patients: Subgroup analysis of the NAPOLI-1 study. Cancer Sci 2019.
[2]. 施維雅胰腺癌治療藥物易安達®在中國獲批. Retrieved from https://mp.weixin.qq.com/s/5SWFDyqLbUmSMeZK-_jXug
南昌 2025年4月28日 /美通社/ -- 4月23日,英中貿易協會會長沙遜勛爵率"投資中國—跨國公司江西行"代表團專程走訪了濟民可信集團。圍繞創新藥物研發、智能生產、質量管控以及國際化布局與全球合作成果等方面,雙方展開了深入交流,為濟民可信集團進一步開展國際合作、實現創新成果全球共享創造了新的契機。
近年來,濟民可信持續加速推進創新藥研發以及商業化、國際化進程,先后與羅氏集團旗下基因泰克、美國RAPT、芬蘭奧立安集團和美國滬亞簽署了產品對外授權獨家合作協議。實現出海的4個創新藥物,覆蓋腫瘤、呼吸、疼痛等重大領域,為濟民可信走向全球化打下堅實基礎,被業界認作中國傳統藥企轉型升級的典型范例。
此外,濟民可信集團還大力推動"5G+智慧工廠"的建設,已在江西、江蘇、浙江等地建成多個符合FDA及歐盟標準的智能化生產基地,全面推行QbD(質量源于設計)、TQM(全面質量管理)等國際標準體系,確保產品從研發到生產的全鏈條可追溯,實現了生產效率與產品質量的雙效提升,為全球客戶提供了"中國質造"保障。
在國際市場拓展上,濟民可信集團的制劑與原料藥已出口50余個國家和地區,并在多個高技術壁壘的藥物領域與跨國藥品經銷商開展技術轉移、知識產權授權、合作開發等多元化合作,推動更多自主研發和生產的藥品進入歐美及新興國家市場。
"基于自身國際化經驗,濟民可信推出‘全球合作伙伴計劃',開放我們在國外的市場網絡、臨床開發及國際準入資源,助力國內藥企‘抱團出海'。"濟民可信集團國際業務負責人表示,國際化的目標是創造生態共贏,希望能夠搭建"出海"生態平臺,助力行業協同發展。目前,該平臺已吸引多家國內藥企共同參與,正大力推動更多"中國方案"在全球主流市場的臨床轉化與商業化進程。
在堅持"走出去"同時,濟民可信集團還積極引進國際領先藥物進入中國市場,以滿足日益增長的中國臨床需求,"雙向合作"的模式不僅加速了自主創新能力的提升,更使國內患者同步受益于全球領先療法。濟民可信集團國際業務負責人表示:"國際化不僅是市場拓展,更是技術、人才與標準的深度融合。期待通過雙向合作,讓中國創新惠及全球,也讓國際領先療法更快服務中國患者。"
]]>南昌2025年4月10日 /美通社/ -- 2025年4月9日,濟民可信集團宣布,公司自主研發的哮喘治療用藥舒力杰®(吸入用丙酸倍氯米松混懸液,2ml:0.8mg)已獲國家藥品監督管理局批準上市,成為國內首家獲批并視同通過一致性評價的仿制藥。
哮喘是一種常見的慢性炎癥性氣道疾病,癥狀嚴重時可出現呼吸困難和低氧血癥,臨床亟需高效、安全的吸入制劑以改善患者預后。在全球范圍內,2021年哮喘患者約2.6億,年死亡病例高達43.6萬例。我國20歲及以上人群哮喘患病率高達4.2%,患者人數約4570萬,且呈上升趨勢[1]。
研究表明,吸入性糖皮質激素可顯著降低急性發作風險,當前已成為哮喘長期控制的核心藥物[2]。吸入用丙酸倍氯米松混懸液作為國際公認的高效局部抗炎糖皮質激素(ICS),其原研藥由意大利凱西制藥開發,通過霧化吸入直接作用于氣道,可有效控制炎癥、緩解癥狀,并減少全身性激素副作用[3]。該藥物于2013年進入中國市場,已被《兒童霧化中心規范化管理指南》[4]列為推薦用藥,并獲《支氣管哮喘防治指南》及全球權威的《哮喘防治全球指南》(GINA)認可[5]。
此次濟民可信集團舒力杰®(吸入用丙酸倍氯米松混懸液)國內首仿上市,將為國內哮喘患者提供高效、安全的治療新選擇,為基層醫療機構和兒童患者提供更便捷的治療方案,并有助于降低我國對哮喘藥物的進口依賴。
舒力杰®(吸入用丙酸倍氯米松混懸液)由濟民可信集團創新技術藥物研究院研發,由江西艾施特制藥有限公司落地生產。創新技術藥物研究院聚焦國際領先的高端創新制劑研發,擁有高端制劑、特色原料藥、創新中藥三大平臺,涵蓋脂質體、微球、吸入劑、口服固體、創新中藥、特色原料藥等技術研發,覆蓋腫瘤、鎮痛、呼吸、關節炎、抗感染、心腦血管、腎病、肝病等多個領域。
]]>靶向克菌 重塑抗真菌治療新標桿
近年來,隨著廣譜抗生素、抗腫瘤藥物、免疫抑制劑等的廣泛應用,以及造血干細胞移植、器官移植等技術的開展,侵襲性真菌病的發病率及死亡率呈明顯上升趨勢。研究顯示[1],全球每年有超過 655 萬人受到真菌疾病的影響,導致超過 375 萬人死亡,其中約 255 萬人的死亡可直接歸因于真菌疾病,給臨床帶來巨大挑戰。
現階段,抗真菌藥物中三唑類、棘白菌素類,抗菌譜相對窄且容易出現耐藥;另外,普通兩性霉素B(AmB-D),腎毒性高且容易出現輸注反應,都未能充分滿足臨床需求。面對當前耐藥真菌、少見/罕見真菌的感染挑戰,亟需新型抗真菌治療方案,幫助患者渡過難關。
其中,兩性霉素B脂質體(L-AmB)憑借革命性脂質體包裹技術,精準輸送藥物至感染組織部位,游離藥物釋放減少,突破性實現高效殺菌與安全性雙提升。研究顯示[2][3]:L-AmB因脂質體體積小,較少被腎臟過濾,避免AmB與遠端小管細胞的相互作用,明顯改善腎毒性;同時因能降低促炎細胞因子的上調,進而減弱輸液反應。作為一款高效低毒的抗真菌利器,可為臨床醫生提供更優選擇。
突破壁壘 為患者提供更多選擇
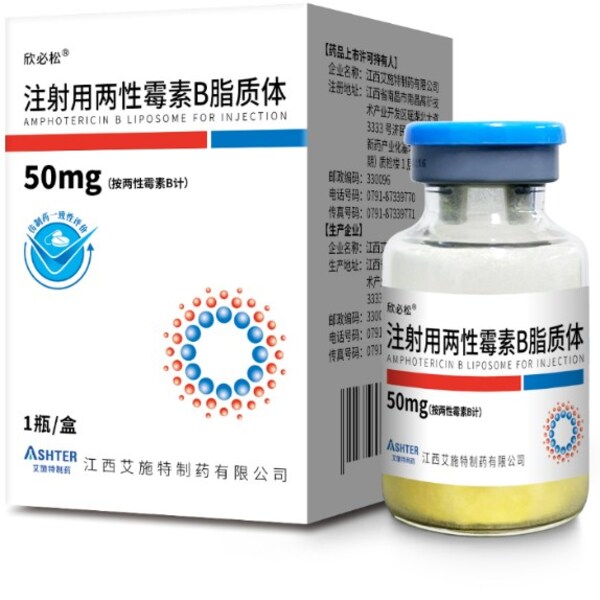
注射用兩性霉素B脂質體,已在全球范圍內廣泛使用近30年,被譽為侵襲性真菌病治療的"金標準"[3][4]。由于其技術壁壘高,面臨著活性成分水溶解性差、制備過程中易產生雜質、工藝多且復雜,周期長等眾多難題,研發挑戰巨大。
濟民可信集團創新技術藥物研究院利用脂質體技術平臺,突破關鍵技術,通過藥學、非臨床和臨床試驗研究證明了欣必松®(兩性霉素B脂質體)與參比制劑藥學和生物等效,并于2025年1月8日獲得國家藥品監督管理局核準簽發的《藥品注冊證書》。欣必松®按新4類注冊要求,以高標準研制,視同通過一致性評價,有望進一步降低臨床負擔,為中國侵襲性真菌病患者帶來更多獲益。
參考文獻
1. Denning DW. Lancet Infect Dis. 2024 Jul;24(7):e428-e438.
2. Adler-Moore J, et al. Clin Infect Dis. 2019,68(S4):S244-S259.
3. Aversa F, et al. J Chemother. 2017 Jun;29(3):131-143.
4. 中華內科雜志,2024,63(3):230-257.
注射用兩性霉素B脂質體(AmBisome®)已在全球范圍內廣泛使用近30年,被譽為侵襲性真菌病治療的"金標準",是世界首例被批準上市的納米脂質體藥物[1]。由于其技術壁壘高,此前國內仿制產品過評僅有一家。濟民可信集團創新技術藥物研究院利用脂質體技術平臺,突破關鍵技術,通過藥學、非臨床和臨床試驗研究證明了該產品與參比制劑AmBisome®藥學和生物等效,該產品的獲批上市可為患者帶來更多福音。
注射用兩性霉素B脂質體是兩性霉素B的小球型單層脂質體,擬用于系統性真菌治療。兩性霉素B與真菌細胞膜上的麥角固醇結合,形成跨膜離子通道,造成細胞膜通透性改變,最終導致真菌細胞死亡。與傳統兩性霉素B相比,兩性霉素B脂質體對真菌細胞的親和力高于哺乳動物細胞,增強了藥物靶向殺菌能力,能夠顯著提升藥物的安全性,有效降低不良反應率。臨床應用時無需劑量爬坡,可依據說明書足量給藥,將輸液時間自6h縮短至2h[2],使用更方便。
注射用兩性霉素B脂質體的研發、注冊申報由濟民可信高端制劑研發平臺完成,此平臺隸屬于濟民可信創新技術藥物研究院。該院聚焦國際領先的高端創新制劑研發,擁有高端制劑、創新中藥、特色原料藥三大平臺,涵蓋脂質體、微球、吸入劑、口服固體、創新中藥、特色原料藥等技術研發,覆蓋腫瘤、鎮痛、呼吸、關節炎、抗感染、心腦血管、腎病、肝病等多個領域。
]]>注射用JMX-2006是一款創新的緩釋制劑,代表了當前藥物制劑領先技術。通過制劑技術的創新,使得JMX-2006能夠在給藥周期內實現更平穩的藥物釋放,進而提升治療效果的持久性與藥物作用的安全性。針對已上市同類產品注射創口大、疼痛感強的臨床缺陷,JMX-2006通過劑型的改良可極大改善患者注射體驗,有望為癌癥患者帶來新的治療選擇。
該制劑技術通過可降解聚合物包裹藥物分子,控制藥物緩慢釋放,顯著減少給藥次數,改善患者體驗,提高藥物療效,成為了醫藥領域探索與創新的焦點,具有明顯的臨床優勢,當前已被廣泛用于精神、神經、疼痛、腫瘤等多個領域。此次JMX-2006的獲批臨床,是濟民可信集團在前列腺癌治療領域的重要突破,也是公司長期致力于新藥研發和創新戰略的又一重要成果。
注射用JMX-2006的研發、申報由濟民可信高端制劑研發平臺完成,此平臺隸屬于濟民可信創新技術藥物研究院。該院聚焦國際領先的高端創新制劑研發,擁有高端制劑、創新中藥、特色原料藥三大制劑平臺,涵蓋脂質體、微球、吸入劑、口服固體、創新中藥、特色原料藥等技術研發,覆蓋腫瘤、鎮痛、呼吸、關節炎、抗感染、心腦血管、腎病、肝病等多個領域。
]]>上海2024年12月24日 /美通社/ -- 上海濟煜醫藥科技有限公司(以下簡稱"濟煜醫藥")與RAPT Therapeutics, Inc.(以下簡稱"RAPT")——一家臨床階段的專注于為炎癥性疾病中未被滿足的重大需求的免疫學生物制藥公司,宣布雙方已簽訂JYB1904獨家許可協議(RAPT產品代號RPT904)。JYB904是濟煜醫藥開發的一款具有更高親和力及更長半衰期的抗IgE單克隆抗體。
根據許可協議的條款,RAPT被授予除中國大陸、香港、澳門和臺灣(統稱為"濟煜地區")以外的全球開發和商業化JYB1904的權利。作為回報,濟煜醫藥將獲得3500萬美元預付款,最高達6.725億美元的里程碑付款,以及未來的梯度銷售提成。一代奧馬珠單抗(Xolair®)已被批準用于多種過敏性疾病,包括哮喘、慢性自發性蕁麻疹(CSU)、慢性鼻竇炎伴鼻息肉以及最近的食物過敏。JYB1904旨在為患者提供一種相較于奧馬珠單抗更優的治療方案。濟煜醫藥正在中國區進行JYB1904治療哮喘和CSU的2期臨床試驗。RAPT計劃在2025年啟動食物過敏的臨床開發。
濟煜醫藥總裁李肖翔表示:"我們很高興與RAPT Therapeutics合作,推進JYB1904在食物過敏和其他過敏性疾病中的開發。我們相信,這次合作將顯著增強和加速JYB1904在全球的開發及商業化進程,從而造福患者。"
RAPT總裁兼首席執行官Brian Wong博士表示:"我們很高興與濟煜醫藥合作,并對RPT904成為食物過敏患者同類最佳新型治療選擇的潛力感到興奮。今年,奧馬珠單抗獲批用于食物過敏并快速普及,證實了這個市場在不斷增長,并存在高度未滿足的需求和巨大的機會。RPT904已在臨床上證明其可延長半衰期,使該分子具有了best-in-class的特性。我們計劃在2025年下半年啟動RPT904在食物過敏中的2b期臨床試驗。"
]]>JMX-2002脂質體注射液是一款集高效性、安全性于一體的創新藥物。脂質體作為藥物載體,能夠顯著提高藥物的靶向性和生物利用度,減少藥物對正常組織的損傷,從而增強療效并降低副作用。JMX-2002脂質體注射液正是利用了脂質體的這一獨特優勢,通過精準遞送藥物至病灶部位,實現對實體瘤的有效治療。該藥物的獲批臨床,不僅有望為癌癥患者帶來新的治療選擇,也為脂質體藥物研發領域注入了新的活力。
作為濟民可信的長期合作伙伴,上海美迪西生物醫藥股份有限公司依托脂質體藥物研發服務平臺,為JMX-2002脂質體注射液的研發提供了臨床前藥代動力學研究和GLP下的安全性評價服務,共同推進了藥物研發進程。
脂質體藥物作為一類備受矚目的改良型新藥,可以通過包裹藥物分子,改善藥物的溶解性、穩定性及靶向性,有效提高了藥物的療效和安全性,成為了醫藥領域探索與創新的焦點。期待JMX-2002脂質體注射液臨床試驗進展順利,早日為飽受實體瘤困擾的患者帶來生命的曙光與希望。
]]>據《柳葉刀》最新數據顯示,目前中國成人慢性腎病(CKD)的患病率為10.8%,患者總數高達1.3億,截至2023年底中國大陸地區透析CKD患者數量已達到 106.8萬人,而高磷血癥正是此類患者最常見的并發癥之一[1][2]。高磷血癥可直接加速腎衰及死亡進程,血磷每升高約0.3mmol/L,腎衰竭風險增加36%,心血管死亡風險增加50%。
碳酸司維拉姆是目前唯一被FDA批準的既不含鈣、又不含其他金屬的新一代磷結合劑,并被國內外指南和規范一致推薦為降磷首選藥物[3]。米內網數據顯示,司維拉姆2021年在中國三大終端6大市場合計銷售規模接近6億元,同比增長48.54%,2023年突破10億元。
相較片劑產品,碳酸司維拉姆干混懸劑將適用人群擴增至兒童群體,在用藥口感和順應性方面均有優勢,將與濟民可信集團已上市的碳酸司維拉姆片形成雙劑型供應,為患者提供更多治療選擇,讓更多患者獲益。
碳酸司維拉姆干混懸劑的研發、申報由濟民可信復雜制劑研發平臺完成,此平臺隸屬于濟民可信研發中心創新技術藥物研究院。該院聚焦國際領先的高端創新制劑研發,擁有復雜制劑、高端制劑、創新中藥三大制劑平臺,涵蓋脂質體、微球、吸入劑、口服固體、創新中藥、特色原料藥等技術研發,覆蓋腫瘤、鎮痛、呼吸、關節炎、抗感染、心腦血管、腎病、肝病等多個領域。
參考文獻:
[1] Zhang L, Wang F, Wang L, et al. Prevalence of chronic kidney disease in China: a cross-sectional survey . Lancet 2012; 379: 815–822. |
[2] 中國醫師協會腎臟內科醫師分會(CNA)2024年學術年會數據 |
[3] 中華腎臟病雜志(2022);38(5),453-464. |
上海2024年9月4日 /美通社/ -- 進入九月初,在云南省曲靖市富源縣黃泥河鎮這片土地上,20000 畝薏苡已進入灌漿期。農技人員正在指導農民以GAP基地標準進行科學管護,為薏苡產業提質增效提供技術支持。
薏苡仁有健脾利濕、清熱解毒、消腫散結等藥用功效,被譽為"植物珍珠",而黃泥河鎮年平均氣溫16℃,平均海拔1550米,降水豐富,無污染,是薏苡種植的理想地區。
多年前,濟民可信集團旗下浙江康萊特藥業有限公司運用現代制藥技術從薏苡仁中提取出了一種抗癌活性成分,并成功研制出一款中藥抗癌乳劑,經中、美等多國臨床試驗證明,該藥物對肺癌、肝癌、胰腺癌等中晚期惡性腫瘤具有顯著的治療效果[1]。
為保障該藥物的安全品質與市場供給,并響應國家鄉村振興戰略,2023年濟民可信集團與黃泥河鎮結緣,開始在當地打造薏苡種植基地,以GAP基地標準精耕細作,為當地農戶帶來實實在在的收益,奏響了一曲產業興農的動人樂章。
"最初,農戶的顧慮還比較多。"為了讓當地農戶安心踏上薏苡種植之路,濟民可信采購管理部員工劉志剛、萬文豪等人通過庭院會、進村入戶等多種方式對薏苡種植進行廣泛宣傳,并精選優質的薏苡種子免費發放給當地農戶。
這些種子如同希望的火種,點燃了農戶們致富的夢想。
從前期的土地規劃到精心的播種,從科學的田間管理到及時的病蟲害防治,每一個環節都凝聚著濟民可信與農戶們的共同心血。為了保障農戶和村合作社的利益,濟民可信集團還承諾薏苡保底收購、承諾收購價格隨行就市,并拿出了按量返利等一系列的惠農政策。
這些舉措,減少了農戶及合作社在面對市場波動時的后顧之憂,極大地提高了種植積極性。2年不到的時間,薏苡種植已經開始成為黃泥河鎮的支柱產業,為當地農民帶來了300-500元/畝的增收,越來越多的農民因此走上了致富的道路。
目前,黃泥河鎮12個村(居)委會81個自然村的薏苡種植戶、種植面積分別較2023年增長了107%、67%,增加至4259戶、20000畝;預計2025年的規模還將進一步擴大,分別增加至4800戶、22500畝。
在幫助黃泥河鎮不斷擴大薏苡種植規模的同時,濟民可信還積極探索產業發展的新模式,與當地企業合作建立了薏苡烘干廠。這不僅解決了農戶的銷售難題,還延長了產業鏈,提高了產品附加值,為當地村民就業增收創造了更多機會。
未來,濟民可信集團將繼續秉承"濟世惠民,信待天下"的企業使命,堅持"捍衛產品質量就是捍衛患者的生命"的質量方針,從種源、種植、施肥打藥到采收加工,每一道環節均以GAP基地標準在黃泥河這片土地上精耕細作,讓薏苡種植產業不斷發展壯大,為企業提供質量可靠的薏苡原料,實現企業與農戶的互利雙贏,共同書寫好鄉村振興大文章。
帕金森病是一種常見的老年神經系統退行性疾病,癥狀包括靜止性震顫、肌強直、運動遲緩、認知障礙等,病情隨著時間加重,給患者家庭和社會造成極大負擔。鹽酸羅匹尼羅作為新型多巴胺受體激動劑,可以進入中樞神經系統,作用于突觸后膜上的多巴胺能受體,通過發揮藥理學作用,可以改善患者的運動遲緩、肢體的震顫、肌張力增高等臨床表現,是治療帕金森病的常用藥之一[1]。
鹽酸羅匹尼羅緩釋片多用于與左旋多巴聯合治療帕金森病,可以延緩病情,顯著減少關期時間(帕金森病患者服用多巴胺替代藥物期間,癥狀會突然在緩解和加重之間波動,緩解期又叫做開期,加重期稱為關期),且安全性較好,相較于羅匹尼羅普通片,減少了服用次數,極大地增加了患者的用藥依從性[1] [2]。
據米內網數據,鹽酸羅匹尼羅緩釋片近5年全國公立醫療機構終端銷售額均超億元,占市場規模不足多巴胺激動劑總體銷售規模的1%。隨著我國老齡化程度的進一步加劇,羅匹尼羅緩釋片未來市場空間巨大,作為國內首仿產品,將幫助更多帕金森病患者受益。
該項目源于濟民可信高端口服固體制劑平臺,此平臺隸屬于濟民可信研發中心創新技術藥物研究院,涵蓋速釋制劑、緩釋制劑、難溶性藥物增溶(含熱熔擠出)及多顆粒給藥系統,研發設施配置先進完備,擁有豐富的制劑研發及產業化技術經驗及資源。近年來,依托這一平臺濟民可信已實現數項高端仿制藥的技術突破,多個產品獲批。在研項目中多個項目已完成放大生產與臨床BE,相關產品有望陸續獲批上市。
參考文獻
1. 中華醫學會神經病學分會帕金森病及運動障礙學組,中國醫師協會神經內科醫師分會帕金森病及運動障礙學組.中國帕金森病治療指南(第四版)[J].中華神經科雜志,2020,53(12):973-986.
2. 抗帕金森藥物-羅匹尼羅. Retrieved from https://m.haodf.com/neirong/wenzhang/7950574580.html
]]>血小板減少癥是一種出血性疾病,嚴重性血小板減少癥如慢性肝病(CLD)、慢性原發免疫性血小板減少癥(ITP)具有較高的自發性出血,嚴重者甚至可以危及生命。
作為全球首個經FDA、EMA批準,擁有CLDT、ITP雙適應癥的血小板生成素受體激動劑(TPO- RA),馬來酸阿伐曲泊帕片通過刺激巨核細胞從骨髓祖細胞的增殖分化,促進血小板的生成,可短時間內(治療后3-5天)快速提升血小板計數,安全且耐受性良好,口服用藥方式不受食物類型限制,大大提高了血小板減少癥患者的生活質量[1] [2]。
從近年來的臨床需求來看,該產品市場發展非常迅速且前景廣闊。根據米內網數據,2023年度馬來酸阿伐曲泊帕片銷售額為10.15億元,是2020年的58倍,上市三年以來平均年增長率為772%,且預計將繼續持續增長。本品的獲批上市,將有助于進一步擴大市場覆蓋率。依托"原料藥+制劑"一體化優勢,濟民可信集團馬來酸阿伐曲泊帕片和原料藥陸續獲批上市,將為患者提供更多治療選擇,并進一步豐富公司產品結構,有助于持續穩定市場份額。
該品種源于濟民可信高端口服固體制劑平臺,涵蓋速釋制劑、緩釋制劑、難溶性藥物增溶、以及多顆粒給藥系統,研發設施配置先進、完備,擁有豐富的制劑研發及產業化技術經驗及資源。近年來,依托這一平臺濟民可信已實現數項高端仿制藥的技術突破,目前已完成5個產品的注冊申報,BE試驗均為一次性通過,多個項目正在研發中。
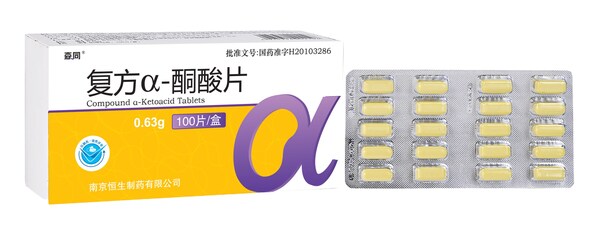
]]>慢性腎臟病(CKD)是各種原因引起的慢性腎臟結構和功能障礙,根據《柳葉刀》最新研究數據,CKD在我國的患病率高達10.8%,患病人數超過1億。隨著疾病的進展,開始發生腎損害,腎功能不斷下降,嚴重危害生命健康。對于腎臟功能衰退的患者,就需要限制蛋白攝入,從而減輕參與腎單位的高負荷工作狀態,低蛋白飲食治療是CKD患者非透析治療的重要手段,但單獨限制蛋白飲食,則會導致營養不良,間接加重慢性腎臟病。
復方α-酮酸片使這一矛盾得以解決,能補充患者的營養,使低蛋白飲食得以維持,從而減輕腎臟負擔,延緩慢性腎臟病進展。它不僅是CKD患者營養治療的補充劑,更是CKD患者多種代謝紊亂(蛋白質、脂類和糖代謝,鈣磷代謝和代謝性酸中毒)的調節器。據米內網數據顯示,復方α-酮酸片2023年全國公立醫療機構終端銷售額近30億,5年增長21%。
該項目源于濟民可信高端制劑平臺,此平臺隸屬于濟民可信醫藥產業集團創新技術藥物研究院,涵蓋速釋制劑、緩釋制劑、難溶性藥物增溶(含熱熔擠出)、及多顆粒給藥系統,研發設施配置先進完備,擁有豐富的制劑研發及產業化技術經驗及資源。近年來,依托這一平臺濟民可信已實現數項高端仿制藥的技術突破,目前已完成多個項目的放大生產與臨床BE,相關產品有望在今年陸續獲批上市。
]]>多年來,濟民可信集團始終堅持"濟世惠民、信待天下"的企業使命,將履行社會責任和實現公共價值置于最優先事務。當下,濟民可信集團正持續打造新質生產力,致力于實現身心有所"醫"、空氣有所"益"、環境有所"宜"、人人有所"依"的品牌理想。
6月5日,濟民可信集團在"世界環境日"首次發布ESG報告——《濟民可信2018-2023環境、社會及治理報告》(以下簡稱ESG報告),圍繞恪守合規公平、造福人類健康、踐行公益慈善、助力員工發展、保護生態環境等五個維度,用嚴謹的數據說話,展現企業近年來在可持續發展領域的實踐經驗與成果,彰顯了濟民可信集團聚焦打造新質生產力,追求高質量可持續發展的決心。
創新研發守護人類健康
濟民可信專注于創新藥(化學藥和生物藥)、特色中藥、高端復雜仿制藥/改良創新藥等開發與創新,通過自主研發、產學研結合以及國際化科研合作,為患者提供"價格可及、療效顯著、安全可靠"的臨床亟需藥物。
ESG報告將創新研發作為企業打造新質生產力最重要的組成部分。報告顯示,截至2023年底,濟民可信醫藥產品研發投入近50億元,在研新藥項目70余個,累計獲批臨床試驗許可30個,累計9個產品獲批上市。2024—2028年濟民可信還將投入100億用于創新藥研發。
濟民可信現有醫藥研發相關科研人員超600人,設有1個國家級博士后科研工作站,1家獲CNAS認證的國家級實驗室,9個省級工程技術中心和3個中試平臺,并與多所知名院校共建制藥工業關鍵技術聯合實驗室。
截至2023年底,集團共申請國內專利140余項,其中38項已獲授權;申請海外專利合作條約(PCT)50余項。濟民可信現有產品批件700余個,均通過GMP認證,部分產品獲得FDA及歐盟認證,產品獲準進入美國、俄羅斯、以色列、西班牙等50多個國家和地區。
綠色發展助力"雙碳"目標
生態環境保護、清潔能源生產、綠色礦產開發是濟民可信在ESG報告中環境責任部分的重要內容。
報告顯示,濟民可信2018年起在江西高安市建設煤制清潔燃氣生產基地,以集中供氣模式改變原煤氣發生爐小、散、亂現狀。經過兩年的試運行,2022年濟民可信清潔能源項目全面供氣,通過40余公里的供氣管線,清潔的工業燃氣源源不斷地輸向建陶基地內陶瓷企業的85條生產線。使用清潔能源后,每年可為基地企業節約標準煤26.3萬噸,相當于82萬個家庭一年的用電量;每年減排二氧化碳70.3萬噸,相當于種植3800萬棵樹,并極大解決酚水、焦油等環境污染問題。
濟民可信還投身礦產資源開發的轉型升級,在上饒德興市投資建設"中國東部首個現代化石材產業基地",以綠色低碳、可持續發展為原則,努力打造綠色礦山的"江西樣板",構建集資源開采、產品加工、尾礦利用、物流運輸等一體化的循環經濟新模式。
公益善行彰顯責任擔當
ESG報告顯示,多年來濟民可信在抗震救災、抗擊疫情、鄉村振興、健康可及、支持教育等方面投入大量資金、物資與人力,捐贈累計近7億元,獲得中華慈善總會"中華慈善突出貢獻獎"。
濟民可信以健康民生為己任,積極開展健康科普與醫患教育,圍繞科學用藥和安全用藥與公眾開展良性互動,同時通過慈善藥物援助,進一步讓患者受益,以提升醫療可及性,為建設"健康中國"貢獻力量。
濟民可信以反不當競爭、反壟斷、財稅合規、產品推廣、數據安全與隱私保護、商業伙伴合規以及知識產權保護等為合規管理重點,建立了覆蓋事前、事中、事后的合規管理全流程,建立完整的合規管理架構以及合規管理機制,保障集團踐行良好的商業道德。
此外,濟民可信堅持以人才經營為核心發展戰略,構建多元化培訓體系,助力員工職業發展,實現員工培訓覆蓋率100%;其線上學習平臺發布培訓項目163個,覆蓋24961人次,人均培訓時長超過50小時。
JYB1904是上海濟煜大分子創新研究院自主研發的靶向IgE重組人源化單克隆抗體創新藥,擁有自主知識產權,屬生物制品1類新藥,此前已獲批開展中至重度過敏性哮喘臨床試驗,目前已完成的I期臨床試驗數據顯示其安全性良好,半衰期較長,支持開展臨床II期試驗。此次獲批臨床的慢性自發性蕁麻疹是JYB1904的第2個臨床適應癥。
慢性自發性蕁麻疹是一種以風團和瘙癢為主要表現的常見慢性皮膚疾病,約20%的患者伴有血管性水腫,給患者日常生活帶來極大困擾,并且近一半患者對口服第二代H1抗組胺藥物應答不足,亟待療效更持久的藥物來控制疾病。
相比目前已有藥物,JYB1904的親和力更高,人源化程度更高,具有更優的穩定性,可實現高濃度皮下注射劑給藥。臨床前研究結果顯示,JYB1904能夠與游離IgE特異性結合,阻斷IgE與其受體結合,體外生物學活性和體內藥效均優于目前藥物。除此以外,無論是動物體內還是I期臨床數據均顯示,JYB1904具有顯著延長的半衰期。
如上研究結果表明,JYB1904注射液具有優良的臨床治療潛力,可為中至重度過敏性哮喘、慢性自發性蕁麻疹等過敏性疾病的臨床治療提供潛在新方案,改善患者生活質量,減輕患者疾病負擔。濟民可信將積極推進JYB1904的臨床試驗,拓展JYB1904在慢性自發性蕁麻疹等過敏性疾病的臨床治療,力爭惠及更多患者。
- 關于上海濟煜醫藥科技有限公司
上海濟煜醫藥科技有限公司是濟民可信集團的研發中心及全資子公司,致力于成為具有全球影響力的藥物研發中心,其研發管線涵蓋生物大分子創新藥、化學小分子創新藥、創新中藥、創新制劑及復雜仿制藥。當前,大分子創新研究院已有6個項目進入臨床研究,2023年有3個單克隆抗體項目獲批IND,并有多個大分子單抗、雙抗以及多肽偶聯藥物等在未來兩年會陸續進入IND申報階段。
2023年上海濟煜醫藥科技有限公司有13個在研項目獲準進入臨床,其中4個獲FDA許可在美國開展臨床試驗。目前,公司正快速推進相關臨床試驗,爭取早日為患者帶來福音。
- 關于濟民可信集團
濟民可信集團創建于1999年,總部位于中國南昌,主要產品管線為腎病、腫瘤、心腦血管、呼吸抗感染、疼痛五大領域,致力于為患者提供高質量的藥品和創新醫藥解決方案。作為中國領先的大型現代制藥集團之一,濟民可信集團已連續多年位列中國醫藥工業百強前十。
如需更多信息
請訪問: www.jemincare.com
JMB2004注射液為國內首創治療膿毒癥類抗體藥物
JMB2004注射液的美國臨床試驗申請于2023年12月19日獲得FDA批準,同意本品開展治療膿毒癥及膿毒癥休克的臨床試驗。全球每年新發膿毒癥病例超過4890萬,其相關死亡人數達1100萬,我國每年約有近250萬膿毒癥患者,并有超過70萬患者死亡。膿毒癥是嚴重威脅人類健康的重大疾病之一,目前臨床主要采用抗感染和對癥支持等非特異性治療方法,尚無有效的針對性治療藥物。
臨床前研究表明使用JMB2004抗體進行治療,可以顯著改善膿毒癥癥狀,提高動物的存活率。與對標抗體相比,JMB2004抗體具有更低的免疫原性以及更高的親和力,以及無毒副作用、安全性高、給藥頻率低等優勢。目前國內尚無用于治療膿毒癥的抗體藥物,JMB2004作為國內首創治療膿毒癥類抗體藥物,有望填補該治療領域的空白并成為BIC藥物。
臨床前研究顯示 JYB1931注射液結合MASP-2優勢明顯
JYB1931注射液于2023年10月16日獲得NMPA批準開展用于IgA腎病患者的臨床試驗。JYB1931是上海濟煜大分子創新研究院自主研發的靶向MASP-2重組人源化單克隆抗體創新藥,擁有自主知識產權,屬生物制品1類新藥,擬用于治療IgA腎病。
IgA腎病是我國最常見的原發性腎小球疾病,是一種嚴重的、可危及生命的進行性加重免疫性疾病,會導致腎功能逐漸下降,最終導致腎功能衰竭。MASP-2(甘露聚糖結合凝集素絲氨酸蛋白酶2)是補體系統凝集素途徑的效應酶,能夠裂解C2和C4,進而激活補體系統,介導了炎癥性疾病的進程,抑制MASP-2可以緩解多種炎癥性疾病或罕見病的進程。
臨床前研究數據顯示,JYB1931特異性高親和結合MASP-2,優于目前臨床進度最快的同類型藥物近百倍,并且在人MASP-2轉基因小鼠中,相同劑量下JYB1931的半衰期更長,最大藥物暴露濃度更高,JYB1931能顯著減輕蛋白尿造成的腎細胞凋亡。
]]>12月20日,JMKX003801注射液獲國家藥品監督管理局批準,同意本品開展革蘭氏陰性菌引起的嚴重感染的臨床試驗。抗生素,尤其是碳青霉素耐藥在大腸埃希菌、肺炎克雷伯菌、鮑曼不動桿菌和銅綠假單胞菌的發生頻率逐年升高,JMKX003801在機制上可以很好地克服現有碳青霉素出現的耐藥,臨床前研究表明具有抗菌譜廣的特點,預期能夠解決現有臨床上抗生素的耐藥問題。
12月12日,JMKX003142片獲國家藥品監督管理局批準,同意本品開展腎性水腫的臨床試驗。我國慢性腎病CKD患病總人數估計高達1.2億,而CKD后期蛋白尿等升高會造成身體水腫。本品是最新一代的利尿劑,研究數據顯示其排水同時會有更小的副作用,預期將改善腎病患者的生活質量。
11月28日,JMKX003948片獲國家藥品監督管理局批準,同意本品開展腎細胞癌的臨床試驗。我國腎癌每年新發6-8萬人,在TKI和/或免疫療法PD-1等治療失敗后缺乏其他新機制的藥物,JMKX003948通過不同的治療機理和途徑,在臨床前研究中無論是單用還是聯用在動物模型上都取得了顯著療效。
12月12日,JMKX000197注射液的美國臨床試驗申請獲得FDA批準,該創新藥物此前已在10月19日獲國家藥品監督管理局批準,同意本品開展BCG治療失敗的非肌層浸潤性膀胱癌臨床試驗。膀胱癌是泌尿系統最常見的惡性腫瘤,我國每年新發約8萬患者。JMKX000197可以調控免疫系統和細胞因子等,臨床前研究表明在BCG治療無應答的動物模型里,有顯著的抗腫瘤作用。
而在稍早前的11月9日,JMKX003002片的美國臨床試驗申請亦獲得FDA批準,同意本品開展治療終末期腎病透析患者的高磷血癥的臨床試驗。我國慢性腎病CKD患病總人數估計高達1.2億,CKD會導致高磷血癥及其誘發的礦物質和骨等異常(CKD-MBD)。本品是最新一代的降磷劑,口服順應好,相比競品具有體外持久活性高,有望能夠持久降血磷,改善腎病患者的生存質量。
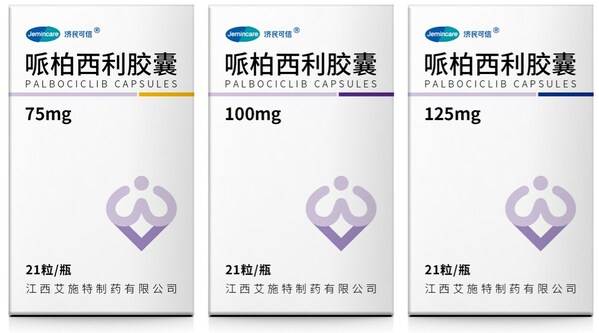
]]>作為一款在2015年獲批上市的乳腺癌新藥,哌柏西利是全球首個細胞周期蛋白依賴性激酶(CDK)一線療法,用于治療未曾接受過系統治療的雌激素受體陽性(ER+)、人表皮生長因子受體 2 陰性(HER2-)的絕經期女性晚期乳腺癌[1],2018年獲批進入中國市場,目前已在全球80多個國家上市,長期占據美國CDK抑制劑絕大部分市場份額,2022年全球銷售額達到51.2億美元[2]。
濟民可信集團充分發揮“原料藥+制劑”一體化優勢,哌柏西利原料藥和膠囊陸續獲批上市,將為患者提供更多治療選擇,并進一步豐富公司產品結構,有助于持續穩定市場份額。
該品種由集團旗下子公司上海濟煜醫藥科技有限公司承擔研發,旗下創新技術藥物研究院打造濟民可信高端口服固體制劑平臺,涵蓋速釋制劑、緩釋制劑、難溶性藥物增溶、以及多顆粒給藥系統,研發設施配置先進、完備,擁有豐富的制劑研發及產業化技術經驗及資源。近年來,依托這一平臺濟民可信已實現數項高端仿制藥的技術突破,目前已完成4個產品的注冊申報,BE試驗均為一次性通過,多個項目正在研發中。
- 關于上海濟煜醫藥科技有限公司
上海濟煜醫藥科技有限公司是濟民可信集團全資子公司,致力于成為具有全球影響力的藥物研發中心,其研發管線涵蓋生物大分子創新藥、化學小分子創新藥、創新中藥、復雜仿制及高端制劑。哌柏西利膠囊的研發申報由該公司創新技術藥物研究院完成,該院聚焦國際領先的高端創新制劑研發,覆蓋腫瘤、鎮痛、呼吸、關節炎、抗感染、心腦血管、腎病、肝病等多個領域,擁有脂質體、微球、吸入劑、口服固體、創新中藥和特色原料藥等六大創新技術研發平臺。
- 關于濟民可信集團
濟民可信集團創建于1999年,總部位于中國南昌,主要產品管線為腎病、腫瘤、心腦血管、呼吸抗感染、疼痛五大領域,致力于為患者提供高質量的藥品和創新醫藥解決方案。作為中國領先的大型現代制藥集團之一,濟民可信集團已連續多年位列中國醫藥工業百強前十。
參考文獻:
[1] 抗乳腺癌新藥palbociclib [J]. 劉恕,徐軍,崔毅. 藥學進展. 2015,39(08)
[2] Cortellis-Generics數據庫
我國目前20歲及以上人群哮喘患病率為4.2%,患者總人數達到4570萬[1]。此外,約1億人罹患慢性阻塞性肺病(COPD),已成為我國居民第三位主要死因[2],吸入藥物是治療哮喘和COPD的首選療法。
吸入用復方異丙托溴銨溶液活性成分為異丙托溴銨和硫酸沙丁胺醇,其中異丙托溴銨通過作用于氣道平滑肌M受體發揮氣道擴張作用,硫酸沙丁胺醇通過作用于氣道平滑肌β2受體發揮氣道擴張作用。一項為期85天的隨機、平行分組研究比較了霧化吸入3.0mg硫酸沙丁胺醇、0.5mg異丙托溴銨或復方制劑治療的療效,該項研究結果顯示,相較于單一成分的藥物作用于單一受體,吸入用復方異丙托溴銨溶液的兩個活性成分分別作用于肺部的M受體和β2受體,起到協同作用,擴張氣道作用更強[3]。
上海濟煜與艾施特制藥合作打造國內領先的吸入制劑研發生產平臺,覆蓋干粉吸入劑、吸入氣霧劑、吸入溶液/混懸液、以及其它粘膜給藥制劑等多種劑型,通過局部給藥的方式快速、直接進入肺部發揮藥效,降低給藥劑量,提高藥物療效,該平臺未來將有多個產品陸續進入注冊申報階段,造福更多患者。
參考文獻:
[1] Chen Wang, Jiangying Xu, Lan Yang, et al. Prevalence and risk factors of chronic obstructive pulmonary disease in China (the China Pulmonary Health [CPH] study) a national cross-sectional study. Lancet 2018 Vol 391 1706-1717.
[2] Kewu Huang, Ting Yang, Jiangying Xu, et al. Prevalence, risk factors, and management of asthma in China a national cross-sectional study. Lancet 2019 Vol 394 407-418.
[3] Routine nebulized ipratropium and albuterol together are better than either alone in COPD. Chest 1997, 1514-1521