中國抗癌協會是中國科學技術協會主管、中華人民共和國民政部注冊登記、具有獨立法人資格的腫瘤學科的國家一級學會。自1984年成立以來,積極開展腫瘤學科的臨床與基礎性研究,開展腫瘤專業繼續教育培訓,創辦多種形式的腫瘤學習培訓班,積極推廣新成果、新技術,舉辦國內外腫瘤學術會議,推動開放型、樞紐型、平臺型建設,為推進我國腫瘤防控事業做出了重要貢獻。
蘇州醫朵云健康股份有限公司是一家以數字醫療為核心的企業,致力于提高醫療效率和質量,提供智慧醫療互聯網服務和數字醫療產品。解決方案圍繞學術科研及患者服務,包括專病庫、患者服務、數字療法、影像服務等,深耕腫瘤、慢病等領域。團隊成員均來自醫療、醫藥、人工智能、信息技術、數據科學、網絡安全等高科技領先企業。與國內外頂級高校及科研機構、研究型醫院、世界500強醫療企業建立了深度技術合作及伙伴關系。
在此基礎上,醫朵云堅守以"患者為中心"理念,秉承中國抗癌協會CACA指南中的"防-篩-診-治-康,評-扶-控-護-生"十字方針,從學術科研、患者服務等多維度與中國抗癌協會達成共同目標,開展戰略合作。
相互賦能,打造多元化腫瘤防治科普體系:一方面,通過短視頻與圖文科普、患者故事等多樣化內容構建特色科普專欄,讓醫護共同參與到CACA指南科普傳播中,積極推動提升CACA指南社會影響力,促進腫瘤整合防治事業的發展。另一方面,通過開展患者康復活動、義診等形式,整合資源、升級服務,幫助腫瘤患者樹立抗癌信心,提升自我疾病管理能力,助力患者康復之路。
強強聯手,推進腫瘤患者數字化全病程管理:在中國抗癌協會的指導下,醫朵云發揮自身優勢,提供圍繞腫瘤患者全程管理數字化解決方案,雙方共同構建學術科研+患者服務閉環,通過真實世界數據積累進一步為指南的推廣、更新提供決策依據,促進醫療AI等創新成果轉化,創新引領腫瘤防治事業未來。
本次合作將有助于降低中國癌癥發病率及死亡率,并更好地滿足人們群眾健康需求。雙方將攜手并進,共同推動中國癌癥防控事業的發展,助力實現"健康中國2030"規劃綱要。
中國公益節設立于2011年,是國內首個由大眾媒體聯袂發起的以“公益”命名的節日。活動旨在弘揚公益精神,倡導公益行為,搭建多方深度對話、合作溝通的平臺。歷經十余年的探索和實踐,公益節已經成為中國公益慈善領域極具影響力的年度盛事。公益界、學界、傳媒界等領域超1200名杰出代表出席本屆公益節,超300家媒體報道關注,影響和互動人數超3000萬。
此次斬獲殊榮的公益項目為恒瑞醫藥“全力去愛”乳腺癌防治科普項目。為積極響應《“健康中國2030”規劃綱要》,恒瑞醫藥“全力去愛”患者關愛公益品牌已連續3年開展形式多樣的乳腺癌防治科普公益活動,旨在連結權威乳癌專家、行業協會、患者組織、媒體及患者關愛生態圈內的合作伙伴,共同傳遞乳腺癌早篩早診和規范治療相關核心知識要點,倡導患者及廣大女性同胞加強身心關懷,關注精神心理康復,進一步提升我國乳腺癌患者的5年生存率,改善患者生命質量。
2020年“全力去愛”中國乳腺癌患者健康管理粉紅絲帶防治科普行動
聯合知名乳腺癌專家、乳腺癌康復明星、小紅書/微博健康達人開展乳腺癌防治宣教直播活動,連結國家腫瘤質控中心乳腺癌專家委員會、中國癌癥基金會、樂活者聯盟等各方力量,在全國范圍內共同開展近30場線上、線下乳腺癌防治科普活動,旨在面向公眾和患者普及全方位、全周期的乳腺癌防治知識,呼吁社會公眾關愛乳腺癌患者,鼓勵患者堅定戰勝癌癥的信心,積極科學應對疾病。
2021年“全力去愛-五整生”康復沙龍
聯合中國抗癌協會各地康復會,在全國范圍內開展“五整生”康復沙龍,為度過5年康復期乳腺癌患者慶生,分享成功康復經驗,從“生物-心理-社會”全方位的醫學模式幫助患者早日康復。
2022年 “在這里遇見力量”乳腺健康科普工作坊暨“全力去愛-粉紅陪伴計劃”發布
聯合中國抗癌協會科普專業委員會、上海粉紅天使癌癥病友關愛中心、乳腺癌康復者、醫生專家和身心治療師,從身心關懷維度,提升公眾對乳腺癌早診早篩的意識,分享乳腺癌康復者的抗癌體悟,倡導患者及女性同胞關注心理健康,掌握放松身心的有效方法。攜手上海粉紅天使癌癥病友關愛中心啟動“全力去愛-粉紅陪伴計劃”,為廣大新發乳腺癌患者提供暖心陪伴福利,祝福乳腺癌患友們重塑生命之美,活出更廣闊的人生。
恒瑞醫藥“全力去愛”患者關愛公益品牌創建于2020年,致力于集結各方力量,積極探索與創新醫療服務生態伙伴的廣泛合作,為腫瘤患者提供覆蓋全瘤種的優質原研創新藥和全病程、全身心的患者關愛服務,并感召全社會關愛癌癥患者家庭,以正能量鼓舞患者家庭,樹立抗癌信心,重塑生命之美。
長期以來,恒瑞醫藥秉承“以患者為中心”的理念,始終把患者的健康福祉放在首要位置。恒瑞醫藥深刻關注中國乳腺癌領域的治療困境,圍繞未滿足的臨床需求,持續探索更多乳腺癌治療方案。截至目前,恒瑞醫藥已針對乳腺癌治療研發了2款1.1類原研創新藥物吡咯替尼和達爾西利,為中國乳腺癌患者提供了更多的治療選擇。恒瑞醫藥乳腺癌領域臨床研發的產品管線布局豐富、梯隊合理,覆蓋了多種乳腺癌亞型和不同作用機制的藥物,涉及晚期二線、晚期一線、新輔助/輔助各疾病階段適應癥人群。
乳腺癌發病趨于年輕化 專家呼吁早發現早治療
根據2020年世界衛生組織國際癌癥研究機構(IARC)發布的數據,乳腺癌已成為全球第一大惡性腫瘤。在我國,乳腺癌發病率增長迅速,已位列中國女性腫瘤發病譜首位[1]。相比西方國家,亞洲國家的年輕乳腺癌發病率更高。在美國,50歲以下乳腺癌患者占21%[2],而我國50歲以下乳腺癌患者達57.4%,絕經前乳腺癌患者的比例更高,達62.9%[3]。這與種族、遺傳基因、生殖和激素因素、心理因素、肥胖、嗜酒、不良飲食及生活習慣等綜合因素有關。
中國抗癌協會科普宣傳部部長支修益教授表示:"疫情后,全球精神障礙疾病愈加嚴重。長期處于抑郁焦慮高壓狀態的女性更易得乳腺癌。這也是我國乃至全球女性乳腺癌發病率增高的重要原因。值此國際乳腺癌關注月之際,中國抗癌協會科普專業委員會聯合多家乳腺癌科普教育基地及患者組織開展系列科普項目,期待能夠將乳腺癌‘早預防、早診斷、早治療、早康復'的理念,傳遞給千萬女性,呼吁大眾關注乳腺健康。"
上海交通大學醫學院附屬瑞金醫院腫瘤科副主任醫師瞿晴教授在活動中提到:"每位女性都應該對自己的健康負責。建議女性朋友養成運動習慣,不熬夜,少喝酒,多攝入新鮮蔬菜和高膳食纖維,哺乳期堅持母乳喂養,保持愉悅平和的情緒狀態,可有效降低罹患乳腺癌的風險。此外,乳腺自檢不可少。如發現無痛性的、質地較硬的、邊界不清的腫塊、皮膚破損或凹陷等異常情況,應及時就醫檢查。40-45歲人群可每年進行一次B超篩查,對于有遺傳等高危因素的人群,35歲起即需篩查。早發現,早治療,早期乳腺癌的治愈率可達到90%以上,且可以進行保乳,不影響生活質量。"
發揮群體抗癌力量 堅持規范全程治療
雖然我國乳腺癌發病率增長迅速,但隨著各類新技術、新藥品的不斷問世,乳腺癌治療逐已逐漸轉變為慢病化管理,越來越多的轉移或復發的晚期乳腺癌患者實現了高質量的長期生存。
乳腺癌康復病友代表在活動上分享:"感謝在我黑暗無光的那段歷程中遇見瑞金醫院的醫護和粉紅天使的姐妹們。這場疾病讓我學會了如何好好愛自己,在各種社會家庭的角色中如何更好地與人相處。病友的支持讓我感受到愛,康復后我投身公益事業,在傳遞愛付出愛的過程中,我感到自己的生命重新獲得了綻放,在大愛中找到了內心力量。"
上海粉紅天使癌癥病友關愛中心主任陸柳梅女士表示:"自2011年成立上海粉紅天使癌癥病友關愛中心以來,我們秉承‘以專業服務提升生命品質,以人文關懷讓乳癌成為祝福'的使命,根據不同病程的需要,為病友們提供身心社靈、全人、全家、全程、全隊的關懷服務。在學姐帶學妹的同伴支持過程中形成了粉紅天使的獨特文化:接受愛、學習愛、傳遞愛。我們欣喜地看到,群體抗癌的力量顯著促進了病友們的身心康復,提升了她們的生命質量。"
瞿晴教授強調:"乳腺癌患者們在康復之路上一定要遵醫囑,堅持科學規律的隨診隨訪、伴隨疾病的全方位管理(包括血脂管理、心臟不良反應管理、靜脈血栓栓塞癥管理、骨質疏松管理等)、和精神心理康復。這些乳腺癌全程治療的關鍵環節對于提高患者治療效果,提升患者健康水平和生活質量均有重大意義。"
中國科學院心理研究所心理咨詢師邵鈺晨女士建議:"乳腺癌患者和廣大女性朋友們都要學會關愛自己的身體和情緒,并允許自己放慢腳步,更要學會一些放松身心的有效方法,比如深呼吸、自由舞動、去到大自然中,及時釋放緊張和焦慮。"
恒瑞醫藥深刻關注中國乳腺癌領域的治療困境,圍繞未滿足的臨床需求,持續探索更多乳腺癌治療方案。此次科普活動的公益支持方江蘇恒瑞醫藥股份有限公司腫瘤事業部副總經理彭湃先生在活動總結環節中表示:"期待見證更多乳腺癌患者從真正用得上、用得起、放心用的中國創新藥中實現高質量的生存,重燃生命的希望。截至目前,恒瑞醫藥已針對乳腺癌治療研發了2款1.1類原研創新藥物吡咯替尼和達爾西利,為中國乳腺癌患者提供了更多的治療選擇。恒瑞醫藥乳腺癌領域臨床研發的產品管線布局豐富、梯隊合理,覆蓋了多種乳腺癌亞型和不同作用機制的藥物,涉及晚期二線、晚期一線、新輔助/輔助等各疾病階段適應證人群。除了研發高質量創新藥物,恒瑞醫藥已于2020年正式推出"全力去愛"患者關愛公益品牌,致力于集結全方位力量,積極探索與創新醫療服務生態伙伴的廣泛合作,力求為腫瘤患者提供全病程、全身心的患者關愛服務。值此國際乳腺癌關注月之際,恒瑞醫藥"全力去愛"公益品牌聯合上海粉紅天使癌癥病友關愛中心啟動"全力去愛-粉紅陪伴計劃",為廣大新發乳腺癌患者提供暖心陪伴福利。衷心祝福乳腺癌患友們全力去愛,重塑生命之美,活出更廣闊的人生!"
參考資料:
1. https://www.iarc.fr/faq/latest-global-cancer-data-2020
2. Hope S et al. N Eng J Med. 2014,371(2):175-176
3. Lei Fan Lancet Oncol 2014;15;e279-89
2022年8月20日,瑞維魯胺全國上市會線上線下同步舉辦,全國12個城市會場聯動。會議邀請中國科學院張旭院士、中山大學孫逸仙紀念醫院黃健教授、復旦大學附屬腫瘤醫院葉定偉教授、中國醫學科學院腫瘤醫院邢念增教授擔任大會主席,多位前列腺癌專家學者齊聚一堂,共同探討領域前沿進展,碰撞思維火花,共話瑞維魯胺廣闊治療前景。
【主席寄語,共啟新篇】
- 大會主席團致辭
會議伊始,大會主席張旭院士致開場辭。張院士指出,當今醫療界,創新與發展、交叉與融合成為主旋律,多款我國自主研發的腫瘤創新藥物上市和進入醫保,為中國腫瘤患者帶來了生命的曙光。瑞維魯胺是恒瑞醫藥自主研發的全新二代AR抑制劑,也是前列腺癌領域首個國產創新藥。瑞維魯胺的成功上市,將為中國轉移性前列腺癌患者帶來新選擇。希望恒瑞醫藥繼續開拓創新,與臨床專家攜手合作,更多參與到腫瘤治療的臨床實踐和探索中,不斷為中國腫瘤患者提供像瑞維魯胺這樣的創新藥物,為實現"健康中國2030"繼續貢獻力量。同時也期待在中國學者、中國藥企、中國患者的相互協作之下,能有越來越多的民族原研藥物問世,進一步推動我國前列腺癌診療水平更上一個臺階。
隨后,大會主席黃健教授致辭談到,我國臨床腫瘤領域的發展日新月異,泌尿腫瘤也取得了突飛猛進的成果。中國專家學者在前列腺癌領域有了更多深入的探索,中國的藥物、中國人群的研究在國際學術舞臺大放異彩,得到國際泌尿外科同道的高度認可和肯定,也為中國轉移性前列腺癌患者帶來新選擇。期待瑞維魯胺在前列腺癌領域繼續披荊斬棘,取得更多成就,也期待民族企業恒瑞立足創新,不斷突破,在泌尿腫瘤領域開發出更多優秀藥物,為更多中國患者帶來生存曙光。
大會主席葉定偉教授表示,東西方人群的差異,讓中國的轉移性前列腺癌患者的診治,存在較大的未滿足需求,臨床亟需更新更好的藥物。瑞維魯胺是全球第四款,更是中國第一款在治療mHSPC患者的三期臨床試驗中獲得陽性結果的二代AR抑制劑。在ASCO年會上,瑞維魯胺CHART三期臨床研究引起廣泛關注,顯示了國際醫學界對于該研究的關注與認可,也代表著越來越多的中國創新藥獲得國際學術界的高度肯定。瑞維魯胺的成功上市絕非偶然,是中國研究者們勇攀高峰、嘔心瀝血,是中國民族藥企肩負重任、十年磨劍的成果。瑞維魯胺的成功上市,開啟了轉移性激素敏感性前列腺癌治療的新時代。
大會主席邢念增教授表示,科學技術是第一生產力,創新是引領發展的第一動力。中國醫療衛生事業的進步和自主原研創新藥的發展,在提高我國人民健康水平的同時,也極大降低了人民群眾的醫藥衛生負擔。以恒瑞為代表的優秀民族制藥企業的崛起,自主原研創新藥物的不斷涌現,在提高中國患者診療水平的同時,也向世界展現了中國力量和中國魅力。期望中國自主研發的全新二代AR抑制劑瑞維魯胺,能夠為中國轉移性前列腺癌患者帶來更多生存獲益。我們也期望將來在泌尿腫瘤領域與民族企業強強聯合,共同研發出更多適合中國患者的優秀藥物,解決臨床未滿足需求,合力推動泌尿腫瘤學的進步。
- 恒瑞領導致辭
恒瑞醫藥總經理戴洪斌致辭表示,瑞維魯胺是恒瑞醫藥自主研發的首個中國全新二代AR抑制劑,自2012年立項至2022年6月28日正式獲批上市,前后歷經10年時間,可謂十年磨一劍的砥礪創新,凝聚了企業與臨床專家投入的巨大心血和智慧。瑞維魯胺的上市將為中國mHSPC患者帶來更具可及性和可負擔性的治療新選擇。作為創新型國際化制藥企業,恒瑞醫藥多年來立足科技創新和民生需求,重點針對中國高發腫瘤等重大疾病領域,不斷加大創新力度,致力于為臨床急需提供更多、更優的產品。在未來的發展中,恒瑞醫藥將繼續堅持自主創新,與各位專家精誠合作,為推動中國抗腫瘤事業的進步而努力,共同為促進中國醫藥創新和守護人民生命健康貢獻力量。
- 分會場主席連線致辭
全國11個城市的分會場主席也同步進行了連線致辭。四川大學華西醫院魏強教授、山東大學齊魯醫院史本康教授、湖北省腫瘤醫院魏少忠教授、安徽醫科大學第一附屬醫院梁朝朝教授、浙江大學醫學院附屬第一醫院金百冶教授、河北醫科大學第四醫院張愛莉教授、昆明醫科大學第二附屬醫院王劍松教授、河南省人民醫院丁德剛教授、南昌大學第一附屬醫院孫庭教授、中國醫科大學附屬第一醫院畢建斌教授、哈爾濱醫科大學附屬第四醫院徐萬海教授、哈爾濱醫科大學附屬腫瘤醫院陳輝教授、福建醫科大學附屬第一醫院薛學義教授、廈門大學附屬第一醫院邢金春教授等各地分會場主席分別致辭。專家高度評價了瑞維魯胺的成功上市,期待瑞維魯胺未來能繼續突破,進一步提高藥物可及性,讓更廣大的患者從治療中獲益。
【十年一劍,畢露鋒芒】
- 厚積薄發:深析瑞維魯胺藥代動力學優勢
大會學術環節,復旦大學附屬腫瘤醫院朱耀教授詳細介紹了瑞維魯胺的研發歷程與藥代動力學優勢。
- 立足臨床:瑞維魯胺CHART研究解讀
復旦大學附屬腫瘤醫院戴波教授對瑞維魯胺關鍵性III期CHART臨床研究進行了深度解讀。CHART研究是一項對比瑞維魯胺聯合雄激素剝奪療法(ADT)和標準治療聯合ADT治療高瘤負荷mHSPC患者的療效與安全性的開放性、國際多中心、III期隨機對照試驗。研究結果表明,截至2022年2月28日,接受瑞維魯胺聯合ADT治療的患者影像學無進展生存期(rPFS)與總生存期(OS)顯著改善,降低影像學進展或死亡風險54%,降低死亡風險42%。此外,在次要終點方面,相較于對照組,接受瑞維魯胺聯合ADT治療的患者客觀緩解率(ORR)、至前列腺特異性抗原(PSA)進展時間、PSA應答率和PSA未檢出率等指標均獲益明顯,且生活質量有明顯提高。安全性方面,瑞維魯胺組治療相關不良事件(TRAE)發生率與嚴重程度與對照組相似,瑞維魯胺導致包括乏力和皮疹在內的嚴重AE發生率較其他二代AR抑制劑更低,無任何級別的癲癇發生。[1]
CHART研究設計體現了對中國臨床實踐的深度思考:入組人群全部為高瘤負荷mHSPC患者,患者體力評分、Gleason評分更差,內臟轉移、骨轉移更多,治療難度更大,與其他同類研究相比,瑞維魯胺聯合ADT治療高瘤負荷mHSPC人群療效更優。CHART研究中入組的患者90%以上為中國人群,更能體現瑞維魯胺在中國患者中的療效。CHART研究對照組選擇中國臨床治療常用藥物比卡魯胺,更具有指導中國臨床實踐的價值。
基于CHART研究的出色結果,2022年6月28日,中國國家藥品監督管理局(NMPA)批準瑞維魯胺聯合ADT用于高瘤負荷mHSPC的治療。《CSCO前列腺癌診療指南(2022版)》也對瑞維魯胺治療高瘤負荷mHSPC作出了I級推薦(1A類證據)。
- 巔峰對話,致敬科學
瑞維魯胺的成功上市離不開各位研究者的貢獻,為感謝各位研究者的付出,葉定偉教授、恒瑞醫藥全球研發總裁張連山、恒瑞醫藥副總經理、首席醫學官(腫瘤)張曉靜為研究者代表進行了頒獎。
葉定偉教授和恒瑞醫藥張連山、張曉靜、馮君、金春雷、李少榮等還就瑞維魯胺的分子結構優化過程、藥代動力學優勢和臨床研發進展等進行了分享。各位研究者指出CHART三期臨床研究有著許多亮點,如:入組90%以上為中國人群,對照組為國內臨床常用的比卡魯胺,入組全部為高瘤負荷患者,試驗難度更大等。與此同時,瑞維魯胺作為高危局限性前列腺癌圍手術期治療的臨床研究、瑞維魯胺聯合多西他賽的研究也正在如火如荼的進行中。
隨后,全國12個城市會場同步進行上市啟動儀式,共同慶祝瑞維魯胺全國上市,開啟我國前列腺癌治療領域新篇章。
【揚帆起航,共創未來】
會議最后,葉定偉教授進行了大會總結。瑞維魯胺作為前列腺癌領域首個上市的中國原研二代AR抑制劑具有重大意義,為中國前列腺癌臨床實踐提供了一把利器。期待未來臨床專家與恒瑞醫藥能夠繼續攜手合作、積極進取,為提高我國前列腺癌患者5年生存率及治愈率做出更多貢獻!
參考文獻:
[1]. Ye DW, Gu W, Han W, et al: A phase 3 trial of SHR3680 versus bicalutamide in combination with androgen deprivation therapy (ADT) in patients with high-volume metastatic hormone-sensitive prostate cancer (mHSPC). J Clin Oncol 40(suppl 16; abstr 5005), 2022
第十四屆健康中國論壇榜單工作,自2021年10月7日啟動以來,歷時7個多月,分別成立了榜單顧問委員會、學術委員會、榜單工作小組等相關工作機構,制定了各榜單入選標準。依據年度創新、臨床突破、藥物惠及面、公眾關注度等維度,評選出"第十四屆健康中國論壇·年度創新榜單",恒瑞醫藥恒曲®(海曲泊帕乙醇胺片)榮列其中,體現了業界和學界對該產品及恒瑞醫藥創新研發成果的關注和認可。
恒曲®(海曲泊帕乙醇胺片)是恒瑞醫藥自主研發并擁有知識產權的1類創新藥,是中國首個自主研發的TPO-R激動劑,其研發曾獲國家"十二五"重大新藥創制科技重大專項支持。作為新一代TPO-R激動劑,恒曲®(海曲泊帕乙醇胺片)通過激活TPO-R介導的STAT和MAPK信號轉導通路,促進血小板生成,是中國血小板減少疾病的迭代藥物,目前已獲得30多項專利。2021年6月,恒曲®(海曲泊帕乙醇胺片)獲批上市,用于既往對糖皮質激素、免疫球蛋白等治療反應不佳的慢性原發免疫性血小板減少癥(ITP)成人患者的治療,以及用于對免疫抑制治療療效不佳的重型再生障礙性貧血成人患者的治療。2021年12月,恒曲®(海曲泊帕乙醇胺片)被納入國家醫保目錄,進一步提高患者用藥的可及性和可負擔性。
國內上市以來,恒曲®(海曲泊帕乙醇胺片)仍在血小板減少疾病治療領域持續探索,并積極推進在海外的臨床研究。2022年1月,恒曲®(海曲泊帕乙醇胺片)治療惡性腫瘤化療所致血小板減少癥(CIT)的III期臨床研究獲批在美國開展臨床試驗;6月中旬,其用于CIT適應癥獲得美國食品藥品監督管理局(FDA)授予的孤兒藥資格認定,臨床試驗及上市注冊的進度將加速推進。除美國外,恒曲®(海曲泊帕乙醇胺片)治療CIT的臨床研究也正在歐洲及澳大利亞開展。
作為從事創新和高品質藥品研制及推廣的國際化制藥企業,恒瑞醫藥長期堅持為患者服務的初心,聚焦未獲滿足的臨床需求大力推進創新研發。目前,公司已有11個創新藥獲批上市,另有60多個創新藥正在臨床開發,250多項臨床試驗在國內外開展,并建立起一批具有自主知識產權、國際領先的新技術平臺,為不斷產出創新成果奠定基礎。未來,恒瑞醫藥將持續實施科技創新和國際化雙輪驅動戰略,努力研制國際一流品質的好藥、新藥,為臨床急需提供更多、更優的產品,服務健康中國、造福更多患者。
研究結果顯示,卡瑞利珠單抗聯合阿帕替尼("雙艾"組合)和注射用替莫唑胺的聯合療法一線治療晚期肢端黑色素瘤的客觀緩解率達到66.7%,中位無進展生存期為18.4個月,有望為晚期肢端黑色素瘤患者帶來新的治療選擇[1]。
肢端黑色素瘤亞型在亞洲占比高 亟需探索新的治療方案
肢端黑色素瘤在歐美是一種比較罕見的黑色素瘤亞型,在所有黑色素瘤中僅占1%-7%;而在亞洲卻有很大不同,占比達到50%以上,是一種常見的黑色素瘤亞型[2、3]。
目前,晚期肢端黑色素瘤沒有標準治療方法,在歐美作為晚期皮膚型黑色素瘤標準治療的抗PD-1單克隆抗體單藥,在亞洲肢端型患者中療效卻不盡人意[4],客觀緩解率僅為14.0%-15.8%[5、6]。郭軍教授團隊前期探索了抗PD-1單抗與抗血管內皮生長因子受體藥物的組合療法,客觀緩解率能提高至22.2%[7]。在免疫治療時代,肢端黑色素瘤仍然缺乏有效的治療手段。
"雙艾"聯合注射用替莫唑胺方案 治療晚期肢端黑色素瘤取得重要突破
本次郭軍教授團隊入選2022ASCO年會口頭報告的是一項卡瑞利珠單抗聯合阿帕替尼和注射用替莫唑胺一線治療晚期肢端黑色素瘤的II期臨床試驗。旨在評價該組合療法在晚期肢端黑色素瘤中的有效性及安全性。
研究納入的主要人群為18-75歲的患有不可切除III期或轉移性的肢端黑色素瘤患者;晚期未接受過系統抗腫瘤治療;體力狀況ECOG評分0-1分;BRAF V600野生型;至少具有一個實體瘤療效評定標準1.1(RECIST 1.1)規定的可測量病灶。
研究的主要終點是客觀緩解率(ORR),次要終點包括無進展生存期(PFS)、疾病控制率(DCR)、總生存期(OS)與安全性[1]。
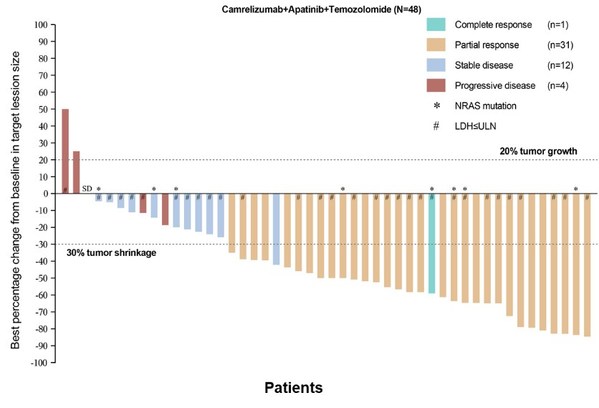
截至2022年4月10日,本研究共納入50名受試者,其中48名可評估療效。確認的ORR達到66.7%(完全緩解(CR)1人,部分緩解(PR)31人),DCR達到91.7%(圖2)。
中位至腫瘤緩解時間(time to response)為2.7個月,中位緩解持續時間(DOR)17.5個月,有11人(22.9%)在第一次影像學評估時達到了PR [1]。
中位治療持續時間為9.2個月。在研究期間,5例患者的病灶變為可切除,因此他們停止了治療并接受了手術;術后發現有1例患者達到病理緩解(pCR)。這5例患者中有4例(包括1例術前CR)仍無疾病進展,1例術后10個月疾病復發。
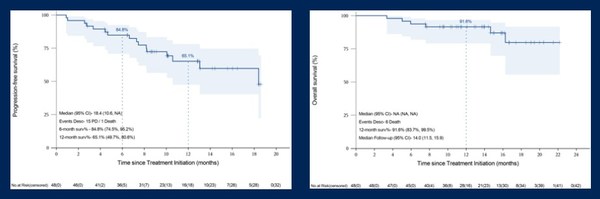
本研究中位隨訪時間為14個月,6個月PFS率為84.8%,12個月PFS率為65.1%,中位PFS為18.4個月。12個月OS率91.6%,中位OS未達到(圖3)[1]。
亞組分析發現,相較于基線時乳酸脫氫酶(LDH)升高的患者,基線時LDH正常的患者的OS有獲益趨勢;達到PR的患者有較好的PFS和OS。
卡瑞利珠單抗聯合阿帕替尼和注射用替莫唑胺的三藥聯合方案在全球屬于首創,其在一線治療晚期肢端黑色素瘤的研究取得了令人振奮的結果。66.7%的客觀緩解率超過了既往文獻報道中其他任何肢端黑色素瘤中探索的藥物組合[4],患者的無進展生存期顯著提升,安全性可控。本研究的出色數據為肢端黑色素瘤一線治療探索了新的可能,有望滿足國際社會對于肢端黑色素瘤治療方案的迫切需求。
恒瑞醫藥圍繞健康中國推進創新研發 致力惠及更多患者
值得一提的是,本研究所用的三種藥物——卡瑞利珠單抗、甲磺酸阿帕替尼、注射用替莫唑胺均為恒瑞醫藥已上市產品,對于國內的肢端黑色素瘤患者而言,有較好的藥物可及性,有望成為惠及我國肢端黑色素瘤患者的創新方案。本研究被選為2022ASCO年會的口頭報告,也體現了由中國專家開展的臨床研究和由中國藥企研發的創新藥物得到國際學界的關注與認可。
長期以來,恒瑞醫藥秉持"科技為本,為人類創造健康生活"的使命,聚焦廣大患者特別是中國患者的需求,大力推進創新研發。目前,公司已有10個創新藥獲批上市,另有60多個創新藥正在臨床開發。未來,恒瑞醫藥將持續實施科技創新和國際化雙輪驅動戰略,努力研制更多新藥、好藥,服務健康中國、惠及全球患者。
參考資料:
[1]. 2022 ASCO, Oral Abstract Session 9508
[2]. Namikawa K, et al. Curr Treat Options Oncol. 2019;20(1):7.
[3]. Desai A, et al. Clin Exp Dermatol. 2017;42(8):845-848.
[4]. Mao L, et al. Front Immunol. 2021;12:680407.
[5]. Tang B, et al. Clin Cancer Res. 2020;26(16):4250-4259.
[6]. Si L, et al. Transl Oncol. 2019;12(6):828-835.
[7]. Wang X, et al. J Clin Oncol. 2021;39(15_suppl):9539.
上海2022年6月7日 /美通社/ -- 正在舉行的2022年美國臨床腫瘤學會(ASCO)年會上,恒瑞醫藥自主研發的雄激素受體拮抗劑SHR3680(瑞維魯胺)的一項III期研究 -- CHART研究入選大會口頭報告,最新研究進展發布。研究結果顯示,SHR3680(瑞維魯胺)聯合雄激素剝奪療法(ADT)可顯著延長高瘤負荷的mHSPC患者的總生存期,并顯著降低患者疾病進展或死亡風險[1],有望為轉移性激素敏感性前列腺癌(mHSPC)患者帶來新的治療選擇。
前列腺癌高發難治 未滿足的臨床需求巨大
前列腺癌是全球范圍內男性第二常見的惡性腫瘤,也是死亡率排名第五的癌種,占全球新診斷癌癥總數的14.1%和男性癌癥死亡總數的6.8%。中國的前列腺癌發病率為15.6/10萬,且發病率呈逐年遞增趨勢[2],多數患者初診時已發生轉移,預后不佳。
前列腺癌細胞的生長具有雄激素依賴性,由于雄激素受體(AR)信號通路的持續激活,即使患者接受了去勢療法,仍不可避免地發展為去勢抵抗性前列腺癌且更容易出現轉移,而轉移性前列腺癌的五年生存率不足30%[3]。轉移性激素敏感性前列腺癌(mHSPC)以新型內分泌治療為主,二代AR拮抗劑可以有效地延緩進入轉移性去勢抵抗性前列腺癌(mCRPC)的時間,延長患者的總生存期[4]。目前,美國食品藥品監督管理局(美國FDA)已批準的二代AR拮抗劑僅三類,仍存在較大的未滿足臨床需求。
SHR3680是恒瑞醫藥自主研發的全新二代AR拮抗劑,其創新性的分子結構引入了雙羥基可提高親水性,具有更高的血漿暴露量和更低的血腦屏障透過率。I/II期研究表明,SHR3680在mCRPC患者臨床試驗的所有劑量均具有抗腫瘤活性[5]。
CHART研究數據發布 治療前列腺癌展現積極結果
CHART研究[1]是一項國際多中心、隨機、對照、開放的III期臨床試驗,由復旦大學附屬腫瘤醫院葉定偉教授牽頭進行,在全球共有72家參研中心,包括22家歐洲中心。這項研究旨在探索SHR3680聯合ADT對比比卡魯胺聯合ADT在高瘤負荷mHSPC患者中的療效和安全性。
研究入組患者為高瘤負荷的mHSPC,主要納入標準為:年齡大于等于18歲,男性,體力狀況ECOG評分0~1分;確診為高瘤負荷mHSPC,即存在4個及以上的骨轉移灶(至少一個在脊柱或骨盆以外)或內臟轉移;既往未接受過ADT、化療、手術或局部治療(以下情況除外:接受單純ADT或ADT聯合一代AR拮抗劑治療大于等于3個月;針對轉移灶導致的癥狀,在臨床研究至少4周前接受經尿道前列腺電切術或單一療程姑息性放療或手術)。患者按照1:1隨機分配接受240mg SHR3680或50mg比卡魯胺每日1次口服給藥,持續用藥直至疾病進展(包括臨床進展伴前列腺特異性抗原(PSA)進展)或不可耐受。患者同時接受促性腺激素釋放激素激動劑(GnRHa)藥物治療或既往接受過雙側睪丸切除術。
研究的主要終點是獨立評審委員會(IRC)評估的影像學無進展生存期(rPFS)和總生存期(OS);次要終點包括研究者評估的rPFS、至前列腺特異性抗原(PSA)進展時間、至下次骨相關事件(包括骨折、脊髓壓迫、針對骨骼的放療或手術)時間、至下次抗前列腺癌治療開始時間、客觀緩解率和安全性終點;探索性終點包括PSA應答率(定義為第12周末的PSA90)、PSA未檢出率和患者報告結局。
從2018年6月28日起,該研究共納入654例患者,其中SHR3680組326例,比卡魯胺組328例,兩組患者的基線特征基本相當,均衡可比,中位年齡均為69.0周歲,兩組的中國人群占比均為90%以上(90.5%vs90.2%)。
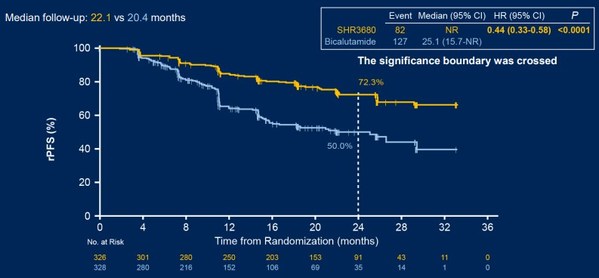
rPFS方面,截至2021年5月16日,SHR3680組與比卡魯胺組的中位隨訪時間分別為22.1與20.4個月。IRC評估的兩組24個月rPFS率分別為72.3%與50.0%,相較于比卡魯胺組,SHR3680組患者的rPFS顯著延長,發生影像學進展或死亡的風險降低了56%(圖1)。
截至2022年2月28日,IRC評估的SHR3680組與比卡魯胺組的中位rPFS數據更新,相較于比卡魯胺組,SHR3680組患者發生影像學進展或死亡的風險降低54%。
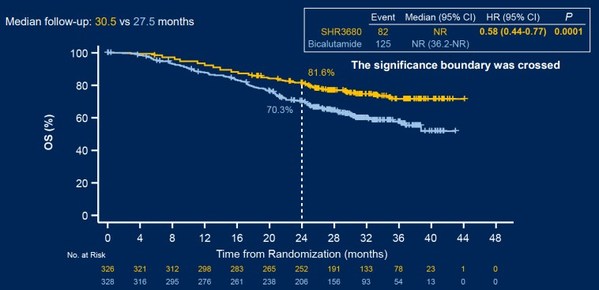
OS方面,截至2022年2月28日,SHR3680組與比卡魯胺組的中位隨訪時間分別為30.5和27.5個月,24個月OS率分別為81.6%與70.3%,SHR3680組患者的OS顯著延長,死亡風險降低了42%(圖2)。
此外,在次要終點方面,截至2022年2月28日,相較于比卡魯胺組,SHR3680組研究者評估的rPFS、至PSA進展時間、至下次骨相關事件時間、至下次抗前列腺癌治療開始時間均獲益明顯。SHR3680組的客觀緩解率為81.0%,高于比卡魯胺組13個百分點。探索性終點方面,SHR3680組的第12周末PSA90較比卡魯胺組提高15.5個百分點(94.4%vs78.9%),PSA未檢出率(PSA大于等于0.2ng/mL)較比卡魯胺組提高35.2個百分點(68.7%vs33.5%)。隨訪期間,SHR3680組前列腺癌患者生存質量測定量表(FACT-P)生存質量評分整體高于比卡魯胺組(圖3)。
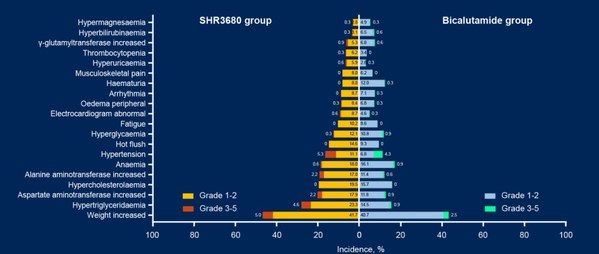
在安全性方面,SHR3680組無治療相關不良事件(TRAE)導致的死亡發生,比卡魯胺組則有1例。
CHART研究結果表明,SHR3680聯合ADT可顯著延長高瘤負荷的mHSPC患者的總生存期,并顯著降低患者疾病進展或死亡風險。與I/II期臨床試驗結果一致的是,SHR3680導致包括乏力和皮疹在內的嚴重不良反應(AE)發生率較其他二代AR拮抗劑更低,無任何級別的癲癇發生。這些令人鼓舞的結果表明,SHR3680聯合ADT有望為高瘤負荷mHSPC的治療提供新選擇。
恒瑞醫藥聚焦中國患者需求 放眼國際推進醫藥創新
值得一提的是,CHART研究納入的大部分患者為中國人群,患者體力評分、格里森(Gleason)評分更差,內臟轉移、骨轉移更多;并且本研究使用的對照藥物比卡魯胺為中國臨床廣泛用于治療mHSPC的常用藥物,更具有針對中國人群的臨床指導價值。這也是恒瑞醫藥長期以來所堅持的一個重要創新研發原則,即緊密圍繞中國患者的需求,積極推進醫藥創新研發,同時放眼國際努力為全球患者提供更多、更好的治療選擇。SHR3680的該項研究在2021年7月宣布取得陽性結果后,于同年8月被國家藥品監督管理局藥品審評中心納入突破性治療品種,用于治療高瘤負荷mHSPC,隨后其上市申請獲得優先審評資格。此外,SHR3680的另一項III期研究,即SHR3680圍手術期治療高危前列腺癌的國際多中心、隨機、對照的III期臨床研究,已于2021年9月啟動入組。期待國產創新藥SHR3680為中國晚期前列腺癌患者帶來治療新選擇。
近年來,恒瑞醫藥大力推進科技創新和國際化戰略,致力于研制更多新藥、好藥,服務健康中國、惠及全球患者。目前,公司已有10個創新藥獲批上市,另有60多個創新藥正在臨床開發。開展的國際臨床試驗近20項,其中國際多中心III期項目7項。
參考資料: |
[1]. 2022 ASCO, Oral Abstract Session 5005 |
[2]. Sung H, et al. CA: A Cancer Journal for Clinicians, 2021, 71(3):209-249 |
[3] 中國抗癌協會泌尿男生殖系腫瘤專業委員會. 2018版轉移性前列腺癌診治中國專家共識 [J] .中華外科雜志,2018,56 (9): 646-652 |
[4]. 中國臨床腫瘤學會(CSCO)前列腺癌診療指南2021版 |
[5]. Xiaojian Qin, et al. BMC Med. 2022 Mar 4;20(1):84 |
美國胸外科協會(AATS)年會是全球規模最大、學術水平最高的心胸外科領域學術會議。每年都有來自世界各地的心胸外科醫師和相關專業人士共同探討交流心胸外科領域臨床與基礎研究的新發現、新技術、新進展。本次由我國研究學者牽頭的ESPRIT研究是繼2021年美國臨床腫瘤學會(ASCO)、SITC、ESMO-IO年會之后再度入選AATS口頭報告,標志著中國研究學者和中國原研創新藥再度受到國際學術界廣泛關注與認可,有望為局部晚期食管鱗癌患者帶來更行之有效、安全可控的新輔助治療選擇。
食管癌是我國高發惡性腫瘤,每年約19 萬例患者死于食管癌[1]。食管癌術后易發生轉移,加之中晚期食管癌患者就診時間較晚,絕大多數初診時已錯過最佳手術時間,僅有20%的患者可直接接受手術治療,致使5 年生存率不足 30%[2]。因此,針對局部晚期、有潛在手術切除可能的患者,新輔助治療方案一直是臨床專家積極探索的重點。近幾年,對于局部晚期可切除的食管癌,"新輔助放化療+手術" 的治療模式已然成為被廣泛接受的標準治療,但新輔助放化療在臨床應用過程中的不良反應較為嚴重。隨著腫瘤免疫治療時代的到來,在新輔助化療的基礎上加入免疫檢查點抑制劑的治療方案已成為當前臨床研究熱點。
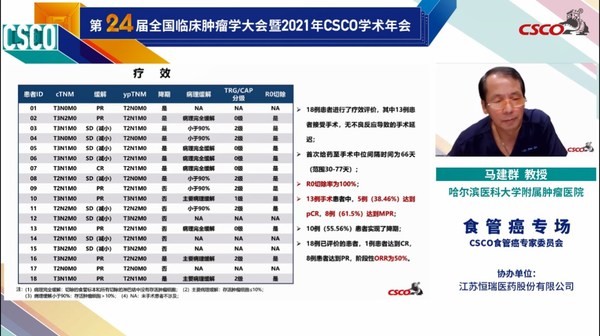
ESPRIT研究是一項關于卡瑞利珠單抗聯合紫杉醇和奈達鉑新輔助治療局部晚期食管鱗癌的單臂、前瞻性、II期臨床研究。主要研究終點是病理完全緩解率(pCR),次要研究終點是客觀緩解率(ORR)、疾病控制率(DCR)、無病生存期(DFS)、總生存期(OS)、藥物安全性等。目前,該項研究已經取得了初步結果。階段性研究數據提示,對于局部晚期可切除的食管癌患者,卡瑞利珠單抗聯合紫杉醇和奈達鉑的新輔助治療能夠縮小腫瘤并完成降期,35%患者達到病理完全緩解。安全性方面,治療藥物引起的不良反應可控,主要是中性粒細胞減少和淋巴細胞減少,所有患者均可從藥物治療中恢復,無吻合口漏且無不良反應導致的治療延遲事件發生[3]。
據ESPRIT研究主要研究者、哈爾濱醫科大學附屬腫瘤醫院馬建群教授介紹:"ESPRIT研究階段性結果給了我們極大的鼓舞,這對于延長食管癌患者生存時間,改善患者預后意義重大。基于ESPRIT研究結果,希望開展進一步的III期研究,為卡瑞利珠單抗+化療新輔助治療的臨床應用提供確鑿的證據,用中國人自己的數據來指導中國人的食管癌臨床實踐,日后讓更多中國食管癌患者從中獲益。目前該項研究正在持續招募患者中,期待這項研究能夠為食管癌新輔助治療提供一種新的治療選擇。"
ESPRIT研究是由哈醫大腫瘤醫院胸外科食管縱隔病房,牽頭開展的II期臨床研究。哈醫大腫瘤醫院胸外科創建于1972年,于2021年獲批成為 "國家臨床重點專科建設項目",胸外科食管縱隔病房于2012年成立,是國內較早成立的食管疾病亞專科,馬建群教授作為科主任,帶領科室重點開展食管、肺和縱隔腫瘤的微創治療及綜合治療,科室年手術量千余臺次,微創手術率達90%以上,手術切除率達95%。馬建群教授是國內較早提倡胸部腫瘤免疫治療的專家,科室團隊針對局部晚期食管癌和肺癌患者,經充分評估后,進行綜合治療、新輔助化療加免疫治療后再行手術,為很多中晚期患者爭取了R0手術切除機會,進一步提高了患者的治療效果。
卡瑞利珠單抗是我國民族創新藥企恒瑞醫藥自主研發并具有知識產權的人源化PD-1單克隆抗體,可與PD-1受體結合,并阻斷PD-1/PD-L1通路,激活T細胞,對腫瘤細胞產生免疫殺傷作用 [4]。目前,卡瑞利珠單抗已在中國獲批用于晚期食管鱗癌一線及二線治療。ESCORT-1st研究結果證實,卡瑞利珠單抗聯合紫杉醇和順鉑一線治療晚期食管癌可顯著延長患者中位總生存期(15.3個月 vs. 12.0個月),降低30%的死亡風險。該項研究成果已發表于國際權威醫學期刊《美國醫學會雜志》(JAMA主刊)[5]。
馬建群,主任醫師 教授 醫學博士 博士后 博士研究生導師
哈爾濱醫科大學附屬腫瘤醫院胸外科食管縱隔病房主任
中國抗癌協會縱隔腫瘤專業委員會常務委員
中國抗癌協會食管癌專業委員會常務委員
中國臨床腫瘤學會(CSCO)縱隔腫瘤專家委員會常務委員
中國臨床腫瘤學會(CSCO)食管癌專家委員會常務委員
《中國肺癌雜志》第五屆編輯委員會編委
AME出版社縱隔雜志編委
全國食管癌臨床研究中心黑龍江省分中心負責人
黑龍江省抗癌協會理事
黑龍江省食管癌診療中心負責人
黑龍江省食管癌縱隔腫瘤專科聯盟負責人
黑龍江省醫學會食管癌專業委員會主任委員
黑龍江省抗癌協會食管癌專業委員會主任委員
黑龍江省醫學會胸部腫瘤外科專業委員會副主任委員會
黑龍江省醫學會縱隔腫瘤專業委員會副主任委員
黑龍江省醫療保健國際交流促進會胸外科分會副主任委員
黑龍江省醫學會醫用機器人分會胸外科學組副組長
專家出診時間:每周六、周一上午。
參考文獻
[1] Chen W, Zheng R, Baade PD, et al. Cancer statistics in China, 2015[J]. CA Cancer J Clin, 2016, 66(2): 115-132.
[2] Malhotra GK, Yanala U, Ravipati A, et al. Global trends in esophageal cancer[J]. J Surg Oncol,2017,115(5):564-579.
[3] Ma J, Zhang J, Yang Y, et al. Camrelizumab combined with paclitaxel and nedaplatin as neoadjuvant therapy for locally advanced esophageal squamous cell carcinoma (ESPRIT): a phase II, single-arm, exploratory research. 2022 AATS, abstract 2675.
[4] Davies M. New modalities of cancer treatment for NSCLC: focus on immunotherapy[J]. Cancer management and research, 2014, 6: 63.
[5] Luo H, Lu J, Bai Y, et al. Effect of Camrelizumab vs Placebo Added to Chemotherapy on Survival and Progression-Free Survival in Patients with Advanced or Metastatic Esophageal Squamous Cell Carcinoma: The ESCORT-1st Randomized Clinical Trial. JAMA. 2021;326(10):916-925.
非小細胞肺癌(2項)
1. IV期無驅動基因非鱗NSCLC一線治療:卡瑞利珠單抗+培美曲塞+鉑類,I級推薦1A類證據
2. IV期鱗狀NSCLC一線治療:卡瑞利珠單抗+紫杉醇+卡鉑,I級推薦1A類證據(更新)
《CSCO非小細胞肺癌診療指南(2022版)》:基于III期CameL-sq研究結果,卡瑞利珠單抗已獲批一線治療鱗狀NSCLC的適應癥,因此更新"卡瑞利珠單抗+紫杉醇+卡鉑一線治療鱗狀NSCLC (I級推薦,1A類證據)"。
至此,卡瑞利珠單抗實現了在非小細胞肺癌(NSCLC)一線治療領域的全壘打,是首個在晚期非鱗癌和鱗癌一線治療III期臨床研究中取得PFS和OS雙陽性結果的中國自主研發免疫檢查點抑制劑。在非鱗非小細胞肺癌和鱗狀非小細胞肺癌一線治療中均獲I級推薦(1A類證據)。同時《CSCO免疫檢查點抑制劑臨床應用指南(2022版)》也對兩項內容進行了相應推薦。
原發性肝癌(4項)
1. 晚期原發性肝癌一線治療:卡瑞利珠單抗+阿帕替尼,I級推薦1A類證據(新增)
2. 晚期原發性肝癌一線治療:卡瑞利珠單抗+奧沙利鉑為基礎的系統化療,III級推薦2B類證據
3. 晚期原發性肝癌二線治療:卡瑞利珠單抗,I級推薦2A類證據
4. 晚期原發性肝癌二線治療:卡瑞利珠單抗+阿帕替尼,II級推薦2A類證據(更新)
《CSCO原發性肝癌診療指南(2022版)》:新增 "卡瑞利珠單抗+阿帕替尼一線治療晚期HCC(I級推薦,1A類證據)",上調"卡瑞利珠單抗+阿帕替尼二線治療晚期HCC證據等級,由2B類證據上調為2A類證據"。
截止目前,恒瑞獨有的雙艾聯合治療方式已經實現了晚期原發性肝癌一線、二線治療的全程推薦。相信未來,更優的療效,更好的藥物可及性定將為中國更多肝癌患者帶來更長生存獲益。
食管癌(5項)
1. 局部晚期食管鱗癌新輔助治療:卡瑞利珠單抗+化療,III級推薦(新增)
2. 不可切除局部晚期/復發或者轉移性食管鱗癌一線治療:卡瑞利珠單抗+紫杉醇+順鉑,I級推薦1A類證據(更新)
3. 不可切除局部晚期/復發或者轉移性食管鱗癌一線治療:卡瑞利珠單抗+阿帕替尼+紫杉醇脂質體+奈達鉑,III級推薦
4. 復發及轉移食管及食管胃交界部癌二線及以上治療:卡瑞利珠單抗,I級推薦1A類證據
5. 復發及轉移食管及食管胃交界部癌二線及以上治療:卡瑞利珠單抗+阿帕替尼,III級推薦
《CSCO食管癌診療指南(2022版)》:基于III期ESCORT-1st研究,更新"卡瑞利珠單抗+紫杉醇+順鉑一線治療不可切除局部晚期/復發或者轉移性食管鱗癌(I級推薦,1A類證據)";基于II期研究NICE研究,新增"卡瑞利珠單抗+化療新輔助治療局部晚期食管鱗癌(III級推薦)"。
這次指南的更新,對于中國患者而言也許是一次改變治療格局的變化,食管癌作為一種在我國發病率較高的癌癥,以卡瑞利珠單抗為基礎的免疫治療在接連取得晚期二線治療、一線治療的成功后,又將拓寬到可手術的食管癌患者中。此外,卡瑞利珠單抗是唯一納入國家醫保目錄的食管鱗癌治療藥物,以中國患者可及的價格,用中國人群自己的研究數據,讓更多中國食管癌患者活得更久活得更好。
鼻咽癌(2項)
1. 復發轉移性鼻咽癌一線治療:卡瑞利珠單抗+順鉑+吉西他濱,I級推薦1A類證據
2. 復發轉移性鼻咽癌二線或挽救治療:卡瑞利珠單抗,II級推薦2B類證據
在鼻咽癌治療領域,《CSCO鼻咽癌診療指南(2021版)》針對復發/轉移性鼻咽癌卡瑞利珠單抗聯合/單藥治療已經進行了一線、二線及以上、三線及以上治療的全線推薦。本次《免疫檢查點抑制劑臨床應用指南(2022版)》又進行了指南推薦新增和推薦級別的更新。同時,雙艾(卡瑞利珠單抗聯合阿帕替尼)研究數據也將亮相美國臨床腫瘤學會(ASCO)年會。期待卡瑞利珠單抗能給更多的鼻咽癌患者提供有效的治療方案,帶來長期生存的希望。
淋巴瘤(4項)
1. 符合移植條件的復發/難治性經典霍奇金淋巴瘤二線及以上治療:卡瑞利珠單抗,II級推薦3類證據;卡瑞利珠單抗+地西他濱,III級推薦3類證據
2. 不符合移植條件的復發/難治性經典霍奇金淋巴瘤二線及以上治療:卡瑞利珠單抗,I級推薦2B類證據(更新)
3. 不符合移植條件的復發/難治性經典霍奇金淋巴瘤二線及以上治療:卡瑞利珠單抗+地西他濱,III級推薦3類證據
4. 原發縱隔大B細胞淋巴瘤二線及以上治療:卡瑞利珠單抗+GVD,III級推薦2B類證據(新增)
《免疫檢查點抑制劑臨床應用指南(2022版)》,基于卡瑞利珠單抗聯合GVD化療治療復發難治性原發縱膈大B細胞淋巴瘤的I//II期臨床研究,新增"卡瑞利珠單抗+GVD二線及以上治療原發縱隔大B細胞淋巴瘤(III級推薦2B類證據)"。《CSCO淋巴瘤診療指南(2022版)》,基于卡瑞利珠單抗單藥治療R/R cHL的II期注冊研究長期隨訪結果,"不符合移植條件的復發難治性經典型霍奇金淋巴瘤患者卡瑞利珠單抗由II級推薦提升為I級推薦"。
黑色素瘤(1項)
- 一線治療晚期肢端黑色素瘤(無腦轉移):卡瑞利珠單抗+阿帕替尼,III級推薦2B類證據
2021年ASCO大會上公布了卡瑞利珠單抗+阿帕替尼在晚期肢端黑色素瘤II期研究數據,基于此數據卡瑞利珠單抗+阿帕替尼被CSCO指南推薦為:晚期肢端黑色素瘤(無腦轉移)一線治療III級推薦、2B類證據。在黑色素瘤領域卡瑞利珠單抗聯合治療方案有多個研究在進行,期望未來產生更多中國原創數據惠及中國黑色素瘤患者。
膽道腫瘤(1項)
1. 一線治療晚期膽道腫瘤:卡瑞利珠單抗+GEMOX,II級推薦2B類證據
卡瑞利珠單抗聯合GEMOX對膽道癌癥患者有較好的療效,不良反應可耐受。希望未來更多的膽道腫瘤患者可以從該方案中獲益。
]]>上海2022年4月15日 /美通社/ -- 4月15日至21日是"第28屆全國腫瘤防治宣傳周"。今年宣傳周的主題為"整合資源 科學防癌"。活動響應《"健康中國2030"規劃綱要》要求,聚焦"防篩診治康"全程管理,開展形式多樣的癌癥防治宣傳教育,助力實現對癌癥的有效防控。
恒瑞醫藥作為民族制藥代表性企業,在抗腫瘤藥物研發生產方面有著悠久歷史和豐富經驗,同時也長期積極支持腫瘤防治科普等公益事業。今年全國腫瘤防治宣傳周,恒瑞醫藥"全力去愛"患者關愛品牌廣泛聯合中國抗癌協會科普專委會、中國抗癌協會肝癌專業委員會、北京癌癥防治學會、主流媒體等各方力量,在乳腺癌、肺癌、肝癌、食管癌、卵巢癌、鼻咽癌等中國高發癌癥領域開展了形式多樣的患者教育、線上義診和系列公眾疾病認知教育活動,助力提升公眾及腫瘤患者對腫瘤防治核心知識知曉率,普及科學防癌理念,倡導健康生活方式,提升患者自我健康管理能力。
關注未滿足需求 為肺癌患者科普PD-1核心用藥知識
以PD-1單抗為代表的免疫檢查點抑制劑作為目前腫瘤治療領域的熱點,臨床應用已逐漸普及。在肺癌領域,越來越多的患者從免疫治療中獲益。其中,恒瑞醫藥自主研發的PD-1抑制劑卡瑞利珠單抗已在肺癌、肝癌、食管癌、鼻咽癌以及淋巴瘤五大瘤種中獲批8個適應癥,是目前獲批適應癥數量最多、覆蓋瘤種最廣的國產PD-1產品之一。同時,隨著卡瑞利珠單抗等中國自主研發PD-1單抗進入國家醫保目錄,肺癌患者的治療負擔進一步降低,PD-1在臨床的廣泛應用進一步加速。
然而,PD-1用藥患者在日常診療過程中接受到的治療指導處于碎片化狀態。為了加快免疫治療科普知識的普及,提升醫患溝通效率,切實推動PD-1規范治療,《中國抗癌協會肺癌患者PD-1用藥科普指南》編寫項目已于去年全國腫瘤防治宣傳周期間啟動,旨在為廣大公眾和肺癌患者提供全面、系統、權威、實用、動態更新的PD-1用藥科普。編寫工作集結了肺癌領域31位資深臨床專家、藥學專家、護理學專家共同參與,歷時200余天,凝聚多學科領域的智慧與經驗,于2021年12月完成指南編寫并發布,全文共7大章節35小節。
今年,由中國抗癌協會指導、中國抗癌協會科普專業委員會牽頭開展、恒瑞醫藥"全力去愛"患者關愛公益品牌支持的指南解讀系列工作將陸續開展。
4月13日,《中國抗癌協會肺癌患者PD-1用藥科普指南》全國首場解讀會在線上順利召開。國家健康科普專家、中國抗癌協會科普部部長、首都醫科大學肺癌診療中心主任、《中國抗癌協會肺癌患者PD-1用藥科普指南》主編支修益教授做核心知識解讀。 中國抗癌協會科普平臺、央視頻、今日頭條、百度、微博、新浪愛問、微視、健康界、醫悅匯、醫呼益吸、樂問醫學、覓健、全力去愛、為ai共免等多平臺同步直播,在線觀看人數達到近100000人次。
食管癌科普義診活動 推動實現食管癌"三級預防"
食管癌是我國的高發惡性腫瘤之一。對于晚期食管鱗癌患者,傳統一線標準治療是雙藥化療,但是單純化療療效欠佳,免疫治療為食管癌治療帶來新的突破。基于ESCORT-1st研究的積極結果,卡瑞利珠單抗食管鱗癌一線治療適應癥于2021年獲批。癌癥防治,重在"關口前移"。為了讓更多的食管癌患者早期診斷、及時治療,盡可能實現食管癌的"三級預防",由恒瑞醫藥"全力去愛"患者關愛公益品牌支持、北京癌癥防治學會特別發起的"食管癌防治科普義診‘百城行動'科普義診活動于4月12日-15日開展。北京大學腫瘤醫院沈琳教授和魯智豪教授分別作為項目主席和執行主席,攜手北京大學腫瘤醫院柯楊教授、北京大學腫瘤醫院陳克能教授、中國醫學科學院腫瘤醫院肖澤芬教授等三位食管癌領域權威專家,聚焦食管癌發病原因、早期篩查和預防、早期癥狀和就診方式、規范診療等方面進行線上科普,百余位食管癌專家進行線上、線下義診,為公眾帶來權威科學的食管癌科普知識,幫助食管癌患者全程規范管理疾病。
規范患教義診 助力肝癌患者長期生存
原發性肝癌是目前我國常見惡性腫瘤,嚴重威脅國人生命健康。目前,原發性肝癌5年生存率偏低,規范化診療需加速步伐。2020年,恒瑞醫藥自主研發的2個創新藥卡瑞利珠單抗(艾瑞卡®)聯合抗血管生成靶向藥物阿帕替尼(艾坦®)的"雙艾"方案進入國家肝癌診療規范,為中國肝癌規范化治療提供新的選擇。
為大力推動中國肝癌診療規范化進程,并進一步提升我國肝癌早診率,全面提高肝癌患者5年生存率,中國肝癌規范行動——CNLC規范患教項目在國家衛生健康委員會領導下、全國肝病多學科診療專家指導下應運而生。該患者教育項目旨在通過患教會以及線上直播學習的形式,結合醫生、護士、患者組織等多方力量,從最新藥物診療進展、科學家庭隨訪、術前術后管理、心理精神疏導、患者個體化答疑等各方面進行系統性教育,幫助患者通過多種途徑獲得權威專業的疾病知識,了解和管理自身疾病進程,有效提升患者生活質量。
在今年的腫瘤防治宣傳周期間,由恒瑞醫藥"全力去愛"患者關愛公益品牌支持的中國肝癌規范行動 -- CNLC規范患教義診活動將于4月20日在線上舉行。中國科學院院士、復旦大學附屬中山醫院院長、上海市肝病研究所所長樊嘉,復旦大學附屬中山醫院副院長、上海市徐匯區中心醫院院長、復旦大學附屬中山醫院肝臟外科主任、復旦大學肝癌研究所常務副所長周儉分別作為會議主席和執行主席為義診活動致辭。來自復旦大學附屬中山醫院的多名肝癌治療領域臨床專家為患者線上答疑,傳遞肝癌早篩早診核心知識要點,同時為上海疫情期間的肝癌患者居家照護和線上隨訪配藥提供全面的悉心指導。
系列公益科普行動 提升公眾科學防癌意識
此外,今年的腫瘤防治宣傳周期間,恒瑞醫藥還將結合當前我國腫瘤治療實踐的現狀,進一步拓展科普宣傳和公益活動范圍。鑒于腫瘤治療相關性血小板減少癥(CTRT)是腫瘤治療中常見的不良反應,往往影響患者的治療進程及完成度,導致患者腫瘤治療獲益降低,因此CTRT的防治也是腫瘤防治中重要的一部分。為提升臨床醫生對CTRT管理的重視,推動CTRT防治的規范化,恒瑞醫藥在全國多個城市支持開展血小板減少管理先鋒論壇,邀請業內權威專家學者就血小板減少癥的管理進行深入探討和科學普及。同時聯合多名臨床專家,分享解析典型案例,提升公眾和患者對CTRT管理的認知,助力新的治療方案的推廣和應用。這方面,恒瑞醫藥自主研發的海曲泊帕乙醇胺片是目前國內唯一獲批免疫性血小板減少癥(ITP)和再生障礙性貧血(SAA)雙適應癥的促血小板生成素受體激動劑。
恒瑞醫藥多年來深耕腫瘤治療領域,聚焦中國高發癌種,洞悉未滿足的臨床治療需求,致力于為患者研發覆蓋多瘤種的創新治療藥物。公司目前已上市的10個創新藥中,超過一半是抗腫瘤藥物,且絕大多數都已納入國家醫保目錄。
恒瑞醫藥還積極投身癌癥防治科普事業。自2020年創立"全力去愛"患者關愛公益品牌以來,依托自身在抗腫瘤治療領域的科研優勢與專長,廣泛集結各方力量,共同推動腫瘤防治科普事業發展,助力提高癌癥患者5年生存率和治愈率。
在今年的腫瘤防治宣傳周期間,恒瑞醫藥全力去愛患者關愛品牌圍繞乳腺癌、肺癌、肝癌、食管癌、胃癌、卵巢癌、鼻咽癌等中國高發癌種,通過創意科普短視頻、裂變傳播H5等多元化形式,倡導每個人都要做好自己的"健康第一責任人",傳遞生動科學的健康科普知識,并邀請公眾、員工、合作伙伴、媒體等多方共同參與公益科普行動,同時開展疾病認知調研,了解公眾對腫瘤防治核心知識要點的知曉現狀,提升公眾科學防癌意識。
當下國家高度重視抗癌工作,部署加強癌癥預防篩查、早診早治工作,提出2030年實現全人群、全生命周期的慢性病健康管理,總體癌癥5年生存率提高15%的目標。為積極響應健康中國國家戰略的號召,幫助群眾獲得更專業、科學和系統性的醫療知識,去年4月,中國臨床腫瘤學會(CSCO)與中國醫學論壇報社(CMT)聯合啟動了“關愛行動 -- 腫瘤患者教育大型公益項目”。項目一期在江蘇恒瑞醫藥股份有限公司“全力去愛”患者關愛公益品牌支持下全面開展肺癌、肝癌、食管癌等疾病的科普教育活動,以助力推動我國腫瘤患者的全流程健康管理,加強患者所關注的腫瘤預防和篩查、疾病科普、診療規范、藥物應用、情緒/心態調整等科普知識。
本次關愛行動肝癌專家組成員共同編寫的肝癌患者教育手冊分為6個章節(以下簡稱“手冊”),分別從認識肝癌、篩查、如何就診并建立檔案、診斷和治療、肝癌疾病名詞解釋進行了介紹。手冊首先為大家介紹了肝癌的基礎知識,幫助患者及家屬認識肝癌的危險因素和篩查手段,了解肝癌的癥狀和預后。手冊更加注重實用性,細心為患者介紹了選擇就診醫院和科室時的注意事項,以及怎樣建立診療檔案,應該做哪些檢查,就診時應該和醫生溝通哪些關鍵問題等,幫助患者在面對肝癌時不至于手足無措。此外,手冊根據肝癌的分期和分型,詳細介紹了不同階段的治療目標、臨床決策因素、治療方式選擇、不良反應監測、隨訪檢查方法和營養康復要點等幫助患者“知己知彼”,更加充滿信心地迎戰肝癌。
手冊后續編排出版時,將適當運用圖表、插圖和患者故事,做到通俗易懂,幫助患者接受和理解醫生是如何選擇治療方案,提高醫患溝通效率,助力醫患同心,守護肝癌患者生命線。
大會主席、肝癌專家組組長致辭
黎功教授作為本次活動的主席及“關愛行動”的肝癌專家組組長,在活動致辭中表示,《肝癌患者教育手冊》在肝癌行動組全體成員的共同努力下,歷時數月的組稿和多方的審校修訂終于完成撰寫工作。該手冊為腫瘤領域的醫生和患者提供了專業、權威、全面的科學抗癌知識,幫助患者及家屬能夠以科學、積極的心態接受和配合臨床多學科規范化的綜合治療。相信隨著關愛行動的深入開展,可以進一步提高患者對肝癌的科學認識,為患者帶來更多信心。
關注肝癌癥狀,早診早治提高肝癌患者生存率
高杰教授介紹,在中國,乙肝病毒感染、酒精性肝病、脂肪肝或脂肪性肝病和食物毒素是最重要的致病因素。在患者疑似肝癌的情況下,醫生會結合高危因素、影像學特征以及血清學分子標志物對肝癌做出臨床診斷。高杰教授還為患者介紹了中國肝癌分期方案(CNLC),對不同分期的患者可選擇的不同治療策略。肝癌治療手段分為局部治療和全身治療,局部治療有根治性切除、消融治療、肝動脈化療栓塞術(TACE)和放療,全身治療包括化療、靶向治療和免疫治療。靶向藥物和免疫抑制劑聯合應用近來獲得突破療效,具有臨床應用前景,如阿帕替尼聯合卡瑞利珠單抗等免靶聯合方案已獲2020版《中國臨床腫瘤學會(CSCO)原發性肝癌診療指南》一線治療推薦。
早期肝癌手術治療是首選,綜合患者情況制定個體化方案
李廣欣博士介紹了早期肝癌的治療現狀。早期肝癌的治療目標在于完整移除腫瘤的同時,保護剩余肝臟的功能。因此醫生在選擇治療方案時需要考慮患者的肝功能儲備、是否存在肝硬化門脈高壓等情況,制定個體化治療方案。
同時對于部分需要手術的患者也應當遵循兩大原則:徹底性,指是否能完整切除腫瘤,切緣無殘留腫瘤;安全性,即是否保留足夠的肝臟組織能夠代償發揮功能,以降低手術并發癥發生率及死亡率,從而最大化患者的治療獲益。
綜合應用多學科診療,為中晚期肝癌患者選擇最佳治療方案
韓玥教授介紹了局部晚期或轉移性肝癌的治療現狀。Ⅲ期肝癌患者的治療目標是最大限度地控制腫瘤進展,延長生存時間,改善患者的生活質量。臨床上,需要綜合應用局部治療與系統治療,因此多學科診療(MDT)模式具有重要意義。韓教授指出,免疫聯合靶向治療成為肝癌治療的新模式,以國內原研創新藥的RESCUE研究為例,卡瑞利珠單抗聯合阿帕替尼組的客觀緩解率高達46%,中位總生存期達20.1個月,被2020版《CSCO原發性肝癌治療指南》推薦用于晚期肝細胞癌的一線治療。
Ⅳ期肝癌治療的首要目標是提高患者生活質量,延長生存時間。治療策略選擇包括最佳支持治療與姑息治療(舒緩療護)、肝移植、中醫藥治療。晚期肝癌患者容易出現營養不良,患者應遵循合理的飲食原則。
在本次活動中,崔玖潔教授、盛立軍教授、王文濤教授、梁雪峰教授、薛軍教授和周軍教授針對線上患者及家屬的提問,進行了悉心的解答。線上提問的觀眾反響熱烈,對各位專家專業且耐心的解答表示衷心地感謝。
黎功教授在活動總結時表示,《肝癌患者教育手冊》在專家組成員的共同努力下即將問世,希望手冊正式出版能盡快與患者們見面。此次手冊定稿暨巡講首場啟動會將成為良好的開端,日后也將繼續開展一系列患教活動,促進醫患間良好的交流,為群眾提供更專業的腫瘤防治知識,助力提升中國肝癌診療水平。
活動于2月25日線上同步直播,收獲超2.6萬人次觀看,患者及家屬在線上與專家積極互動,對各位專家的講解和公益關愛表示由衷的感謝。
CSCO-CMT關愛行動患教公益項目將繼續秉承“以愛為銘,規范前行”的理念,積極開展各項患教活動和醫學科普,為患者撐起一把傘,點亮一盞燈。本次活動是CSCO-CMT關愛行動肝癌專家行動組的首場全國巡講,后續巡講和形式多樣的患者關愛活動也將陸續開展,為廣大患者們帶來更科學的抗癌知識和指導,帶領患者們更好地認識肝癌、抗擊肝癌,與患者一起共筑健康長城。
中國醫學科學院腫瘤醫院徐兵河院士、解放軍總醫院江澤飛教授、江蘇省人民醫院殷詠梅教授、中國科學院大學附屬腫瘤醫院王曉稼教授、中山大學孫逸仙紀念醫院劉強教授、中山大學腫瘤防治中心王樹森教授、中國醫學科學院腫瘤醫院馬飛教授、中國醫學科學院腫瘤醫院張頻教授以及上北廣三地主持人復旦大學附屬腫瘤醫院余科達教授、中國醫學科學院腫瘤醫院李俏教授、廣東省中醫院陳前軍教授等專家在主會場出席。
哈爾濱醫科大學附屬腫瘤醫院張清媛教授、河北醫科大學第四醫院耿翠芝教授、江蘇省腫瘤醫院馮繼鋒教授、中國醫科大學附屬第一醫院金鋒教授、中國醫科大學附屬第一醫院滕月娥教授、天津醫科大學腫瘤醫院佟仲生教授、河南省腫瘤醫院劉真真教授、湖南省腫瘤醫院歐陽取長教授、中南大學湘雅二醫院陳干農教授、空軍軍醫大學西京醫院凌瑞教授、青島大學附屬醫院王海波教授和四川大學華西醫院羅婷教授等專家在分會場出席。復旦大學附屬腫瘤醫院邵志敏教授、吳炅教授、胡夕春教授視頻寄語參會。
業內知名學者和全國各地的乳腺癌專家通過線下線上的形式齊聚盛會,見證恒瑞醫藥自主研發的CDK4/6抑制劑達爾西利上市,共話乳腺癌治療新局面,共謀乳腺癌治療新未來。
此次上市會以達爾西利的“孕育-萌芽-誕生-成長-陪伴”為邏輯線,講述了CDK4/6抑制劑達爾西利立項、研發及上市歷程,呈現了恒瑞醫藥在乳腺癌領域的戰略布局,展現出恒瑞醫藥立足中國、走向世界的行業擔當。
十年磨一劍,聚焦患者需求推進研發
會議伊始,通過曙光初現短劇,回顧了恒瑞醫藥副總經理張連山帶領的研發團隊對于達爾西利的立項初心。“頭道水,二道茶,三道四道是精華”,體現了恒瑞達爾西利會迎頭趕上,有信心、有決心成為最適合中國患者的“中國達案”之一。
復旦大學附屬腫瘤醫院余科達教授、中國醫學科學院腫瘤醫院李俏教授和廣東省中醫院陳前軍教授介紹全國多個分會場的專家同道,大家共襄榮耀盛會,熱烈祝賀達爾西利的成功上市。
隨后,恒瑞醫藥常務副總經理戴洪斌致辭指出,達爾西利為恒瑞醫藥又一個十年磨一劍的成果。從2013年立項到2021年上市,達爾西利的研發之路經歷了眾多挑戰,其成功為中國醫生和患者提供了更多的治療選擇。達爾西利對激素受體陽性(HR+)、人表皮生長因子受體2陰性(HER2-)乳腺癌的晚期解救治療和早期輔助治療等相關臨床研究正有條不紊地推進,在HER2+乳腺癌、三陰性乳腺癌領域,恒瑞醫藥的眾多產品也正在布局,相信將為臨床提供更多更好的服務。
回顧探索之路,分享心路歷程
大會還回溯了達爾西利從2013年到2021年的八年探索歷程。恒瑞醫藥研發中心副總經理李心和高級醫學總監朱曉宇講述了與達爾西利一路走來的心路歷程,分享了遇到困難和挑戰時的彷徨、研究取得成效時的激動人心、成功上市時的喜悅和欣慰等刻骨銘心的時刻。
100%中國循證,更貼近中國患者
達爾西利的III期臨床注冊研究(DAWNA-1研究)于2021年榮登國際頂級期刊《自然· 醫學》(Nature Medicine,影響因子:53.44)。上市會上,研究主PI徐兵河院士全面深入解讀了DAWNA-1研究。
徐兵河院士特別指出,DAWNA-1研究入組患者100%為中國人群,達爾西利研究組27%患者既往解救治療中接受過化療,44%絕經前(圍絕經期)患者,貼近中國乳腺癌診療現狀。
隨后,中國醫學科學院腫瘤醫院馬飛教授、復旦大學附屬腫瘤醫院胡夕春教授、中國科學院大學附屬腫瘤醫院王曉稼教授、中國醫學科學院腫瘤醫院張頻教授及中國醫科大學附屬第一醫院金鋒教授、天津市腫瘤醫院佟仲生教授、中山大學附屬腫瘤防治中心王樹森教授結合乳腺癌臨床實踐展開精彩對話,闡述了中國HR+晚期乳腺癌患者與西方的差異,剖析了DAWNA-1研究立足中國人群的巨大意義,一致對達爾西利給予了積極評價。
揚帆遠航,努力惠及更多患者
在逐浪未來短劇中,彰顯了恒瑞人希望攜手中國臨床醫生從夯實中國規范出發,開拓國際市場的雄心。
會上,解放軍總醫院江澤飛教授、江蘇省人民醫院殷詠梅教授、復旦大學附屬腫瘤醫院吳炅教授、復旦大學附屬腫瘤醫院邵志敏教授及哈爾濱醫科大學附屬腫瘤醫院張清媛教授、中山大學孫逸仙紀念醫院劉強教授、河北醫科大學第四醫院耿翠芝教授共同探討了醫療實踐、臨床研究、中國企業走向國際的未來發展之路。
江澤飛教授和張清媛教授表示,在國家各種政策的加持下,隨著藥物的良好準入、指南的推動、規范診療的巡講等,國內區域發展的不平衡將會越來越小,越來越多的醫生和患者能夠“想得到、用得起、用得好”創新藥物,全國的醫療水平也會獲得整體的提升。
對于民族藥企的國際化道路,江澤飛教授指出,對于國際化應該有更加開闊的路,國際上下不同區域、不同時段的醫療需求并不一樣。立足中國,放眼世界,不墨守成規,是破局的又一思路,同時他也寄語恒瑞的國際化越走越寬。
劉強教授表示,在大浪淘沙的時代,恒瑞醫藥應牢記初心,選定正確的賽道,建立自己的標準,為中國更為世界做出貢獻。耿翠芝教授為基層醫生發聲,提出了原研藥物通過進入國家醫保能惠及更多患者的愿望。殷詠梅教授和邵志敏教授指出,科研或醫療機構與醫藥企業進一步的深入合作可助力中國醫療健康事業發展,推進中國智慧的國際化道路。吳炅教授展望未來,期待更多民族企業能夠聚焦新的靶點、研發新的藥物,為癌癥患者帶來長期生存和提高生活質量的希望。
達爾西利全國上市會在激動人心的上市儀式環節中推向高潮,各會場的眾多專家共同為達爾西利的上市注入能量,與會嘉賓線上線下共同見證了達爾西利上市的榮耀時刻,正式開啟中國“達”案。
中國醫學科學院腫瘤醫院徐兵河院士總結道,目前達爾西利為全球第四個上市的CDK4/6抑制劑,希望上市后造福更多患者。
孕育,萌芽,誕生,成長,陪伴,這就像貫穿在每個人生命中的必然階段,2月26日達爾西利全國上市會在13個全國會場,線上線下數萬人的關注下圓滿落幕。然而,這一份中國“達”案才剛剛開啟,希望未來它能更成熟,書寫更多“中國達案”。
2022年2月19日,“云程發軔·氟來居上”氟唑帕利醫保上市會在青島線下盛大召開,且通過線上形式,主會場青島與北京、河南、安徽、湖北、貴州、廣東和重慶7個分會場實時聯動。中國工程院院士、華中科技大學同濟醫學院附屬同濟醫院馬丁院士,山東大學齊魯醫院孔北華教授,中山大學腫瘤防治中心劉繼紅教授,中國醫學科學院腫瘤醫院吳令英教授,復旦大學附屬腫瘤醫院吳小華教授和重慶大學附屬腫瘤醫院周琦教授等業內知名專家學者和全國各地的婦瘤專家出席會議,共話中國卵巢癌靶向治療新局面。
會上各位專家就中國卵巢癌所面臨的挑戰,氟唑帕利的研究布局和最新研究進展進行了討論。各位專家一致認為,氟唑帕利進入醫保將會為卵巢癌的治療提供更多的選擇空間,進一步降低患者的經濟負擔。對于氟唑帕利創新性引入三氟甲基,各位專家也展開了深入討論,這一結構增加了藥物的結構穩定性和脂溶性,使得藥物體內活性更高,血藥濃度更均一,個體間變異更小。對氟唑帕利的療效和安全性,氟唑帕利FZOCUS系列臨床研究的主要研究者(Leading PI)吳令英教授在報告中指出,氟唑帕利療效與同類PARP抑制劑相當,且因相關不良事件(TRAE)導致的終止治療率更低,耐受性更好。
恒瑞醫藥副總經理戴洪斌代表恒瑞醫藥致辭,他指出,恒瑞醫藥在腫瘤治療領域進行了豐富的研發布局。氟唑帕利是中國首個自主原研的PARP抑制劑,也是恒瑞研發上市的第七個創新藥。基于出色的臨床數據,氟唑帕利以非常惠民的價格被納入新版國家醫保目錄。目前氟唑帕利的多項國際多中心臨床研究正在有條不紊地推進,相信氟唑帕利未來不僅能夠更好造福中國患者,還有望進入歐美市場,推動民族醫藥創新走向世界。
會議落下了帷幕,但為中國卵巢癌患者造福的努力卻從未停止。氟唑帕利獲批上市及納入醫保,更好地滿足了患者的需求,給患者帶來優質優價選擇的同時,也帶來了更好的生活質量。未來,在產學研醫共同努力下,希望出現更多氟唑帕利這樣的民族創新藥,為卵巢癌等各瘤種患者提供更多治療方案,帶來更好生存獲益。
本研究是首個在全部入組人群均為HER2陽性乳腺癌腦轉移患者中報道吡咯替尼聯合卡培他濱療效和安全性的前瞻性研究,也是首個在中國患者中根據乳腺癌腦轉移既往局部治療情況,劃分為兩個獨立隊列進行分析和比較的前瞻性臨床研究,為臨床上乳腺癌腦轉移治療和個體化決策帶來新的啟示。
在曲妥珠單抗為基礎治療的時代,仍有大約30%-50%的人表皮生長因子受體2(HER2)陽性轉移性乳腺癌患者會發生腦轉移[2-5],導致預后不佳。目前腦轉移的治療以局部治療手段為主,包括手術切除、立體定向放療和全腦放療。然而,局部治療后6-12月內復發率仍然較高,且會帶來認知功能下降等不良反應[6],給臨床治療帶來巨大挑戰。
PERMEATE研究是一項在全國8家中心開展的多中心、單臂、雙隊列、Ⅱ期臨床研究,旨在研究吡咯替尼聯合卡培他濱治療HER2陽性乳腺癌腦轉移的有效性及安全性。PERMEATE研究主要研究者閆敏教授表示:“我國乳腺癌治療必須依照本國人群疾病發展特征和臨床診療現狀才能指導臨床實踐。這也是發起我國自主研發創新藥吡咯替尼聯合卡培他濱治療HER2陽性乳腺癌腦轉移II期臨床研究的最重要的意義所在。研究結果提示,對于HER2陽性乳腺癌腦轉移,吡咯替尼聯合卡培他濱方案對顱內和顱外病灶均能有效控制,尤其是對于既往未接受顱腦局部放療的患者。吡咯替尼有望成為中國HER2陽性腦轉移人群的優選治療方案,同時有望為需要推遲局部治療的患者提供了系統治療的選擇。”
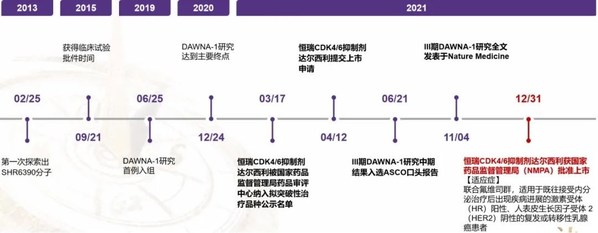
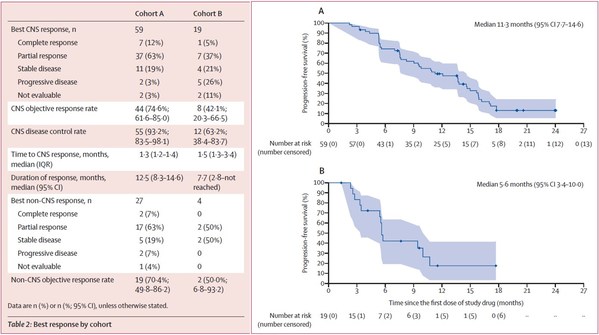
PERMEATA研究于2019年1月開始,共入組78例有顱內可測量病灶的HER2陽性乳腺癌腦轉移患者,其中69例既往接收過曲妥珠單抗的治療。根據患者中樞神經系統病灶既往局部治療情況,分為——隊列A:未經局部放療的腦轉移患者(N=59);隊列B:局部放療后再次進展的腦轉移患者(N=19)。均接受吡咯替尼(400 mg,qd,po)聯合卡培他濱(1000mg/m2, bid,po,d1-14,q3w)治療。主要研究終點為中樞神經系統病灶客觀緩解率(CNS ORR)。結果顯示隊列A的中樞神經系統病灶客觀緩解率(CNS ORR)高達74.6%(95%CI:61.6~85.0),其中有7例(11.9%)患者達到完全緩解(CR)。隊列B的中樞神經系統病灶客觀緩解率(CNS ORR)為42.1%(95%CI:20.3~66.5)。次要終點結果顯示,在31例同時伴有顱外可測量病灶的患者中,兩個隊列非中樞神經系統病灶客觀緩解率(Non-CNS ORR)分別為70.4%和50%。中位隨訪15.7個月,隊列A和隊列B的中位無疾病進展生存期(PFS)分別為11.3個月(95% CI:7.7~14.6)和5.6個月(95% CI:3.4~10.0)[1]。安全性方面,腹瀉和手足綜合征是最常見的不良事件,總體可耐受和控制。
PERMEATA研究在2020年歐洲內科腫瘤學會(ESMO)會議和2021年美國臨床腫瘤學會(ASCO)年會上獲得壁報展示,獲得國內外專家的廣泛關注。如今,該臨床研究成果榮登國際權威學術期刊《柳葉刀.腫瘤學》,展現了國際學界的肯定。
吡咯替尼是恒瑞醫藥自主研發且具有知識產權的口服表皮生長因子受體(EGFR)/人表皮生長因子受體2(HER2)/人表皮生長因子受體4(HER4)酪氨酸激酶抑制劑,是中國首個原研EGFR/HER2/HER4靶向藥物。2018年,吡咯替尼憑借II期臨床研究數據獲國家藥監局(NMPA)附條件批準上市,是實體瘤領域中國首個憑借II期臨床研究獲附條件批準上市的創新藥。2019年,吡咯替尼被納入國家醫保,大大提升可及性和可負擔性。2020年,吡咯替尼憑借兩項重要III期研究(PHENIX、PHOEBE)結果獲得國家藥監局完全批準上市。目前,吡咯替尼還在進行涵蓋乳腺癌、肺癌、膽道癌等多個瘤種的多項臨床研究,持續探索不同疾病不同階段的治療方案,造福更多中國病患。
參考文獻: |
[1] Yan M, Ouyang Q, Sun T, et al. Pyrotinib plus capecitabine for patients with human epidermal growth factor receptor 2-positive breast cancer and brain metastases (PERMEATE): a multicentre, single-arm, two-cohort,phase 2 trial. Lancet Oncol 2022; published online Jan 24. https://doi.org/10.1016/S1470-2045(21)00716-6. |
[2] Bendell JC, Domchek SM, Burstein HJ, et al. Central nervous system metastases in women who receive trastuzumab-based therapy for metastatic breast carcinoma. Cancer. 2003. 97(12): 2972-7. |
[3] Gori S, Rimondini S, De Angelis V, et al. Central nervous system metastases in HER-2 positive metastatic breast cancer patients treated with trastuzumab: incidence, survival, and risk factors. Oncologist. 2007. 12(7): 766-73. |
[4] Brufsky AM, Mayer M, Rugo HS, et al. Central nervous system metastases in patients with HER2-positive metastatic breast cancer: incidence, treatment, and survival in patients from registHER. Clin Cancer Res. 2011. 17(14): 4834-43. |
[5] Olson EM, Najita JS, Sohl J, et al. Clinical outcomes and treatment practice patterns of patients with HER2-positive metastatic breast cancer in the post-trastuzumab era. Breast. 2013. 22(4): 525-31. |
[6] Tanguturi S, Warren L. The Current and Evolving Role of Radiation Therapy for Central Nervous System Metastases from Breast Cancer. Curr Oncol Rep. 2019. 21(6): 50. |
https://www.thelancet.com/journals/lanonc/article/PIIS1470-2045(21)00716-6/fulltext
這場“五整生”大型慶生會吸引了300多名康復會員、多個患者組織、社會團體和各界人士的現場參與。現場開展了義診答疑、抗癌經驗分享、文藝演出等豐富多彩的活動。康復患者們用歌聲唱響生命的希望,用舞姿展示生命的光彩,并以充滿正能量的抗癌故事激勵更多病友堅持科學規范治療,提升疾病自我管理能力,同時,活動為癌癥患者提供廣闊的社交平臺,從“生物-心理-社會”全方位的醫學模式幫助患者早日康復,并助力提升公眾對腫瘤的認知。
看見你的光,追求更高質量的五年生存
《“健康中國2030”規劃綱要》提出,到2030年,實現全人群、全生命周期的慢病健康管理。在此背景下,“全方位、全周期”腫瘤患者健康管理模式應運而生。這就要求既往以疾病為中心的診療模式轉變為以患者為中心,即以人為中心的模式。康復護理、心理疏導和生活質量這部分曾經被忽視的領域已被置于患者全生命周期管理的重要位置。
“四川省抗癌協會作為專業的癌癥防治學術組織,始終堅持‘知識是重要的抗癌力’,致力于集結各方力量傳播科學的抗癌科普知識,幫助廣大癌癥患者科學康復。‘五整生患者慶生會’公益活動作為四川省抗癌協會康復會每年的保留項目,希望為勇敢跨越5年生存的癌友們慶祝新生,發揮群體抗癌優勢,鼓舞更多的癌友在康復會的大家庭中尋找快樂、在快樂中收獲康復。”四川省抗癌協會秘書長張文彬表示。
“曾經埋怨老天不公,是我的主治醫生鼓勵我堅持治療,是我的家人和康復會的姐妹們一次次的鼓勵幫我走出低谷,讓我學會愛自己,去發現當下最簡單的快樂。今天為五整生的兄弟姐妹們慶生,也是為自己加油,希望我們既能看見自己的光,又能匯聚更多光亮,為更多兄弟姐妹們照亮抗癌之路。”患者代表在慶生會后表示。
各方聚力,讓腫瘤患者活得更好、更有質量
今年10月,四川抗癌協會康復會聯合恒瑞醫藥“全力去愛”患者關愛品牌共同開展了腫瘤患者認知調研。調研發現,腫瘤患者對疾病認知、治療方案的選擇能力、治療藥物的不良反應處理應對以及康復過程中的隨訪意識均有待提升。在漫長的全程管理中,患者需要更多全方位、全周期的康復知識,提升規律性隨訪意識,提高疾病管理能力,獲得更高質量的5年生存。
以全球第一大癌乳腺癌為例。雖然我國乳腺癌發病率逐年上升,但隨著早期篩查和治療手段的發展,乳腺癌已成為療效最佳的實體腫瘤之一,轉變為可控可防的“慢性病”。然而,在長期的慢病管理過程中,患者規范管理疾病的意識仍有待增強。患者需要系統學習的乳腺癌規范診治科普知識,配合好醫生,才能安全跨越5年,獲得更好的生活質量。四川省抗癌協會乳腺癌專業委員會主任委員李卉教授強調:“首次診療規范對乳腺癌的療效而言尤為重要。在精準醫學時代,乳腺癌患者首先需要根據分期和分子分型進行精準施治。此外,基于影像、超聲、核醫學、病理、乳腺外科、腫瘤內科和放療科等多學科參與的綜合診療模式也是乳腺癌患者全程疾病管理的基本原則。比如在過去,HER2陽性晚期乳腺癌治愈率較低。然而,隨著臨床證據的不斷豐富以及國家醫保的納入,吡咯替尼等一系列中國原研抗HER2靶向藥被指南推薦的級別和強度持續升。HER2陽性晚期乳腺癌患者長期生存已不再是夢想。以后可能乳腺癌就像高血壓、糖尿病一樣是一種慢性病,通過綜合診療、精準施治、全程規范管理,達到與癌共存,延長壽命。”
活動支持方江蘇恒瑞醫藥股份有限公司代表王亮先生在活動現場表示:“恒瑞醫藥秉承‘以患者為中心’的理念,始終把患者的健康福祉放在首要位置,引領中國制藥企業自主創新。近年來,隨著中國原研力量的不斷崛起,越來越多的腫瘤患者從高質量的中國創新藥中獲益,突破了五年生存,甚至迎來第二個、第三個五年的到來。除了研發高質量創新藥物,恒瑞醫藥已于2020年正式推出‘全力去愛’患者關愛公益品牌,致力于集結全方位力量,積極探索與創新醫療服務生態伙伴的廣泛合作,力求為腫瘤患者提供全病程、全身心的患者關愛服務。今年10月,恒瑞醫藥‘全力去愛’公益品牌還特別推出女性健康關愛IP‘看見你的光’,旨在倡導中國女性應加強自我關懷,提升自我健康管理意識,加強疾病管理能力,鼓勵女性以積極健康的身心狀態,回歸本真自我,綻放生命光彩。作為本次‘五整生’患者慶生活動的支持方,恒瑞醫藥希望攜手抗癌協會及康復會,傳播科學的腫瘤防治核心知識要點,為患者提供全程疾病管理工具和科普知識,鼓勵患者及其家庭堅定戰勝病魔的信念,讓腫瘤患者活得更好更有質量。”
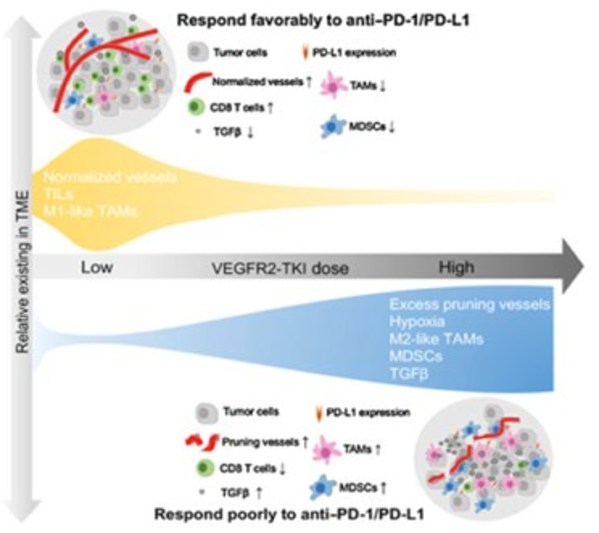
介入治療(TACE)在惡性腫瘤治療中發揮著重要作用。然而,在臨床上發現,TACE治療會導致組織缺氧,使PD-L1表達升高,還會誘導VEGF等促血管生長因子分泌增加,導致血管新生。因此,亟需新的治療模式改變TACE的治療現狀。隨著靶向治療和免疫治療的發展,以綜合治療為核心的多種治療手段聯合應用得到廣泛關注。
據該項研究主要研究者、北大荒集團總醫院腫瘤內三科主任醫師高峰教授介紹:“一方面,血管介入療法聯合免疫檢查點抑制劑為代表的免疫治療在激活免疫功能方面具有協同作用。另一方面,抗血管生成藥物既可以抑制腫瘤血管生成,也可通過誘導血管正常化降低免疫抑制,增強效應免疫細胞浸潤,進而增強抗腫瘤免疫的效果。因此,抗血管生成藥物與PD-1單抗被認為是潛在的機制互補,優勢聯合的治療方法。過往研究表明,卡瑞利珠單抗聯合低劑量甲磺酸阿帕替尼可誘導腫瘤血管正常化,重塑腫瘤免疫抑制性的微環境[2],兩者聯合可協同增效。這種聯合治療模式已在多個瘤種中的確證性研究中得到證實。未來期待介入治療聯合抗血管生成藥物和免疫治療的三聯方案能夠為不可手術切除的實體瘤患者提供一種療效良好、毒性可控的新的治療選擇。”
本研究計劃入組30例不可手術切除的實體瘤患者。符合具體入組條件的患者首先接受血管介入治療,同時局部給予卡瑞利珠單抗200 mg,每4周一次,介入治療可進行2 - 4次,之后進入維持治療階段:卡瑞利珠單抗(200mg,iv,q3w),阿帕替尼(250 mg,qd),每3周為一個周期。主要研究終點是安全性、無進展生存期,次要研究終點是客觀緩解率、疾病控制率、總生存期[1]。目前,該研究仍在進行中。
卡瑞利珠單抗是一種人源化抗PD-1單克隆抗體,目前在中國已獲批霍奇金淋巴瘤、肝癌、肺癌、食管癌、鼻咽癌等6大適應癥,且晚期肺癌、肝癌、食管癌和霍奇金淋巴瘤等4個適應癥已被納入新版國家醫保目錄。甲磺酸阿帕替尼片作為我國“十一五”、“十二五”重大新藥創制專項重點產品,于2004年被中國藥品監管部門獲批成為全球首個在晚期胃癌中應用安全有效的小分子抗血管生成靶向藥物。目前在國內已獲批晚期胃癌和肝癌等兩項適應癥。2020年《中國臨床腫瘤學會(CSCO)肝癌診療指南》已經將卡瑞利珠單抗聯合甲磺酸阿帕替尼的“雙艾”方案列為晚期肝癌一線推薦治療方案。
專家簡介:
高峰,主任醫師
北大荒集團總醫院腫瘤內三科主任
1991年畢業于臨床醫療系,從事惡性腫瘤綜合治療近30年。目前工作內容主要是腫瘤診斷、評估和放射、化療、靶向、微創及姑息治療。
中國老年腫瘤學會放療專委會常務委員
黑龍江省醫學會理事,黑龍江省醫學會腫瘤專業委員會委員,黑龍江醫學會省肺癌、腫瘤姑息治療專業委員會常務委員
黑龍江省醫師協會理事
黑龍江省醫療保健國際交流促進會腫瘤精準醫療醫療、放療專業委員會副主任委員
黑龍江省研究型醫院學會呼吸病學專業委員會常務委員
政協黑龍江省第十屆、十一屆、十二屆委員。
參考文獻:
[1] Feng G, Lili L, Lei S, et al. Vascular intervention combined with camrelizumab and apatinib for patients with inoperable solid tumors: An exploratory study. Annals of Oncology (2021) 32 (suppl_5): S829-S866. |
[2] Zhao S, Ren S, Jiang T, et al. Low-Dose Apatinib Optimizes Tumor Microenvironment and Potentiates Antitumor Effect of PD-1/PD-L1 Blockade in Lung Cancer. Cancer Immunol Res. 2019;7(4):630-643. |
食管癌是具有“中國特色”的腫瘤,每年新發和死亡病例均占全球病例的一半以上[1]。早期食管癌癥狀常不明顯,近75%的患者確診時已進展為晚期或伴有遠處轉移。對于局部晚期可切除的食管癌,單純手術治療患者預后較差,5年生存率低至14% [2,3] ,手術切除后患者復發率高達16%-47%[4]。多項研究發現,新輔助治療可延長患者生存。目前,“新輔助放化療+手術” 的治療模式是被廣泛接受的標準治療。但“新輔助放化療+手術”的應用仍存在局限性,即使患者接受新輔助放化療,術后仍有較高的復發率和遠處轉移率。此外,放化療的不良反應的毒性疊加,可能導致患者死亡率增加。因此,局部晚期食管癌患者新輔助治療亟需一種更為安全有效的治療模式。
ESPRIT研究的階段性數據顯示,對于局部晚期可切除的食管癌患者,“新輔助免疫聯合化療” 的治療模式能為患者帶來良好的疾病緩解,客觀緩解率達到50%,約56%的患者在完成新輔助治療后能夠實現降期。在13例手術患者中,所有患者均實現了完全手術切除,病理完全緩解率達到38.46%,主要病理緩解率達到61.5%。同時,這項研究也發現, “新輔助免疫聯合化療” 的治療模式具有良好耐受性,新輔助免疫聯合化療不會增加患者的手術難度。
馬建群教授在口頭報告中指出:“ESPRIT研究的結果提示,卡瑞利珠單抗聯合紫杉醇和奈達鉑新輔助治療局部晚期食管鱗癌,能夠實現腫瘤縮小并完成降期,為患者帶來良好的疾病緩解。目前,這項研究仍在持續招募患者中。我們也期待這項研究的終期結果的公布能夠為食管癌新輔助治療提供一種新的治療選擇。”
該項前沿研究對于延長患者生存時間,改善患者預后意義重大。據悉,由馬建群教授團隊發起的ESPRIT研究的研究摘要已在2021年美國臨床腫瘤學會(ASCO)年會上在線發表,其研究設計及階段性結果已獲得國際學術界關注與認可。
卡瑞利珠單抗由江蘇恒瑞醫藥股份有限公司自主研發,是一種人類免疫球蛋白G4(IgG4)單克隆抗體。目前,卡瑞利珠單抗在中國已獲批霍奇金淋巴瘤、肝癌、肺癌、食管癌、鼻咽癌等6大適應癥,且晚期肺癌、肝癌、食管癌和霍奇金淋巴瘤這4個適應癥已被納入新版國家醫保目錄。除新輔助治療以外,ESCORT-1st研究也證實,卡瑞利珠單抗聯合紫杉醇和順鉑一線治療晚期食管鱗癌患者具有顯著獲益,客觀緩解率達72.1%,中位總生存期達15.3個月。該突破性研究成果已全文在線發表于國際頂尖醫學期刊《美國醫學會雜志》(JAMA主刊)[5]。
參考文獻:
[1]. Chen W, et al. Cancer statistics in China, 2015[J]. CA Cancer J Clin, 2016, 66(2): 115-132. |
[2]. Reeh M, Nentwich MF, Asani S, et al. Locally advanced esophageal carcinoma: is there still a role of surgery alone without neoadjuvant treatment?[J]. Journal of Gastrointestinal Surgery, 2015, 19(4): 587-593. |
[3]. Yu S, Zhang W, Ni W, et al. A propensity-score matching analysis comparing long-term survival of surgery alone and postoperative treatment for patients in node positive or stage III esophageal squamous cell carcinoma after R0 esophagectomy[J]. Radiotherapy and Oncology, 2019, 140: 159-166. |
[4]. Jung HK, Tae CH, Lee HA, et al. Treatment pattern and overall survival in esophageal cancer during a 13-year period: A nationwide cohort study of 6,354 Korean patients[J]. PloS One, 2020, 15(4): e0231456. |
[5]. Luo H, Lu J, Bai Y, et al. Effect of camrelizumab vs placebo added to chemotherapy on survival and progression-free survival in patients with advanced or metastatic esophageal squamous cell carcinoma: the ESCORT-1st randomized clinical trial[J]. JAMA, 2021, 326(10): 916-925. |
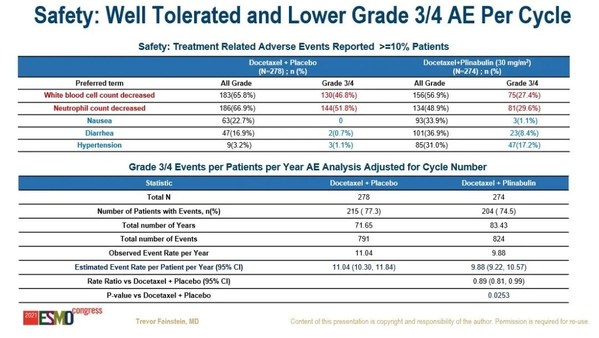
普那布林屬于GEF-H1(鳥嘌呤核苷酸交換因子)激活劑的新型“升白藥”(提升白細胞數的藥物),還可以阻止由化療藥物誘導的骨髓中性粒細胞的損傷,達到早期保護作用,是化療引起的中性粒細胞減少癥(CIN)治療的潛力藥物。在中性粒細胞保護方面具有良好的臨床療效。當前尚無與普那布林作用機制相似的藥物在臨床研究中用于預防中性粒細胞減少癥。其獨特的作用機制可顯著降低非髓性癌癥患者因化療引起的全周期中性粒細胞減少癥發生率,為廣大接受化療的患者帶來了新的獲益。
根據《柳葉刀》雜志統計,中國近年來年新發癌癥患者數量已達約450 萬人,需要預防中性粒細胞減少癥的患者總體占比超10%。中性粒細胞減少癥(CIN)是化療引起的骨髓抑制最常見的不良反應。中性粒細胞減少的程度、持續時間與患者是否容易發生感染甚至因感染導致死亡有直接的關聯。中性粒細胞減少,還會影響患者使用化療藥物的劑量、時間延遲,對患者的治療效果產生不良影響。
2020年9月,普那布林因PROTECTIVE-2(106研究)研究中的出色數據而收獲中、美兩國在中性粒細胞減少癥(CIN)治療領域的“突破性療法”雙認定。
普那布林還可以通過激活免疫防御蛋白鳥嘌呤核苷酸交換因子(GEF-H1),GEF-H1作為一種重要的生物學調節因子,在哺乳動物的一系列細胞功能中有重要作用,從而加速樹突狀細胞(DC 細胞)成熟。DC細胞負責的抗原遞呈,是免疫系統發揮作用的關鍵環節之一,從而激活T細胞來殺死腫瘤細胞,起到“免疫系統點火劑”的作用,是一款全新的、擁有獨特作用機制的免疫抗腫瘤藥物。
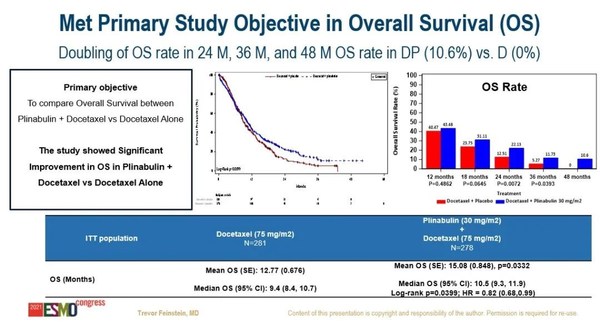
本次大會上公布的DUBLIN-3研究便是普那布林在腫瘤治療領域的新探索。DUBLIN-3是一項國際多中心、III 期、隨機對照臨床研究,旨在評估普那布林聯合多西他賽對比單藥多西他賽在EGFR野生型NSCLC二/三線治療中的安全性和有效性。根據DUBLIN-3研究結果顯示,相較于單用多西他賽組,普那布林聯合多西他賽組的平均總生存期(OS)為15.08個月vs 12.77個月,中位總生存期OS為10.5個月vs 9.4個月, 24個月OS率(22.1% vs 12.5%)、36個月OS率(11.7% vs 5.3%)以及48個月OS率(10.6% vs 0%),顯示出該聯合方案具有持久的抗癌獲益。
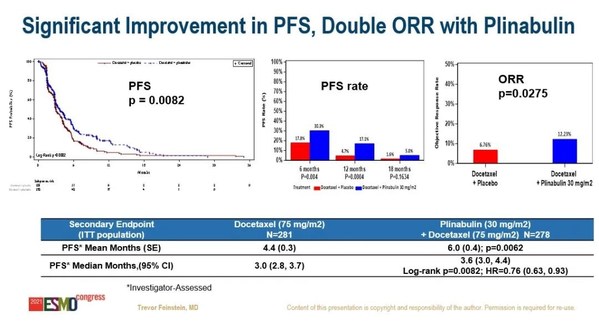
平均無進展生存期(PFS)為6.0個月vs 4.4個月,中位無進展生存期(PFS)為3.6個月vs 3.0個月,客觀緩解率(ORR)為12.23% vs 6.76%,4級中性粒細胞減少癥的發生率顯著下降(第一療程第8天:27.8% vs 5.26%;全部療程第8天:33.58% vs 5.13%)。
安全性方面,聯合治療組的耐受性良好,相較于對照組,患者生活質量更好。
DUBLIN-3研究牽頭人之一孫燕院士表示,DUBLIN-3研究顯示出良好的OS(總生存期)獲益,是自2015年納武利尤單抗上市以來首次有全新機制的藥物在NSCLC二線治療領域取得OS獲益上的突破,這是一個令人鼓舞的喜訊。DUBLIN-3研究牽頭人之一韓寶惠教授指出,這些數據充分顯示出普那布林聯合多西他賽具有良好的風險/收益比,有望改寫領域治療現狀,成為EGFR野生型NSCLC患者更好的二線及以上治療新選擇。
據悉,普那布林聯合PD-1及CTLA-4抑制劑治療小細胞肺癌(SCLC)的研究已經顯示出令人欣喜的療效,普那布林用于PD-1/PD-L1單抗治療失敗或疾病進展患者的I期臨床試驗也已在啟動當中。普那布林這一類腫瘤免疫激活療法有望成為除PD-1/PD-L1單抗以外免疫治療的新基石。
2021年4月,普那布林已向國家藥品監督管理局藥品審評中心和FDA遞交用于中性粒細胞減少癥(CIN)的新藥上市申請。同年8月,恒瑞醫藥與萬春醫藥子公司大連萬春簽訂戰略合作協議,獲得GEF-H1激活劑普那布林在大中華地區的聯合開發權益以及獨家商業化權益,以用于防治所有人類與動物疾病,包括但不限于化療引起的中性粒細胞減少癥(CIN)和癌癥,普那布林對恒瑞醫藥在抗腫瘤領域的管線布局形成有效補充。作為中國原研力量代表,恒瑞醫藥今年攜30余項重要研究入選2021歐洲腫瘤內科學會(ESMO)年會Poster Session。涵蓋肺癌、肝癌、胃癌、食管癌、乳腺癌、卵巢癌等多個癌種。相信在PROTECTIVE-1/2、DUBLIN-3等研究出色數據的支撐下,在恒瑞醫藥的強勢助力下,普那布林這一民族原研First-in-Class新藥距離獲批上市,走向世界惠及全球患者已不遙遠。
“關愛行動 -- 腫瘤患者大型公益項目”于4月整體啟動。項目一期在江蘇恒瑞醫藥股份有限公司的公益支持下,圍繞目前腫瘤患者所關心的腫瘤預防、疾病科普、規范診療、藥物應用、情緒/心理管理等腫瘤治療相關知識,聚焦肺癌、肝癌、乳腺癌、胃癌和食管癌五大癌種,全面開展各項大眾科普和患者關愛活動,以助力推動我國腫瘤患者的全流程健康管理,推進健康中國行動全面落地。
肺癌是中國發病率和死亡率增長最快的惡性腫瘤之一。2020年新發患者數為82萬,其中肺癌致死人數高達71萬,我國肺癌防治工作面臨巨大挑戰。近年來,伴隨著精準診療技術的進步,肺癌的治療格局日新月異,靶向治療和免疫治療的出現,為肺癌患者帶來了新的希望。
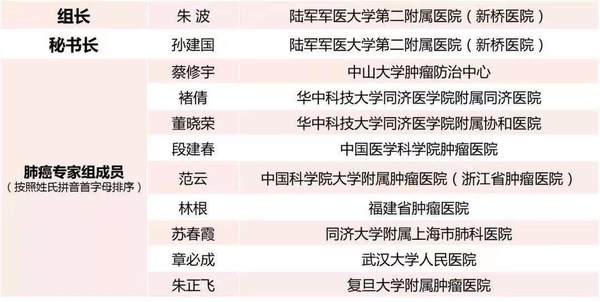
關愛行動-肺癌專家組組長、大會主席、陸軍軍醫大學第二附屬醫院(新橋醫院)朱波教授在啟動會致辭中指出:“臨床醫生不斷探索新療法,尋找新突破,提升肺癌患者生存質量、延長患者生存期的同時,更需要患者的理解與配合,以及全社會的廣泛參與。秉承“關愛每一位患者”的醫者初心,我們此次成立關愛行動肺癌專家組,開展患者關愛專題活動。未來,專家組將圍繞肺癌全程管理、免疫治療等新療法在肺癌領域中的應用與進展等方面,為肺癌患者與家屬提供最專業的知識科普與答疑。相信未來通過更多“關愛行動”,切實加強更有效的醫患溝通,盡可能地為更多的肺癌患者提供有益的診療信息與生存信心。”
傳統治療模式下,許多晚期腫瘤患者的長期生存不佳,臨床亟需新的腫瘤治療藥物和治療方法。近年來,免疫治療異軍突起,PD-1/PD-L1抑制劑已獲批多個腫瘤適應證。免疫系統是人體重要的防御系統,除了發揮免疫防御和維持內環境穩定的作用外,還能夠識別并清除腫瘤,免疫檢查點抑制劑(ICIs)正是通過激活免疫系統來殺死腫瘤細胞。免疫治療具有長拖尾效應,即有效的患者可以獲得持久的生存獲益,5年生存率較傳統的治療方案明顯提高。免疫治療在非小細胞肺癌(NSCLC)治療領域有著較為廣泛的應用場景。
同濟大學附屬上海市肺科醫院蘇春霞教授在“免疫治療在非小細胞肺癌的應用”專題討論中指出:“在非鱗非小細胞肺癌NSCLC中,免疫治療占據驅動基因陰性患者一線治療的主導地位,聯合化療可顯著提高治療有效率。卡瑞利珠單抗CameL研究是第一個針對中國NSCLC患者的一線免疫聯合化療的III期臨床研究,研究結果顯示中位總生存(OS)達到27.9個月,是目前全球同類臨床研究中最長的中位OS數據。至此,驅動基因陰性的晚期非鱗狀NSCLC的治療發展跨越50年長河,患者的OS提高至50年前的6倍。免疫治療同樣給晚期鱗狀NSCLC一線治療患者帶來顯著生存獲益。在中國人群中開展的CameL-sq研究為中國患者的臨床實踐提供了堅實的證據,研究結果顯示,卡瑞利珠單抗聯合紫杉醇/卡鉑組的中位PFS達到8.5個月,進展風險降低63%,患者生存獲益明顯。”
據蘇春霞教授介紹:“免疫治療較傳統化療有著非常規的應答模式。免疫治療后,腫瘤可能不會立刻縮小,免疫治療啟動抗腫瘤的細胞免疫過程需要一定時間,PD-1/PD-L1抑制劑起效時間通常為3個月左右。并且部分患者在免疫治療初期可能出現假性進展,病灶暫時增大或出現一些小的新病灶,但臨床癥狀無明顯加重,繼續用藥后腫瘤可逐漸縮小甚至消失。免疫治療需要長期維持,在多項III期臨床研究中,治療持續時間通常是至疾病進展或患者出現不可耐受的毒性反應,有研究顯示,停藥可導致腫瘤再次復發。目前,被批準用于治療晚期非小細胞肺癌的常見PD-1抑制劑有帕博利珠單抗、納武單抗、卡瑞利珠單抗、替雷利珠單抗、信迪利單抗等。國家醫保積極推動免疫治療惠及更多中國患者,首個被納入國家醫保目錄的肺癌領域PD-1抑制劑是卡瑞利珠單抗,也是目前唯一肺癌適應證可報銷的PD-1抑制劑,這為患者的長期維持治療提供了有力保障。”
專家講座結束后,針對患者高頻咨詢的問題,中山大學腫瘤防治中心蔡修宇教授和武漢大學人民醫院章必成教授在線上進行了答疑。本次活動面向全國患者及家屬直播,引起了強烈反響。患者們通過線上形式積極與專家互動交流,對各位專家的講解和公益關愛表示由衷的感謝。后續肺癌專家行動組將在全國范圍內開展形式多樣的患者關愛活動,助力腫瘤健康科普事業,共筑健康長城。
附:第一屆CSCO-CMT關愛行動肺癌專家組成員名單
卵巢癌,女性健康頭號威脅
卵巢癌,包括輸卵管癌及原發腹膜癌是婦科最常見的惡性腫瘤之一,其發病率居女性生殖道惡性腫瘤第三位,且呈逐年上升的趨勢,死亡率高居婦科腫瘤首位,嚴重威脅女性健康。
卵巢癌起病隱匿,70%患者確診即為晚期,治療以手術及術后含鉑方案的聯合化療為主。復發率高,隨著化療線數的增加,腫瘤對于含鉑方案治療的敏感性逐漸降低,至疾病進展時間(TTP)逐漸縮短,同時化療產生的毒性、過敏反應發生率也會隨著化療周期數增加而逐漸增加,因此最大程度延長無鉑治療間期(PFI)是治療復發性卵巢癌的關鍵。
為卵巢癌維持治療帶來新希望
PARP抑制劑是目前公認的更為有效的用于卵巢癌維持治療的藥物,可有效降低卵巢癌的復發風險,延長患者生存,而高效低毒則是PARP抑制劑用于維持治療的先決條件。
作為中國首個原研PARP抑制劑,恒瑞醫藥研發的氟唑帕利在先后兩次適應癥的臨床研究中,均高度驗證了其高效低毒的特點。
2020年12月,氟唑帕利獲批上市用于既往經過二線及以上化療的伴有胚系BRCA突變(gBRCAm)的鉑敏感復發性卵巢癌、輸卵管癌或原發性腹膜癌患者的治療。同月,恒瑞醫藥提出本次新適應癥申請,后獲得優先審評審批資格。
本次適應癥批準基于由中國醫學科學院腫瘤醫院吳令英教授牽頭的一項氟唑帕利對比安慰劑用于鉑敏感的復發性卵巢癌維持治療的隨機、對照、雙盲的全國多中心III期臨床研究(FZOCUS-2臨床研究),研究期中分析結果顯示,氟唑帕利維持治療能夠顯著延長鉑敏感復發性卵巢癌患者的PFS,降低患者75%的疾病進展/死亡風險,且無論患者是否伴BRCA1/2突變,均能從氟唑帕利治療中獲益。同時,氟唑帕利耐受性良好,治療安全可控。
該研究結果于今年SGO年會口頭報告公布,引起業內高度關注與一致認可。
前景廣闊,氟唑帕利未來可期
半年內,氟唑帕利先后獲批兩個適應癥,足見其優異的臨床價值。
與此同時,氟唑帕利并未停下探索適應癥拓展的腳步。目前,恒瑞醫藥關于氟唑帕利的研究已登記30余項,除卵巢癌外,還在小細胞肺癌、乳腺癌、胰腺癌、前列腺癌、胃癌等瘤種中開展相關研究。除用于鉑敏感的復發性卵巢癌、輸卵管癌或原發性腹膜癌治療外,氟唑帕利膠囊單藥或聯合甲磺酸阿帕替尼片的多個適應癥開發已處在III期臨床研究階段,另有多種聯合治療方案,包括與阿比特龍聯合、與抗PD-L1抗體SHR-1316聯合、以及與替莫唑胺聯合治療多種實體腫瘤已處于臨床開發階段。
作為創新型民族制藥企業,恒瑞醫藥多年來一直堅持原研,致力于為中國患者提供更多的治療機會。未來,恒瑞將進一步充分發掘氟唑帕利的潛力,為更多患者造福。





































![2021年歐洲腫瘤內科學會(ESMO)年會壁報展示[1] 2021年歐洲腫瘤內科學會(ESMO)年會壁報展示[1]](https://mma.prnasia.com/media2/1661242/1.jpg?p=medium600)