綠葉生命科學集團董事局主席劉殿波、綠葉制藥(國際)總裁張業泓博士、綠葉制藥(國際)亞太區副總裁Andy Siow、明仁制藥董事長Hang-Myung Lee、明仁制藥總裁兼工廠經理Jae Hyuk Kim、明仁制藥業務拓展總監Jung Uk Lee、明仁制藥業務拓展經理Wonmo Suh等雙方公司代表出席合作簽約儀式,共同見證這一里程碑時刻。
當前,阿爾茨海默病已成為全球范圍內一大公共健康挑戰。隨著韓國人口老齡化程度的加劇,該疾病在當地的患病率亦持續攀升[1],[2]。由阿爾茨海默病造成的記憶障礙、認知異常等問題,使該疾病的治療存在諸多困難。實際臨床治療過程中,患者存在用藥依從性差、因不良事件停藥發生率高、用藥管理困難等問題,不僅嚴重影響治療效果,也給家庭、社會帶來沉重的照護和經濟負擔。
利斯的明是治療輕、中度阿爾茨海默病的一線用藥。利斯的明透皮貼劑(2次/W)通過創新的給藥途徑,每周經皮膚給藥兩次。與市售的利斯的明單日透皮貼劑相比,每周給藥兩次的利斯的明透皮貼劑具有更低的使用頻率,可改善患者的用藥依從性;與口服制劑相比,利斯的明透皮貼劑(2次/W)通過穿透皮膚被人體吸收,亦為存在吞咽困難的病患提供了良好的用藥便捷性,并有望降低惡心、嘔吐等腸胃不良反應的發生率。
合作方明仁制藥是中樞神經系統(CNS)治療領域的韓國本土領軍企業,圍繞該治療領域布局重點品種并形成豐富的產品組合。談及此次合作,明仁制藥董事長Hang-Myung Lee表示:"阿爾茨海默病是一種神經退行性疾病,患者數量不斷增加,而現有治療選擇卻很有限。我們很高興與綠葉制藥攜手合作,將這一給藥便捷的創新產品帶給廣大患者。CNS是我們的核心治療領域,利斯的明透皮貼劑(2次/W)將作為我們產品組合的重要戰略補充,進一步強化我們在該治療領域的領先地位,更好地服務患者所需。"
"相信憑借明仁制藥在CNS領域豐富的經驗和專長,以及在韓國當地強大的運營體系,能夠助力利斯的明透皮貼劑(2次/W)上市后盡快惠及當地患者。"綠葉制藥(國際)亞太區副總裁Andy Siow表示:"我們很高興與明仁制藥就該產品達成合作。綠葉制藥亦長期深耕CNS治療領域,并已積累了一系列具有國際化競爭力和差異化優勢的創新產品組合。我們期待持續深化在韓國的伙伴關系,助推公司更多CNS產品引進韓國市場,造福當地患者。"
綠葉制藥面向全球市場開發和商業化利斯的明透皮貼劑(2次/W)。當前,該產品已分別在歐洲多國和中國獲批上市。公司亦在歐洲多國、日本、中國、墨西哥、泰國等國家與當地合作伙伴達成該產品的合作。
[1] Tae Ho Huh, Jong Lull Yoon, Jung Jin Cho, et al. Survival Analysis of Patients with Alzheimer's Disease: A Study Based on Data from the Korean National Health Insurance Services' Senior Cohort Database. Korean Journal of Family Medicine 2020;41(4):214-221. |
[2] Min Seok Baek, Han-Kyeol Kim, Kyungdo Han, et al. Annual Trends in the Incidence and Prevalence of Alzheimer's Disease in South Korea: A Nationwide Cohort Study. Front Neurol. 2022; 13: 883549. |
關于綠葉制藥集團
綠葉制藥集團是致力于創新藥物的研發、生產和銷售的國際化制藥公司。綠葉制藥在中國、美國和歐洲設有研發中心,擁有超過30個中國在研藥物和10多個海外在研藥物。綠葉制藥在微球、脂質體、透皮釋藥等先進藥物遞送技術領域達到國際先進水平,在新分子實體、生物抗體領域收獲多項創新成果,并在細胞治療、基因治療等領域進行了積極布局和開發。
綠葉制藥深度布局全球供應鏈體系,已在全球建有8大生產基地,并建立了與國際接軌的GMP質量管理和控制體系。公司現有30余個上市產品,產品覆蓋腫瘤、中樞神經、心血管、消化與代謝等治療領域;業務遍及全球80多個國家和地區,其中包括中國、美國、歐洲、日本等全球主要醫藥市場,以及高速增長的各地新興市場。
關于明仁制藥
明仁制藥(Myung In Pharm)成立于1985年,總部位于韓國首爾,是一家全面綜合型制藥公司。該公司的業務范圍涵蓋藥物生產、加工和處理。明仁制藥是韓國中樞神經系統治療領域的本土領軍企業,與當地1,200名神經科醫生和98%的神經科醫院科室建立了客戶關系。公司擁有先進的生產設施與生產設備,以保障藥品質量。所有生產設施均符合cGMP標準。

Abacus Medicine Pharma Services亞洲有限公司總經理William Van與綠葉制藥(國際)亞太區商務總監蕭幸偉簽署Lurbinectedin香港分銷服務協議,用于“指定患者藥物使用計劃”
該項"指定患者藥物使用計劃"旨在幫助罹患小細胞肺癌卻尚無其他治療選擇的患者,在符合當地法律法規和倫理規范的前提下以及在臨床醫生專業評估的支持下獲得治療藥物Lurbinectedin,項目覆蓋香港地區所有醫院。
Lurbinectedin是一種選擇性的致癌基因轉錄抑制劑,于2020年獲得美國食品藥品監督管理局(FDA)的加速批準,用于治療在含鉑類化療過程中或化療后出現疾病進展的轉移性小細胞肺癌成年患者。該藥物是最近二十五年來首個獲得美國FDA批準的用于治療復發性小細胞肺癌的新分子實體,目前在中國香港處于新藥上市審評階段。
小細胞肺癌是一種高級別神經內分泌癌,約占肺癌的15%[1]。該疾病確診時多為晚期,預后極差,五年生存率僅7%,廣泛期小細胞肺癌患者的五年生存率僅3%[2]。大多數小細胞肺癌患者會在初始治療后出現復發及耐藥,該疾病的高復發為其治療帶來巨大挑戰,臨床亟需創新治療方案。
香港中文大學內科及藥物治療學系榮譽臨床副教授、臨床腫瘤科專科醫生梁廣泉指出:"小細胞肺癌是一種治療相對困難的肺癌亞型,具有惡性程度高、預后差、復發性高的特點。該疾病復發后缺乏新的藥物治療選擇是當下臨床應用中所面臨的主要挑戰。我們非常高興地看到,通過‘指定患者藥物使用計劃'可以幫助符合條件的病人獲得這一創新療法,改善他們的預后。"
香港精準腫瘤醫學會主席、臨床腫瘤科專科醫生區兆基表示:"肺癌是香港地區致死率最高的癌癥。而過去30年來,因缺乏有效的藥物使小細胞肺癌的治療尤為‘棘手'。我們相信,Lurbinectedin是該治療領域的一大突破,能夠為復發性小細胞肺癌的患者提供更好的治療選擇。"
綠葉制藥(國際)亞太區商務總監蕭幸偉表示:"綠葉制藥以未滿足治療需求為出發點,研發、生產和銷售抗腫瘤新藥。啟動‘指定患者藥物使用計劃'能夠幫助患者及時獲得Lurbinectedin,滿足臨床急需,為飽受疾病困擾的小細胞肺癌患者帶來新的希望。"
Abacus Medicine Pharma Services 亞洲有限公司總經理William Van表示:"我們很高興能夠與綠葉制藥達成分銷合作,支持Lurbinectedin在香港地區的‘指定患者藥物使用計劃'。期待通過我們在相關項目運營上的廣泛經驗以及在當地的業務網絡和渠道優勢,與綠葉制藥共同努力、緊密協作,更好地為當地患者服務。"
除了在中國香港地區,Lurbinectedin也已作為臨床急需藥品落地海南博鰲樂城國際醫療旅游先行區特定醫療機構服務于中國內地患者。
參考文獻:
1. Rudin CM, et al. Nat Rev Dis Primers. 2021 Jan 14;7(1):3.
2. Cancer.Net. Lung Cancer - Small Cell. Available at https://www.cancer.net/cancer-types/33776/view-all. Accessed in October 2022.
]]>博安生物成立于2013年,致力于在中國及海外開發、制造及商業化優質生物制品,為腫瘤、代謝、自身免疫及眼科等主要治療領域提供創新、可及的治療方案。作為一家全面綜合性生物制藥公司,博安生物憑借差異化的產品組合、覆蓋"研發-生產-商業化"的全產業價值鏈運營體系、以及不斷成熟的商業化能力構筑起自身獨特的競爭優勢。
差異化的產品組合,多款在研藥物具先發優勢
憑借高效的內部創新能力,博安生物的所有產品均為自主研發。目前,公司的產品管線中已構建了多個擁有國際知識產權保護的創新抗體候選藥物和生物類似藥候選藥物的產品組合,既為公司短期的商業化提供明確路徑,也為其長期的可持續發展奠定良好基礎。
截至目前,博安生物已成功實現兩款產品的商業化:首款產品博優諾®(BA1101)是國內第三個獲批上市的貝伐珠單抗生物類似藥,用于多種癌癥的治療。第二款產品博優倍®(BA6101)為全球首個獲批上市的地舒單抗生物類似藥,用于骨質疏松癥的治療。
公司另有12種候選藥物,其中多個品種已臨近商業化階段:腫瘤領域的BA1102(地舒單抗注射液,安加維®生物類似藥)、眼科領域的BA9101(阿柏西普眼內注射液,艾力雅®生物類似藥)、代謝領域的BA5101(度拉糖肽注射液,度易達®生物類似藥)均在中國處于III期臨床階段,且開發進度位處前列。此外,BA6101與BA1102亦在歐盟處于I期臨床階段。公司預計將在未來兩年內陸續提交多個候選藥物的生物制品許可申請(BLA)。
在創新抗體的開發上,博安生物兼顧"創新價值"與"商業能見度",在構建具有差異化特色的產品組合的同時,亦加快研發速度以獲得更多先發優勢。例如:公司自主研發的ADCC增強型Claudin18.2靶向的全人源單克隆抗體BA1105,有望成為同類治療轉移性胰腺癌、晚期胃癌及食管胃交接部腺癌的最佳靶向藥物;抗CD25全人源單克隆抗體BA1106為國內首個開始臨床試驗的、治療實體瘤的抗CD25創新抗體;自身免疫治療領域的抗IL-4Rα全人源單克隆抗體BA2101是國內首個進入臨床試驗階段的抗IL-4Rα長效新藥。
完整的生物藥運營體系,鍛造全產業鏈核心優勢
通過多年的積累,博安生物已完成從0到1的、完整的生物藥運營體系的構建。公司已建立的三大自主創新技術平臺,涵蓋從研發到生產再到商業化運營的一體化生態系統,以及一支分布在煙臺、南京、新加坡、波士頓的國際化專業化團隊,為產品管線的高效推進及卓越上市奠定了扎實的基礎。
通過三大自主創新技術平臺,博安生物已建立起強大的技術優勢:一方面,公司基于全人抗體轉基因小鼠BA-huMab®及噬菌體展示技術平臺,提高全人源單克隆抗體產品的研發效率。博安生物也是中國少數擁有自主轉基因小鼠平臺的企業之一。另一方面,在單抗產品基礎上,公司通過雙特異T-cell Engager技術平臺、抗體藥物偶聯(ADC)技術平臺開發雙特異性抗體、ADC藥物等特色領域,形成差異化的產品組合。
博安生物擁有全面綜合性及可擴展的生物制藥平臺,涵蓋抗體發現、細胞株開發、上游及下游工藝開發、分析及生物分析方法開發、技術轉移及中試與商業化規模生產的全整合型產業鏈。不僅如此,其強大的CMC能力為整個藥物開發及商業化生產過程中的高質量及成本效率保駕護航,并能夠縮短藥物開發時間,為其產品的首發優勢鋪路。
成熟的商業化能力,保障產品卓越上市
博安生物是中國為數不多的能夠從最初藥品發現及開發到最終提交BLA并實現產品商業化的生物制藥公司,更是為數不多的在掛牌上市時便擁有兩款商業化產品的18A生物科技公司。
博安生物的首款產品博優諾®針對龐大的癌癥治療需求,自2021年5月面市后便獲得理想的銷售業績。該產品于2021年實際銷售的8個月內實現銷售收入1.59億元人民幣,2022年上半年的銷售收入達到2.21億元人民幣。
依托博優諾®的順利上市,博安生物已建立起廣泛的商業化網絡和成熟的商業化能力。截至目前,其廣泛的分銷網絡已覆蓋全國千余家醫院。此外,通過博優諾®的商業化,博安生物打通了"研發-生產-商業運營"各個環節,為其后續多個臨近商業化階段的藥物實現加快上市、迅速上量奠定堅實基礎。
博安生物的第二款產品博優倍®用于骨折高風險的絕經后婦女的骨質疏松癥。該產品于2022年11月在中國獲批上市后,即于當月底開始面向全國銷售。作為目前唯一在中國獲批的國產地舒單抗注射液,博優倍®在商業化方面具有先發優勢。公司已從生產、準入、銷售等各個環節做好準備,將持續提升博優倍®的用藥可及性。
此外,博安生物積極攜手業內優秀的合作伙伴,借助其豐富的資源,最大程度地挖潛產品的臨床價值和市場潛力。例如公司授予阿斯利康中國在各省市及自治區的多個縣域地區獨家推廣博優諾®;公司與歐康維視就BA9101在中國的產品開發、推廣及商業化展開合作等。
立足中國,志在成為"全球領先的生物制藥公司"
成功登陸港交所,不僅是博安生物發展歷程中的重要里程碑,也為其邁向下一階段的發展開啟新篇章。博安生物將抓住全球生物藥產業的發展浪潮,延續當下蓬勃發展的態勢,進一步加快在研產品在中國和海外市場的臨床開發,豐富創新抗體產品組合,深化內部制造能力及全球化商業化能力,并積極拓展各項業務合作,以加快推動公司從Biotech向Biopharma進階。
博安生物董事會主席兼首席執行官姜華表示:"今天的掛牌上市是博安生物發展歷程中的又一個新起點。回望博安生物建立的初心,我們不僅立足中國,更致力于成為'全球領先的生物制藥公司'。我們期待早日以高品質的國產生物藥產品,服務于全球患者亟待滿足的治療需求,為人類健康貢獻一份‘博安'力量。"
綠葉制藥集團執行主席劉殿波表示:"'生物藥戰略'是綠葉制藥集團當下及未來發展中極其重要的業務戰略之一。我們很高興地看到,經過多年的積累,博安生物已在生物藥業務領域構筑起獨特的競爭優勢。我們非常看好博安生物上市后的表現,也將利用集團深厚的產業積淀全力支持其下一階段的發展。期待博安生物持續協同集團的其他業務板塊,踐行我們'以專業技術服務于人類健康'的使命。"
關于博安生物
博安生物為綠葉制藥集團的控股子公司,是一家全面綜合性生物制藥公司,專業從事治療用抗體開發、生產和商業化,專注于腫瘤、自身免疫、眼科和代謝疾病。公司的抗體發現活動圍繞三大平臺展開,即全人抗體轉基因小鼠及噬菌體展示技術平臺、雙特異 T-cell Engager 技術平臺及抗體藥物偶聯(ADC)技術平臺。目前,博安生物的產品管線中已擁有兩款商業化產品,以及多個具有國際知識產權保護的創新抗體和生物類似藥的在研產品組合。
博安生物擁有完整的涵蓋抗體發現、細胞株開發、上游及下游工藝開發、分析及生物分析方法開發、技術轉移及中試與商業化規模生產的全整合型產業鏈。除了在中國,博安生物也在美國及歐盟市場從事生物藥產品開發。
關于綠葉制藥集團
綠葉制藥集團是致力于創新藥物的研發、生產和銷售的國際化制藥公司。綠葉制藥在中國、美國和歐洲設有研發中心,擁有超過30個中國在研藥物和10多個海外在研藥物,在中樞神經和腫瘤領域已有多個創新制劑和創新藥在歐洲、美國、日本開展注冊及臨床研究。綠葉制藥在微球、脂質體、透皮釋藥等先進藥物遞送技術領域達到國際先進水平,在新分子實體、生物抗體領域收獲多項創新成果,并在細胞治療、基因治療等領域進行了積極布局和開發。
綠葉制藥深度布局全球供應鏈體系,已在全球建有8大生產基地,超過30條生產線,并建立了與國際接軌的GMP質量管理和控制體系。公司現有30余個上市產品,覆蓋腫瘤、中樞神經、心血管、消化與代謝等治療領域;業務遍及全球80多個國家和地區,其中包括中國、美國、歐洲、日本等全球主要醫藥市場,以及高速增長的各地新興市場。
北京大學第六醫院陸林院士、中南大學湘雅二醫院李凌江教授、北京大學第六醫院于欣教授、上海市精神衛生中心趙敏教授、廣東省人民醫院賈福軍教授、北京回龍觀醫院楊甫德教授、上海市精神衛生中心方貽儒教授、中南大學湘雅二醫院王小平教授等專家與線上逾千名醫生共同參加上市會,并與綠葉制藥集團總裁楊榮兵、綠葉制藥集團副總裁、綠葉制藥(中國)負責人李莉、綠葉制藥集團非臨床研究部副總裁田京偉博士、綠葉制藥(中國)中樞神經系統事業部負責人陳哲等企業代表共同見證了這一里程碑時刻。
北京大學第六醫院院長陸林院士對于若欣林®的上市表示祝賀:"抑郁癥影響著全球近3億人,自新冠疫情以來,該疾病患病率更是呈現增高趨勢,我們面臨的相關發病情況與疾病負擔日益嚴峻。然而,精神疾病領域的新藥研發難度大,一直是創新藥物的‘研發洼地',很高興看到若欣林®作為我國首個自主研發的抗抑郁化藥1類創新藥上市,實現國產創新藥在該治療領域的重大突破。"
中華醫學會精神醫學分會主任委員李凌江教授在會上指出:"抑郁障礙是患病率很高的精神障礙,據中國精神疾病流行病學報告為6.8%,臨床治療面臨很多困境。若欣林®的上市,打破了國產抗抑郁化藥創新藥的研發瓶頸,開啟國內抑郁癥治療的新篇章。作為臨床醫生,我們非常期待該藥物投入臨床應用,以更好的療效與安全性,惠及更廣泛的抑郁癥患者群體。"
曙光在望:若欣林®有望改變抗抑郁治療格局
作為最普遍的情緒障礙之一,抑郁癥治愈率低,大量患者在達到臨床緩解后仍長期存在殘留癥狀,導致社會功能受損,復發風險陡增;而藥物不良反應也影響患者的用藥依從性,成為導致預后差的又一重要因素。抑郁癥復發率高達50%~85%,其中50%的患者會在疾病發生后的2年內復發1。
上海市精神衛生中心院長趙敏教授指出:"抑郁癥患者人群龐大,但臨床表現卻不盡相同。現有抗抑郁藥物雖總體有效,但治愈率尚不理想,部分癥狀維度在治療中仍是難點。如何改善藥物治療效果和預后,是擺在抗抑郁治療面前的重要課題。面對廣大患者的未滿足需求,臨床期待新的治療武器。"
抑郁癥有著復雜且多元的癥狀表現,其多維癥狀受到5-羥色胺(5-HT)、去甲腎上腺素(NE)和多巴胺(DA)三種神經遞質的共同影響。同時提高突觸間隙5-HT、NE和DA的水平,可實現治療作用相互協同,更全面地緩解抑郁癥患者不同維度的癥狀,同時增加DA的干預可能拮抗5-HT水平增加帶來的DA能下降所引起的副作用2。
若欣林®是綠葉制藥自主研發的全新分子實體。臨床前研究表明,其對于5-HT、NE和DA均具有再攝取抑制作用。臨床研究結果證實:若欣林®能夠全面、穩定的治療抑郁癥,顯著改善患者焦慮狀態、阻滯/疲勞癥狀、快感缺失和認知能力,促進社會功能恢復;而且具有良好的安全性和耐受性,不引起嗜睡,不影響性功能、體重和脂代謝。此外,若欣林®不經肝臟CYP450酶系代謝,藥物相互作用少。
若欣林®研發項目負責人、綠葉制藥集團非臨床研究部副總裁、新藥發現研究部負責人田京偉博士表示:"很高興看到若欣林®的上市,為廣大患者帶來新的治療選擇。若欣林®通過多靶點的干預治療可實現更好的療效和安全性,有助于患者全面緩解多維度癥狀,幫助其恢復社會功能,為患者早日回歸家庭、社會提供有力支持。"
蔚然成"林":兼顧常見殘留癥狀,若欣林®多重治郁
針對抑郁癥治療,國內外權威指南均強調以"獲得臨床治愈、減少復發風險、改善功能損害、提高生活質量"為目標,倡導全面重視情感、軀體和認知在內的所有癥狀維度。
研究發現,抑郁癥患者治療后殘留癥狀發生比例約為30%~50%3-4,常見的殘留癥狀包括焦慮、認知損害、疲勞、快感缺失等5-6。殘留癥狀的多少與患者社會功能、生活質量等密切相關:殘留癥狀越多,患者社會功能受損越嚴重,同時患者的生活質量滿意度、醫療滿意度也越低,病程越傾向于慢性化,自殺企圖就會越高7。
北京大學第六醫院精神科主任醫師張鴻燕教授指出:"許多患者在接受抗抑郁治療后,核心癥狀得到緩解,但伴隨癥狀的殘留可能造成社會功能受損,甚至因癥狀殘留導致抑郁癥的復發。若欣林®對于抑郁癥多維度癥狀的全面兼顧,尤其在改善焦慮、快感缺失、疲勞、認知癥狀等方面的療效潛力,填補了抗抑郁治療中亟待滿足的患者需求,有助于患者生活品質的提升和社會功能的恢復,以達到穩定和真正意義上的臨床痊愈。"
向"欣"而行:良好的安全耐受性,利于提升全病程治療依從性
除了殘留癥狀,接受藥物治療的抑郁癥患者也面臨著藥物不良反應帶來的主觀痛苦及軀體共病,性功能障礙、體重增加、嗜睡等均是抗抑郁藥物治療中常見的不良反應8。研究顯示,超過80%的患者至少經歷過一種不良反應,每位患者平均經歷過4種不同的不良反應9-10。不少患者因藥物不耐受而自行停藥,甚至從一開始就抗拒治療,使治療效果受到很大影響。
臨床研究結果顯示:若欣林®具有良好的安全耐受性。其患者治療依從性達到90%以上,且不影響性功能、體重和脂代謝,對血壓和睡眠影響小。此外,若欣林®不經肝臟CYP450酶系代謝,對CYP450酶系無抑制或誘導作用,藥物相互作用風險低。
針對若欣林®上述特性帶來的臨床價值,與會專家紛紛指出,抑郁癥的治療是一個長期治療的過程,臨床提倡全病程規范治療,涵蓋急性期、鞏固期和維持期。藥物的不良反應是全病程治療的"絆腳石", 易引發治療中斷,加劇復發風險。安全性和耐受性良好的抗抑郁藥能夠提升患者治療的依從性,更利于患者的全病程規范治療,提高臨床治愈率。
同"欣"協力:加速藥品可及,服務患者所需
若欣林®獲得上市批準后,為了使這一創新治療方案盡快惠及患者,綠葉制藥憑借自身在中樞神經治療領域長期積累的優勢與資源,通過專業化的自有營銷團隊、強大的商業化網絡,實現該藥物在獲批后的短短27天內正式投入臨床使用,并通過醫院、藥店和線上平臺等各大渠道服務全國患者。
與此同時,綠葉制藥積極擁抱各種創新資源與合作契機,通過與恩華藥業、好心情平臺等同樣深耕中樞神經治療領域的合作伙伴達成戰略合作,并通過與母集團旗下的精神心理健康專科品牌 -- 曼朗醫療的協同聯動,發揮彼此的優勢專長,以更快的速度、更廣泛的覆蓋,滿足廣大患者治療所需。
綠葉制藥集團總裁楊榮兵表示:"抑郁癥是嚴重危害大眾健康和生活質量的一大疾病難題,不僅影響患者的正常工作和生活,也為其家庭和社會帶來沉重的經濟和照護負擔。針對臨床亟待滿足的治療需求,我們正在加快推動若欣林®在各個層面的市場準入,積極提升藥物可及性。期待若欣林®能夠幫助更多患者,更好地提高其治愈水平、助力其早日回歸社會。"
參考文獻:
1. 中國抑郁障礙防治指南(第二版):47
2. Murugaiah A. M. J. Med. Chem. 2018, 61(6), 2133-2165.
3. RUSH AJ.TRIVEDI MH.WISNIEWSKI SR,et al. Acute and longer-term outcomes in depressed outpatients requiring one or several treatment steps: a STAR*D report[J]. Am J Psychiatry.2006,163(11): 1905-1917.
4. 肖樂.豐雷.朱雪泉.等.中國抑郁癥患者急性期治療后殘留癥狀的現況調查 [J].中華精神科雜志,2017,50(3): 175-181.
5. 趙榮江,等. 精神醫學雜志,2020,33(5):326-329.
6. Hiranyatheb T, et al. Neuropsychiatric Disease and Treatment, 2016, 12: 3175.
7. NIL R,LUTOLF S,SEIFRITZ E. Residual symptoms and functionality in depressed outpatients: A one-year observational study in Switzerland with escitalopram [Jl. J Affect Disord, 2016,197: 245-250.
8. Cartwright C,et al. Patient Prefer Adherence. 2016 Jul 28;10:1401-7.
9. MGH Housestaff Manual. Department of Medicine, Massachusetts General Hospital June 2019.
10. Managing the Adverse Effects of Antidepressants. Psychiatric Times, Vol 31 No 7, Volume 31, Issue 7
]]>今年是上合組織憲章簽署20周年和成員國長期睦鄰友好合作條約簽署15周年,同時正逢中國同包括烏茲別克斯坦在內的中亞五國建交30周年。2016年中烏兩國關系提升為全面戰略伙伴關系。近年來,中國已成為烏茲別克斯坦第一大貿易伙伴和第一大出口目的國。在"一帶一路"建設框架下,雙方在經貿、文化、投資、能源等領域緊密合作,深耕發展。
世紀疫情與百年變局交織,為響應構建"人類健康命運共同體"和建設"一帶一路"的倡議,踐行"中國將努力讓疫苗成為各國人民用得上、用得起的公共產品"的大國擔當,立足當下烏茲別克斯坦及中亞地區疫苗產業現狀、遠未被滿足的疫苗市場需求,綠葉生命科學集團與烏茲別克斯坦共和國創新發展部將共同致力于建立"烏茲別克斯坦創新疫苗中心",具體包括疫苗中心建設、疫苗研發生產、人員培訓、技術交流、產品推廣等。雙方將烏茲別克斯坦確定為優先合作區域,同時促進上合組織成員國之間的合作,加強信息交流和業務合作;并建立健全長期聯系機制,開展多種形式的交流活動。
烏茲別克斯坦共和國創新發展部部長伊布洛西姆·阿卜杜拉赫莫諾夫表示:"我們很高興與綠葉生命科學集團簽署這項合作備忘錄。烏茲別克斯坦與中國在包括抗擊疫情等多個領域開展深度合作,不僅為我們的民眾健康謀福祉,亦有機會帶動我們的疫苗技術和產業發展,推動我們的醫學進步、并加深兩國友誼。期待此次合作的圓滿成功。"
綠葉生命科學集團董事局主席劉殿波表示:"綠葉生命科學集團作為一家旗下擁有制藥、疫苗、醫療、診斷等生命科學業務板塊,產品及服務網絡分布全球80多個國家和地區的國際化企業,我們非常榮幸能夠參與到該項目。除了疫苗,我們也期待未來能夠以優質創新的藥品、價值導向的醫療服務和精準高效的診斷技術造福烏茲別克斯坦人民,為中烏的合作發展貢獻一份力量。"
優替德隆是華昊中天自主研發的國內首個埃博霉素類抗腫瘤創新藥,于2021年獲得國家藥品監督管理局批準上市,用于治療復發或轉移性晚期乳腺癌。目前該藥物已被納入 《CSCO 乳腺癌診療指南(2021版)》以及《中國晚期乳腺癌規范診療指南(2020版)》。此外,與優替德隆多項新適應癥相關的臨床研究也在進行中,涉及非小細胞肺癌、消化道腫瘤、婦科腫瘤、頭頸部腫瘤等多種晚期實體腫瘤的治療。
“作為國內首個且唯一獲批的埃博霉素類抗腫瘤藥物,優替德隆打破了我國長期以來晚期乳腺癌治療的瓶頸,實現了乳腺癌化療領域近三十年來的新突破。”華昊中天董事長唐莉博士表示:“很高興與綠葉制藥就優替德隆的市場推廣開展合作。綠葉制藥在腫瘤治療領域深耕多年,擁有廣泛的市場覆蓋和渠道資源,我們期待雙方共同打造優勢互補、協同發展的共贏合作模式,助力優替德隆惠及更多患者。”
“秉承‘以患者為中心’的理念,綠葉制藥致力于為解決患者未滿足的健康需求而不懈努力。腫瘤領域是我們長期布局的戰略領域之一,我們期待為優替德隆帶來更具廣度和深度的覆蓋,切實幫助更多的腫瘤患者。”綠葉制藥集團總裁楊榮兵表示:“優替德隆也是綠葉制藥在腫瘤領域產品組合的有益補充,將持續強化我們在該領域的戰略優勢。”
]]>作為國內最權威和最具影響力的雇主品牌評選項目之一,此次評選有來自各行業約200家領先企業參與評選。怡安臻選評委團對所有參選企業的五大員工健康維度(身體健康、心理健康、財富健康、社交健康、職業發展健康)的277個細項以及參選企業提供的實踐案例進行綜合打分,評選最終勝出者。此次評選,綠葉生命科學集團能夠從跨越多個行業的兩百余家知名企業中脫穎而出,是對其多年來高度關注員工健康所取得成果的充分肯定和認可。
綠葉生命科學集團作為一家專注于生命科學發展與創新的企業,在堅持“以患者為中心”發展業務的同時,也將“成就員工”作為企業經營理念之一,倡導“快樂工作,健康生活”,并充分利用自身的資源優勢以及合作伙伴的專業力量,為員工健康保駕護航。
為提升員工的健康保障,綠葉生命科學集團為員工設計了完善的薪酬福利體系,包括在國家規定的保險計劃以外,對員工現有的商業和醫療保險計劃不斷優化;同時依托集團下屬醫療機構的優勢,加強員工健康篩查,防患于未然,降低健康風險。此外,集團還充分利用精神健康業務板塊的資源優勢,通過心理健康講座、員工心理援助熱線等,幫助員工解決在職場和生活中遇到的心理困擾。
在企業文化建設與員工溝通工作方面,綠葉生命科學集團在管理文化、歸屬認同、學習分享、業務激勵、雇主品牌、創新傳播等六大板塊搭建系統落地項目,通過積極推進集團全球社交傳播渠道優化整合、開展全球聯動的企業文化活動、提升企業領導人與全球員工溝通質量等,營造多樣化和包容的企業文化氛圍,傳遞企業正能量,在改善員工社交健康的同時,提升全球員工士氣與凝聚力。
綠葉生命科學集團副總裁李莉表示,“員工是企業最寶貴的財富,綠葉生命科學長期致力于發掘和培養優秀的人才,為他們打造廣闊的發展空間和成長平臺,并從公司角度關心員工的健康,制定健康戰略,搭建健康體系,打造健康項目,傳遞健康文化,全方位保障員工健康。”
與此同時,綠葉生命科學還將員工全面健康和“健康中國”戰略、“共同富裕”奮斗目標結合到了一起,在賦予了員工健康更豐富含義的同時,也為社會和企業的可持續發展創造價值。
五大主題10項行動 可持續助力共同富裕探索與實踐
綠葉生命科學集團品牌與公共關系副總裁楊亮出席了頒獎典禮,并發表主題演講。楊亮系統闡述了綠葉生命科學圍繞“1、支持科研創新,深化高校合作;2、幫扶小微企業,促進產業升級;3、振興鄉村經濟,帶動農民增收;4、關注基層健康,共享醫療資源;5、關愛弱勢群體,推動文體事業”五大主題,通過持續開展的十項卓有成效的公益行動,在助力共同富裕方面進行的探索與實踐,在會場引起了熱烈反響。
楊亮特別提到,綠葉生命科學一直在嘗試更具可持續性的公益形式。通過高校聯合辦學、科技人才基金與獎勵、國際生物科技園、現代農業產業園、患者援助、基層義診、康復關懷、助學貧困學生、扶貧困難群眾、公共文體事業等項目,綠葉生命科學集團努力結合企業的優勢技術與資源、借助商業能力創新公益方法,運用商業邏輯更有效率地解決社會問題,從而讓公益走得更遠,讓企業在創造經濟價值的同時,也創造了巨大的社會福祉。
責任引領,逐夢前行
作為一家具有高度社會責任感的企業,綠葉生命科學集團在全球化的發展過程中,始終秉承“商業價值和社會價值并重”的理念,堅持綠色生產、可持續供應鏈管理,聚焦鼓勵創新、援助患者、支持教育、慈善捐贈回饋社會。
2021(第四屆)社會責任大會以“聚合力 創未來”為主題,圍繞公益慈善、社會責任管理等話題,展開多方對話,聚焦責任創新和發展。現場參會的有來自公益組織、基金會、部委領導、商界領袖、權威媒體、學術機構、公眾人物等各領域嘉賓,大家探討公益領域的熱點議題,倡導可持續發展理念,向社會大眾持續傳遞企業品牌公益的價值。
隨著藥物生產領域的技術不斷革新,數字化轉型逐漸在生物制藥產業發展中扮演越來越重要的角色。博安生物將加快建設“數字化工廠”,通過構建智能化的數據環境,推進生產數據貫通化、制造柔性化、管理智能化,從而進一步提升其生產效能,提高生產操作的靈活性,優化生產成本的同時保障品質和患者安全。
為了加速實現這一目標,博安生物與默克在如下領域建立戰略合作伙伴關系,持續展開全面、深入合作,包括:Bio4C? ProcessPad數據收集可視化和分析軟件平臺以及抗體強化工藝、連續工藝過程設備、經濟適用型培養基開發、成本分析以及工藝優化方案、耗材(包括上市前原型產品)供應預測及按需分批到貨等多個領域。
博安生物是國內首家引入Bio4C? ProcessPad數字化平臺的制藥公司。Bio4C? ProcessPad是默克研發的數據可視化、工藝監控和分析的平臺,支持生物工藝生命周期管理、報告、調查和持續工藝驗證。通過該系統,博安生物的生產體系能夠實現更有效地控制、連接、收集和協作,將過程數據智能組合到單個的、關聯的、整合的數據源中,實現數據采集、聚合和流程分析,并促進實時工藝監控、偏差調查等關鍵活動的高效開展和管理。
“博安生物致力于為中國乃至全球患者提供高品質創新生物藥,其生產基地在建設之初即引進國際先進的設計理念并持續開展生產工藝的創新升級,”博安生物首席執行官姜華表示:“我們期待通過默克的專業技術賦能博安生物的‘未來數字化工廠’,助推我們實現更高效、更高產能、更優產品質量以及更大程度的造福病患。”
“生物制藥的智能化是未來的趨勢和方向。通過建設‘未來數字化工廠’,可以打破各生產模塊間的信息孤島,實現對數據的高效分析和利用,將進一步提高博安生物的生產效率和流程經濟性,加強對生物藥工藝過程的深度理解與提升,持續保障產品的高質量水平。未來,伴隨著預防性維護和連續、實時的生物工藝生產策略支持,數字化文檔和數據分析將實現更快的產業化過程,以及更精準和高效的自動化控制。”博安生物制造與供應鏈副總裁王廣泉博士表示。
“我們很高興能夠與博安生物達成戰略合作。博安生物是國內領先的生物制藥公司,具備完整的從抗體發現到產業化的全整合型產業鏈。我們期待與其開展更全面深度的合作,助力其數字化進程的加快推進,實現創新資源的高效配置和高質量發展。”默克生命科學生物工藝中國副總裁麥軒愷(Ian Carmichael)博士表示。
博安生物致力于成為“全球領先的國際化生物技術創新企業”,在中國、美國及歐盟市場從事生物產品開發。公司已建有2.5萬平方米的現代化生產基地,另有4萬平方米的新生產線及立體倉庫處于建設階段,預計先后于2022年、2023年投入使用。所有生產線均按照中國、美國、歐洲等國際GMP標準設計與建設,以確保為各地患者提供全球標準的高品質生物藥。
]]>《中國心血管健康與疾病報告2020》[1]顯示:2018年,心血管病死亡占我國城鄉居民總死亡原因的首位;該報告估計,我國現有約3.3億人患有心血管疾病,隨著罹患高血壓、血脂異常、糖尿病和肥胖的絕對人數不斷攀升,我國心血管病的發病率和死亡率將進一步推高。積極有效地進行血脂管理對于心血管疾病的一級預防、降低心血管疾病的相關死亡率尤其重要。
血脂康®膠囊60粒裝的推出,能夠有效減少患者的購藥次數,增加其長期用藥管理的便利性和治療依從性,尤其能為廣大基層患者帶來福音;同時也利于醫生根據患者實際情況提供更適合的個體化用藥方案,并可通過降低續方開藥的頻率,在一定程度上降低醫療資源負荷。結合已上市的12粒裝和24粒裝,血脂康®膠囊將以三種不同的包裝規格,滿足多元化的臨床需求。
血脂康®膠囊由綠葉制藥集團自主研發,是目前國內唯一有臨床硬終點獲益的天然調脂藥物,并已在美國完成II期臨床研究,為國內外公認的調脂藥品牌。多項大型臨床循證醫學研究均證實:血脂康®能夠抑制膽固醇合成,并顯著降低冠心病患者總死亡率、冠心病死亡率以及心血管事件發生率,不良反應少。
基于明確的調脂療效和安全性,血脂康®作為一級預防用藥,被寫入首部《中國心血管疾病一級預防指南》;該藥物還被納入《國家基層高血壓防治管理指南(2020版)》、《中國成人血脂異常防治指南(2016年修訂版)》等多部心血管領域權威指南。截至2020年,血脂康®也是唯一被心血管領域多部權威指南收錄的天然調脂藥,并被納入最新版《國家基本醫療保險和工傷保險藥品目錄》和《國家基本藥物目錄》。
為了推動該藥物惠及更多患者,2019年1月,綠葉制藥將血脂康®膠囊在中國大陸地區的推廣權獨家授予阿斯利康,此舉開創了大型跨國藥企推廣中國高品質天然藥物的先河。過去兩年來,隨著雙方合作的不斷深入,使得該藥物在各地區的市場覆蓋、以及包括醫院及藥店在內的渠道拓展等方面均取得積極進展,助力廣大患者的用藥可及性得到顯著提升。
“血脂康®膠囊上市二十多年來,已積累了豐富的循證證據,擁有良好的臨床用藥基礎,療效和安全性得到醫生和患者的廣泛認可。”綠葉制藥集團管理層表示:“此次血脂康®膠囊60粒新包裝的上市,是對原有包裝規格的有益補充。我們期待通過該產品,更好地服務于患者的臨床用藥需求,助力其治療依從性的提升和長期血脂管理。”
[1]《中國心血管健康與疾病報告2020》. 中國循環雜志,2021, 36:562-586.DOI:10.3969/j.issn.1000-3614.2021.06.001. |
]]>
《Antibody Therapeutics》由牛津大學出版社出版,是華人抗體協會旗下一份同行評議專業期刊,關注全球治療性抗體的研究開發和商業化等領域的最新進展。
CEA作為一種常見的廣譜性腫瘤標記物,其在結直腸癌、胃癌、胰腺癌、肺癌、乳腺癌等多種實體瘤中均高表達,且其表達與疾病進展呈相關性。
同時,靶向腫瘤抗原和T細胞CD3的T細胞engager抗體是雙特異抗體研發中最為活躍的領域之一。其不僅可以有效殺傷表達抗原的腫瘤細胞,還能增加免疫細胞在腫瘤組織的浸潤,刺激冷腫瘤成為熱腫瘤,如果結合使用免疫抑制劑,則可提高其對冷腫瘤的治療療效。
然而,當前CD3抗體的開發依舊面臨不少挑戰,包括CD3高親和力造成的細胞因子風暴的毒性,早期上市抗體在體內的半衰期過短等問題。
博安生物位于美國波士頓的研發團隊采用了一種新型的butterfly蝴蝶抗體結構,保留了Fc區域;證明了此結構展示出對腫瘤抗原的二價結合,對T細胞CD3的單價結合;團隊還針對行業痛點對CD3的親和力做了大幅度的下調。
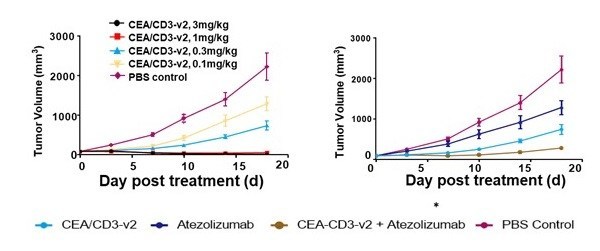
論文研究結果顯示:
- BA1202的CD3親和力弱化后,不影響對靶細胞的殺傷作用,但細胞因子分泌大為降低,繼而降低毒性;
- 在結直腸癌小鼠模型中顯示出完全抑制腫瘤的良好藥效, 同時呈現明顯的劑量相關性, 在0.1 mg/kg 即有抑瘤效果;
- 相較于同類可比的在研CEA/CD3抗體藥物, BA1202顯示出更強的體外活力和體內藥效(數據尚未公開);
- 與免疫抑制劑antiPD-L1 Atezolizumab有協同效應, 并伴隨T細胞腫瘤浸潤的大幅度增加;
- BA1202抗體顯示良好的特異性,只結合腫瘤, 不結合正常組織。
該研究論文的通訊作者、博安生物抗體發現部及細胞治療研究部副總裁周立博士表示:“我們建立了一個獨特的CD3雙特異抗體平臺,通過該平臺研發的CEA-CD3雙特異抗體與同類在研產品相比,進一步增強了藥效,同時降低了多種細胞因子的釋放,具有差異化優勢。我們將加快推動該產品進入臨床,以期盡早為實體瘤患者提供有效、安全的創新治療方案。”
博安生物在美國波士頓的研發中心聚焦前沿新技術和進展,專注于抗體開發和細胞治療,現已擁有獨特的雙特異T-cell engager抗體平臺和CAR-T非病毒載體平臺。其中,雙特異T-cell engager抗體平臺已申請專利保護,CAR-T非病毒載體平臺開發的細胞治療產品采用非病毒載體制備晚期實體瘤CAR-T, 并布局新一代通用型及可調控CAR-T,快速研發更安全、有效、可負擔的CAR-T產品。
]]>南京金陵醫院秦叔逵教授、山東省腫瘤醫院于金明院士、哈爾濱血液病腫瘤研究所馬軍教授、中國醫學科學院腫瘤醫院石遠凱教授、北京大學國際醫院梁軍教授、解放軍總醫院江澤飛教授、天津腫瘤醫院郝繼輝教授、北京康盟慈善基金會副理事長吳先飛等上百名專家學者及嘉賓出席了上市會活動,與綠葉制藥集團總裁楊榮兵、綠葉制藥(中國)總裁謝文敏、博安生物首席執行官姜華、博安生物研發總裁兼首席運營官竇昌林博士等企業代表共同見證了這一里程碑時刻。
博優諾®與原研藥同等療效,貝伐珠單抗為多瘤種治療“金標準”
貝伐珠單抗注射液是抗腫瘤血管生成的代表性藥物,其原研藥在全球范圍內獲批用于治療非小細胞肺癌、結直腸癌、膠質母細胞瘤、腎細胞癌、宮頸癌、卵巢癌等多種實體瘤,顯著的療效和良好的安全性已在長期臨床應用中得到醫生和患者的廣泛認可。
博優諾®作為貝伐珠單抗的生物類似藥,在與原研藥的兩項關鍵臨床研究中進行了頭對頭比對,即健康志愿者中的藥代動力學PK比對研究,轉移性或復發性非鱗狀細胞非小細胞肺癌患者中的療效、安全性及免疫原性比對研究。兩項研究均達到等效標準,證明博優諾®與原研貝伐珠單抗PK特征高度相似,療效等效、安全性相似、免疫原性相似。
“在臨床研究中,博優諾®展現出良好的療效和安全性,與原研藥高度相似。”博優諾®III期臨床試驗的主要研究者、中國癌癥基金會理事長、中國醫學科學院腫瘤醫院石遠凱教授表示:“貝伐珠單抗生物類似藥的研發,是滿足患者臨床需求的重要途徑。博優諾®的上市將為需要抗血管生成治療的廣大患者帶來新的治療選擇,滿足更多用藥所需。”
回顧博優諾®的研發歷程,該項目負責人、博安生物研發總裁兼首席運營官竇昌林博士表示:“博優諾®遵循嚴謹的生物類似藥研發路徑,通過藥學、非臨床、臨床研究等各個環節,以完整的證據鏈全面證明了該產品在一級和高級結構、理化特性、純度、生物學活性、非臨床藥代動力學、藥效學、毒理學特征、臨床藥代動力學特征以及臨床有效性和安全性等方面與原研藥的一致性。通過博優諾®的上市,我們進一步夯實了在生物藥領域的研發和生產實力,期待通過持續創新,為患者提供更多高品質、可負擔的生物藥。”
救助項目同步啟動,減輕患者治療負擔
近年來,我國癌癥發病人數不斷攀升。世界衛生組織國際癌癥研究機構(IARC)數據顯示:2020年我國新發癌癥人數達457萬人,占全球新發癌癥人數的23.7%,居全球首位;其中肺癌、結直腸癌位列我國癌癥新發病率前兩位,2020年新發病例數分別達到約82萬人和56萬人。
抗血管生成藥物是惡性腫瘤治療中不可或缺的手段之一。在非小細胞肺癌領域,貝伐珠單抗可與化療、靶向治療、免疫治療三種治療方案聯合使用;在結直腸癌領域,貝伐珠單抗聯合化療可用于轉移性結直腸癌的一線、二線、跨線、三線和轉化治療。此外,貝伐珠單抗聯合包括紫杉醇脂質體在內的紫杉醇類化療藥物也具有獨特的優勢。
北京大學國際醫院梁軍教授表示:“貝伐珠單抗能夠與諸多其他治療方式聯用,其組合應用的治療模式具備眾多優勢,在非小細胞肺癌、結直腸癌等惡性腫瘤治療中持續發揮出重要作用。基于這些疾病領域大量未滿足的治療需求,期待博優諾®能夠惠及更多患者,幫助他們提高生存質量并延長生命。”
為進一步提升患者的治療可及性及可負擔性,博安生物攜手北京康盟慈善基金會共同啟動了“博優諾®患者救助項目”。該項目將在全國范圍內開展,旨在對更多需要幫助的患者提供藥品救助,切實減輕其經濟負擔。博安生物將向北京康盟慈善基金會無償捐贈治療藥物博優諾®,由該基金會負責項目的具體管理和運作,向符合項目申請條件的患者提供慈善藥品。
北京康盟慈善基金會副理事長吳先飛表示:“感謝博安生物的鼎力支持,希望通過‘博優諾®患者救助項目’,能使更多患者及時獲得規范化、持續性的治療,減輕他們的經濟負擔,提高生存質量,與患者共渡難關。”
多方合力加速藥品可及,立足創新服務全球患者
博優諾®是博安生物的首個生物抗體藥物。自獲得上市批準后,為盡快投入臨床使用,從宣布獲批到首批發貨,博優諾®僅用了10天時間,并相繼在全國多地開出首張處方。
在患者覆蓋方面,博安生物通過自有的業務團隊、商業化資源和網絡,積極提升核心市場的患者用藥可及性;同時,通過授權阿斯利康在中國21個省市及自治區的縣域地區獨家推廣博優諾®,致力于滿足更多廣闊市場的患者治療需求。
“我們已從生產、準入、銷售等各個環節做好積極準備,并與各方合作伙伴通力協作,為服務患者所需不懈努力。”博安生物首席執行官姜華表示:“通過博優諾®的上市,博安生物打通了從研發、臨床、生產到商業運營的各個環節,構建了我們在生物藥領域完整的全產業鏈能力,也為我們后續產品管線的高效推進打下了堅實的基礎。”
目前,博安生物已開發了10多個擁有國際知識產權保護的創新抗體、以及包括博優諾®在內的8個生物類似藥,并圍繞細胞治療等前沿技術領域積極布局。
“生物藥是綠葉制藥集團當下及未來發展的戰略領域之一。我們正在通過博安生物加速推進生物藥業務的全球布局,期待以更多高品質的創新產品,為中國乃至全球患者服務。”綠葉制藥集團總裁楊榮兵總結道。
]]>此次合作的達成基于雙方在中國各級市場的資源互為整合:博安生物通過自有的業務團隊、商業化資源和網絡,積極提升核心市場的患者用藥可及性;同時,為了進一步加大博優諾®的患者覆蓋,博安生物聯合阿斯利康,借助其在中國縣域深耕多年所積累的廣闊的市場覆蓋及渠道拓展能力,推動該產品進一步惠及更多患者人群。
博優諾®是由博安生物自主開發的生物抗體藥物。該產品于近期獲得中國國家藥品監督管理局的上市批準,用于治療晚期、轉移性或復發性非小細胞肺癌和轉移性結直腸癌。自獲得上市批準后,為了盡快幫助更多患者實現臨床獲益,從宣布獲批到首批發貨,博優諾®僅用了10天時間,并已相繼在全國多地開出首張處方。
博安生物首席執行官姜華表示:“阿斯利康在腫瘤治療領域和縣域市場深耕多年,擁有廣泛的創新資源和市場覆蓋。此次與阿斯利康的戰略合作是對博優諾®商業化網絡的重要補充和拓展。未來,我們將在多層級市場發揮各自的渠道優勢和患者人群覆蓋優勢,并積極探討海外市場的合作機會,為更多患者提供高品質、可負擔的用藥選擇。”
阿斯利康全球執行副總裁、國際業務及中國總裁王磊表示:“一直以來,阿斯利康秉承‘以患者為中心’的理念,積極攜手社會各方資源,致力于讓更多縣域患者受益于先進的創新治療以及全病程、全生命周期的解決方案。博安生物是具備全產業鏈能力的綜合型生物制藥公司,擁有優秀的研發和生產團隊,是中國領先的本土企業,我們期待未來雙方緊密協作,將更多創新解決方案帶給縣域患者,為滿足中國不斷增長的健康需求而不懈努力。”
]]>博優諾®用于治療晚期、轉移性或復發性非小細胞肺癌和轉移性結直腸癌。該產品獲得上市批準后,為了盡快幫助更多患者實現臨床獲益,滿足治療所需,博安生物的所有團隊齊心協力,克服種種困難與挑戰,從生產、質檢、物流到營運等各個環節高效聯動,彰顯了公司高效的運營管理能力以及“以患者為中心”的使命與責任。
貝伐珠單抗注射液作為抗腫瘤血管生成的代表性藥物,已被納入多種惡性腫瘤治療指南全球推薦的標準方案。作為安維汀®(Avastin®)的生物類似藥,博優諾®經與安維汀®的頭對頭比對,被證明與后者的藥代動力學(PK)特征相似、臨床療效具有等效性,安全性、免疫原性高度相似。
“我們期待博優諾®能夠惠及更多需要抗血管生成治療的患者,為病患提供高品質的治療新選擇。公司已從生產、準入、銷售等各個環節做好積極準備,為持續提升用藥可及性,滿足患者需求不懈努力。”博安生物首席執行官姜華表示:“博優諾®是博安生物首個實現商業化的生物藥,未來我們也將推動更多創新產品的加速上市,為中國乃至全球患者服務。”
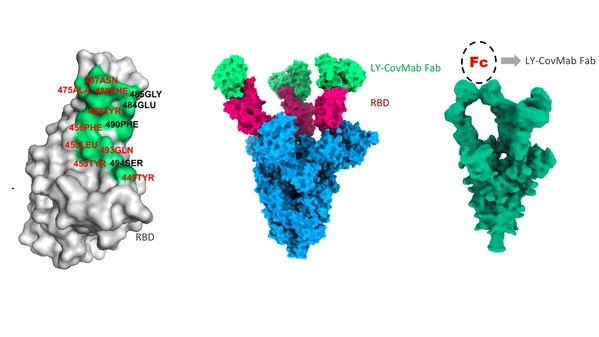
]]>嚴重急性呼吸系統綜合征冠狀病毒2(SARS-CoV-2)造成新型冠狀病毒肺炎大流行,對全球人民健康以及經濟帶來巨大威脅。LY-CovMab是一款重組全人源單克隆中和抗體,以高親和力特異性結合SARS-CoV-2表面刺突蛋白受體結構域(RBD),并能有效阻斷病毒與宿主細胞表面受體血管緊張素轉換酶2(ACE2)的結合。
研究結果顯示:LY-CovMab在假病毒和新冠病毒中分別展示了優異的中和活性。
- 引入LY-CovMab的FALA突變消除了與Fc受體或補體受體的結合,以避免抗病毒抗體常伴隨的ADE效應(抗體依賴的增強作用)的發生;
- LY-CovMab表現出較長的半衰期,在小鼠和恒河猴體內的末端消除半衰期分別為9.5天和9.3天;
- LY-CovMab在馴化的SARS-CoV-2株感染的小鼠新冠模型中顯示出顯著的治療效果。20 mg/kg LY-CovMab在病毒感染后第3天能夠將肺組織的病毒載量相比安慰劑組降低104.5倍,同時,LY-CovMab也抑制了病毒引起的肺部間質性肺炎;
- 基于冷凍電鏡(cryo-EM)進行的結構分析表明,LY-CovMab在SARS-CoV-2表面刺突受體結構域上的表位與ACE2重合。LY-CovMab IgG/Fab與表面刺突蛋白復合體的3D結構顯示,LY-CovMab Fab形式能同時結合一個SARS-CoV-2刺突蛋白三聚體上的所有三個RBD,其中一個RBD處于關閉狀態、另外2個RBD處于開發狀態;LY-CovMab 完整IgG形式也能同時結合三聚體上的所有三個RBD,但三個RBD都處于開發狀態,這提示LY-CovMab 以IgG形式結合開發狀態的RBD后促進了相鄰RBD構想的改變。另外,3D結構顯示一個LY-CovMab/IgG 分子很可能同時結合一個三聚體上的2個RBD。這些屬性綜合起來賦予了抗體優異的中和潛力。
該研究論文的通訊作者、博安生物研發總裁兼首席運營官竇昌林博士表示:“以上結果顯示LY-CovMab在抑制新冠病毒中的良好效果,具有較高的潛在臨床價值。近期未發表研究結果顯示,LY-CovMab對發生頻率較高的起源于英國的突變株B.1.1.7依然有較好的中和活性。”
博安生物是國內首批研發新冠抗體的創新生物藥企之一。在新冠抗體開發過程中,博安生物顯示出高效的抗體開發能力 -- 借助其完善的全人抗體轉基因和小鼠噬菌體展示技術平臺,從自有的全人抗體轉基因小鼠BA-huMab篩選出的抗體,無需經過傳統的抗體人源化過程,從Spike蛋白免疫到中和抗體獲得僅用了40余天,大大提高了抗體開發速度。此外,LY-CovMab采用特殊的Fc序列設計,可避免抗體依賴的增強作用發生,避免為病毒所用加重細胞因子風暴,從而提高了抗體藥物的安全性和臨床的成功率。
目前,LY-CovMab已在中國處于I期臨床試驗的收尾階段。此前該在研產品已被納入科技部《新型冠狀病毒中和抗體產品研發應急項目》。博安生物亦將在美國啟動臨床研究,推進其全球上市進程。
]]>瑞欣妥®是注射用緩釋微球制劑,基于綠葉制藥全球領先的微球技術平臺開發。作為中國首個具有自主知識產權并開展全球注冊的創新微球制劑,同時也是國內首個自主研發的第二代抗精神病藥長效針劑,瑞欣妥®的上市為我國約1000萬名精神分裂癥患者的重返社會帶來新希望。
依從性低導致病情反復,成精神分裂癥治療主要痛點
精神分裂癥是一種反復發作的慢性遷延性疾病。因患者中斷治療或自行減藥而導致的病情反復是當下精神分裂癥治療的主要難點。數據顯示:首次發作的患者有60%服藥依從性差,5年內的復發率超過80%。多次復發導致病程遷延、增加治療難度、也使治療費用大幅增加[1]。
“精神分裂癥的治療理念已從控制癥狀轉變為改善認知、促進康復,最終使患者回歸社會。在此過程中,提升患者依從性以預防復發,是精神分裂癥的治療關鍵。”上海交通大學醫學院附屬精神衛生中心主任醫師蔡軍教授表示:“抗精神病藥長效針劑相比口服制劑可顯著改善患者依從性,是預防復發的重要治療策略。”
目前,《抗精神病藥長效針劑治療精神分裂癥的專家共識》已將第二代抗精神病藥長效針劑作為急性期和維持期精神分裂癥患者的一線治療策略[2]。從全球治療理念和趨勢來看,長效制劑的使用也是未來精神分裂癥治療的主要手段之一。蔡軍教授指出:“基于精神分裂癥高復發的疾病特點,我們提倡在病程的各個階段盡早啟用長效針劑的治療。作為我國首個自主研發的第二代抗精神病藥長效針劑,瑞欣妥®在現有市售長效針劑基礎上進一步改良升級,適用于精神分裂癥的全病程治療,為患者提供新的治療選擇。”
創新微球制劑,提升精神分裂癥治療安全性和依從性
瑞欣妥®每兩周肌肉注射一次,可顯著改善口服抗精神病藥物在精神分裂癥患者中普遍存在的用藥依從性。
與口服制劑相比,瑞欣妥®的用藥頻率顯著降低,可有效改善患者漏服、忘服的用藥情況。此外,瑞欣妥®在體內的血藥濃度平穩,相比口服制劑縮小了血藥濃度波峰與波谷的差異,有助于降低劑量依賴性副作用的發生風險,提升了患者的用藥安全性。
“多數精神分裂癥患者難以堅持每天服用口服藥物,其中一部分是因為無法耐受藥物的不良反應而停止用藥,這也是服藥依從性差的原因。瑞欣妥®的給藥方式和平穩持久的血藥濃度可更好地保障患者長期有效用藥。”蘇州市廣濟醫院主任醫師梅其一教授指出。
此外,與另一種市售藥物相比,首次注射瑞欣妥®后無需同時補充口服制劑,且比該市售藥物能更快達到穩態血藥濃度。
“瑞欣妥®注射后起效迅速,可快速控制患者精神病性癥狀,并在停藥后快速清除,更利于醫生根據病情快速調整治療方案。”梅其一教授補充道:“很高興看到我國在精神分裂癥治療領域實現制劑創新,為患者提供了更有臨床優勢的新藥。相信隨著瑞欣妥®的上市,能夠為更多患者的預后改善、回歸社會帶來福音。”
建設全球領先微球技術平臺,持續改善患者臨床獲益
“制劑創新的目的在于解決未滿足的臨床需求,涵蓋療效、順應性、副作用等各方面。我們關注患者的體驗和需求,致力于通過提供有差異的、具有臨床價值的創新產品,為減輕患者的疾病負擔、改善患者的臨床獲益而不懈努力。”綠葉制藥集團總裁楊榮兵表示。
微球制劑作為新型高端制劑的代表之一,針對臨床需求設計釋放速度和周期,可持續釋放藥物一周至數月,并達到平穩釋放藥物,提高療效,降低副作用的目的。作為一種復雜制劑,微球制劑的研發、生產難度大、技術壁壘高,該技術主要被幾家國外企業所掌握。
瑞欣妥®的上市,意味著綠葉制藥成功打破了海外技術的長期壟斷,成為國內少數已掌握微球制劑關鍵工藝的企業。經過十多年的不懈努力,綠葉制藥已建立起包括高載藥量低突釋微球制備技術、長效緩釋制劑體內外釋放相關性評價、微球產業化制備技術及設備等核心關鍵技術的平臺建設,形成了在該領域的國際競爭力。特別是其微球技術平臺的工業化研究水平已處于國際領先地位,中試的技術設備、制備工藝全部自行研發。
微球技術平臺的研發和產業化攻堅突破后,首個微球產品瑞欣妥®的商業化進程也在不斷提速。2021年1月12日獲上市批準后僅40多天,瑞欣妥®已開始面向全國多個省市供藥。此外,為惠及更多全球患者,瑞欣妥®的全球注冊申報工作也在同步開展,目前已在美國進入新藥上市申請階段,并在歐洲開展關鍵臨床研究。
“瑞欣妥®的上市意義重大,它印證了我們長期以來致力于圍繞患者所需,提供創新治療方案的這一堅定承諾;同時也是我們的微球技術平臺實現從0到1的突破性成果,推動該平臺后續更多的創新微球制劑加速上市,為更多患者服務。”楊榮兵表示。
除了已上市的瑞欣妥®,綠葉制藥的創新微球平臺將繼續發揮核心技術優勢,在腫瘤和中樞神經等重大疾病領域深度布局,一系列處于不同研發階段的微球產品包括:治療帕金森病的注射用羅替戈汀緩釋微球(LY03003)、治療前列腺癌、乳腺癌等性激素依賴性疾病的注射用醋酸戈舍瑞林緩釋微球(LY01005)、治療帕金森病、不寧腿綜合癥的 LY03009等優質創新藥物。后續新藥將與瑞欣妥®形成豐富的產品組合,發揮公司在這一技術領域的優勢力量,為患者帶來高品質的治療新選擇。
[1] 趙靖平, 施慎遜. 中國精神分裂癥防治指南[M].2 版. 北京:中華醫學電子音像出版社, 2015.
[2] 司天梅, 李凌江. 抗精神病藥長效針劑治療精神分裂癥的專家共識. 中華精神科雜志2020年4月第53卷第2期.
根據協議,Italfarmaco獲得在德國、意大利、葡萄牙和希臘商業化利斯的明多日透皮貼劑的獨家權利。Italfarmaco也將擁有在智利和越南商業化該產品的優先權利。Italfarmaco將在該協議簽署后向綠葉制藥支付首付款,并在達到若干銷售里程碑時支付額外款項。綠葉制藥也將獲得來自Italfarmaco的特許權使用費。
Italfarmaco集團業務及產品開發副總裁Antonio Nardi表示:“阿爾茨海默病是一種神經退行性疾病,患者數量不斷增加,而現有治療選擇卻很有限。我們非常樂意與綠葉制藥攜手合作,將這一給藥便捷的創新產品帶給廣大患者。我們也期待在自身的研發專長之上,進一步構建以神經系統疾病為主的產品組合,為一線臨床醫生提供治療神經退行性疾病的更多選擇。”
綠葉制藥(瑞士)總經理Bruno Delie表示:“與Italfarmaco的攜手合作是我們服務于歐洲市場,致力于解決當地老年患者未滿足的治療需求的一項重要里程碑。憑借Italfarmaco在中樞神經疾病領域積累的豐富經驗以及強大的業務運營體系,相信能夠盡快將這一新的治療選擇帶給當地患者。我們致力于為改善癡呆癥患者及其家庭、朋友和照護者的生活質量不懈努力。”
隨著患者數量的日益攀升,阿爾茨海默病已成為全球范圍的一大公共健康挑戰。《2018年世界阿爾茨海默病報告》顯示:每3秒鐘,全球就有一名癡呆癥患者產生。2018年,全球癡呆癥患者約為5000萬人;預計到2030年,這一數字將達到8200萬[i]。該疾病治療領域的新藥開發挑戰重重,利斯的明是目前治療阿爾茨海默病相關癡呆癥的一線用藥,在全球市場銷售。
[i]《2018年世界阿爾茨海默病報告》, 國際阿爾茨海默病協會, 2018年9月, |
中國阿爾茨海默病患者群體龐大,照護壓力大
阿爾茨海默病已成為當下乃至未來人類所面臨的最大的全球公共健康和社會保健挑戰之一。隨著我國人口老齡化趨勢加快以及主要心血管疾病及相關因素流行趨勢增加等多種因素的影響,阿爾茨海默病的患病率和患者數量也呈逐年遞增的趨勢。據預測,2020年我國阿爾茨海默病患者約有900萬,2050年將達到2100萬[i]。
面對日益龐大的患者群體,一方面,阿爾茨海默病造成的記憶障礙、認知異常等問題給老人的生活、健康造成嚴重威脅;另一方面,由于基本生活自理能力的下降,老人需要長期、全天候的家庭照護和社會保健服務,也給家庭和社會帶來沉重的經濟和照護負擔。國內一項調查顯示:照護者中約57%為全天陪同,將近2/3的照護者表示感到輕度及以上的負擔[ii]。
“阿爾茨海默病是最常見的不可逆的神經退行性疾病,及早干預對于改善或延緩病情發展至關重要。”上海交通大學醫學院附屬精神衛生中心老年病診治中心主任肖世富指出:“但在臨床診療實踐中,由于認識不足、病恥感、患者失智、失能等原因,導致就診晚、治療率低、停藥率高,治療依從性差,往往無法獲得最佳療效。安全、有效的治療方案,能夠明顯改善病情,減輕照料負擔,提高患者和家屬的生活質量,從而減輕疾病負擔。”
金斯明®提升阿爾茨海默病治療安全性、依從性
利斯的明是目前治療輕、中度阿爾茨海默病的一線用藥,獲得多國權威指南推薦。金斯明®改變給藥途徑,經皮膚給藥,使藥物透過表皮由真皮內的血管吸收進入全身血液循環,達到有效血藥濃度,可明顯改善阿爾茨海默病患者認知功能和總體功能,且與利斯的明口服制劑療效相當。
與口服制劑相比,金斯明®具有更好的安全性和依從性。在安全性方面,利斯的明透皮貼劑既不經肝臟CYP450酶代謝,也不加重腎臟負擔;并可減少全身不良反應事件、尤其是胃腸道相關的不良反應。耐受性方面,利斯的明透皮貼劑提供平穩、連續的給藥和持久的治療性血漿藥物濃度,更容易滴定至目標劑量,可使患者盡早開始高劑量用藥治療,有助于延緩病程發展。與此同時,一天一次的貼劑給藥形式,便利性更好,不僅能夠改善患者的用藥依從性,也能減少照料者的用藥管理時間。
中日醫院神經科主任、老年醫學中心執行主任彭丹濤表示:“相較口服制劑,透皮貼劑的載藥量更大,有助于延緩阿爾茨海默病的疾病發展、減輕癥狀。透皮貼劑使用方便,胃腸道不良反應小,對肝臟和腎臟的保護更好,能夠更好的幫助到那些吞咽困難、口服藥物不耐受、肝腎損傷以及有合并疾病、有消化道病史、出現精神癥狀不配合吃藥的患者、以及需要使用大劑量的患者群體。”
德國子公司專注透皮釋藥技術逾20年,后續產品迭代更新
作為金斯明®的上市許可持有人,綠葉制藥集團德國子公司Luye Pharma AG超過20年專注于透皮貼劑的開發和生產,也是歐洲最大的獨立透皮系統制造商之一。憑借在透皮釋藥領域領先的研發實力、一流的制造技術,Luye Pharma AG長期為全球客戶提供透皮貼劑的一站式服務平臺。Luye Pharma AG開發的利斯的明透皮貼劑已于2013年開始,相繼在美國、歐洲11國、泰國等國家和地區上市。
除了一日一貼的金斯明®,Luye Pharma AG還進一步開發了一周給藥兩次的利斯的明透皮貼劑(多日貼),該在研產品在歐洲的上市申請已獲得歐盟主管部門受理,并在國內進入臨床階段,有望為阿爾茨海默病患者帶來更多的治療選擇。
綠葉制藥聚焦中樞神經治療領域,全球布局一系列新藥
包括阿爾茨海默病在內的中樞神經治療領域是綠葉制藥集團長期聚焦的核心戰略領域之一。圍繞這一領域,公司已有一系列創新藥和創新制劑同步在中國和海外市場開發,涵蓋抑郁癥、帕金森病、精神分裂癥、雙相情感障礙等多個病種。
今年1月,治療精神分裂癥的創新制劑瑞欣妥®已在中國獲得上市批準,這也是中國首個自主研發、開展全球注冊的、具有自主知識產權的創新微球制劑。另外,多個新藥已在美國、歐洲等國家和地區進入臨床后期或新藥上市申請階段。
“中樞神經領域相關疾病不僅嚴重困擾患者的身心健康,也給患者的家庭乃至社會造成沉重負擔。”綠葉制藥(中國)總裁謝文敏表示:“中樞神經領域是我們當下及未來的戰略重點,經過多年的布局,我們希望充分發揮在這一領域的優勢力量,為深受疾病困擾的患者帶來高品質的治療新選擇,為人類健康事業貢獻自己的力量!”
]]>
金斯明®用于治療輕、中度阿爾茨海默病,經皮膚每日給藥一次,由Luye Pharma AG的透皮釋藥技術平臺開發。Luye Pharma AG深耕該技術領域超過20年,也是目前歐洲最大的獨立透皮系統制造商之一。
提升阿爾茨海默病治療安全性和依從性,減輕照護壓力
隨著我國人口老齡化趨勢加快以及主要心血管疾病及相關因素流行趨勢增加等多種因素的影響,阿爾茨海默病的患病率和患者數量呈逐年遞增的趨勢。據預測,2020年我國阿爾茨海默病患者約有900萬,2050年將達到2100萬[i]。面對龐大的患者群體,一方面,由阿爾茨海默病所造成的記憶障礙、認知異常等問題,已對大量老年人的生活質量、家庭關系產生嚴重影響;另一方面,擺在阿爾茨海默病患者面前的一大難題是治療藥物的缺乏。阿爾茨海默病被譽為最難突破的領域之一,新藥開發挑戰重重。
利斯的明是目前治療輕、中度阿爾茨海默病的一線用藥,并獲得多國權威指南推薦。金斯明®改變給藥途徑,經皮膚給藥,使藥物透過表皮由真皮內的血管吸收進入全身血液循環,達到有效血藥濃度,可明顯改善阿爾茨海默病患者認知功能和總體功能,且與口服制劑療效相當。此外,與口服制劑相比,金斯明®具有更好的安全性和依從性,也利于減輕照料者的照護壓力。
浙江大學醫學院精神衛生中心老年認知障礙診療中心主任陳斌華教授談到使用透皮貼劑治療阿爾茨海默病的患者獲益時表示:“阿爾茨海默病的促智藥物治療是有效的,雖然不能逆轉疾病進程,但可有效延緩阿爾茨海默病的發展,也可以改善精神行為方面的問題。有相當一部分阿爾茨海默病的老年患者存在治療依從性不佳的問題,很多時候讓老人服藥對于照料者來說較為困難。在阿爾茨海默病的藥物治療方面,透皮貼劑的臨床應用,可以說解決了相當一部分患者治療中的實際困難。”
陳斌華教授指出:幾乎每一個阿爾茨海默病患者都會出現精神行為方面的問題,包括幻覺、妄想等以及行為方面的異常,如不配合藥物治療、沖動傷人、毀物行為等。不配合服藥是其中一個常見的問題。對于這樣的老人,醫藥界一直在尋找解決辦法,于是有了口服液、口服崩解片、透皮貼劑等藥物劑型。相對而言,透皮貼劑更具有優勢,可以由照料者貼在患者不易觸及的身體皮膚上,如肩胛部的皮膚。同時,透皮貼劑由皮膚緩慢穩定吸收,血液里的藥物濃度相對口服藥物更穩定,沒有大起大落,副反應可能更小。也避免了口服藥物可能存在的對胃腸道的刺激作用。
德中兩國團隊緊密協作,金斯明®加快引進中國
金斯明®的產品及其制劑工藝獲得全球多個專利的保護。作為該藥物的上市許可持有人,Luye Pharma AG長期深耕透皮釋藥技術并已形成核心優勢。憑借其在透皮釋藥領域先進的研發實力、一流的制造技術,Luye Pharma AG為全球客戶提供透皮貼劑的一站式服務平臺。從2013年開始,利斯的明透皮貼劑已相繼在北美、歐洲11國、泰國等多個國家和地區成功上市。
為了使這一優質藥物盡快惠及廣大中國阿爾茨海默病患者,綠葉制藥集團的歐洲團隊和中國團隊持續保持緊密協作。收到進口藥品注冊證后,Luye Pharma AG在新冠疫情的挑戰下克服重重困難組織生產,并順利完成歐美追溯碼體系與中國“碼上放心”的對接。疫情不僅影響生產,亦使大部分客運和貨運機停運。兩國供應鏈團隊提前準備各種預案,保障金斯明®產品從德國到中國運輸的無縫銜接。藥品抵達中國后,中國團隊亦爭分奪秒地加速推進這個復雜制劑產品的首次進口藥檢,助力金斯明®早日面向全國供貨,為阿爾茨海默病患者的健康服務。
[i] 中國阿爾茨海默病一級預防指南,中華醫學雜志,2020年9月22日第100卷第35期
血脂康®、力撲素®、貝伐珠單抗注射液(LY01008)是綠葉制藥在心血管及腫瘤領域自主研發的核心產品/在研產品。其中,血脂康®是國內唯一有臨床硬終點獲益的天然調脂藥物,并已完成美國食品藥品監督管理局(FDA)二期臨床研究。力撲素®是首個商業化的紫杉醇脂質體制劑,也是目前全球唯一上市的紫杉醇脂質體制劑,用于治療乳腺癌、非小細胞肺癌和卵巢癌。貝伐珠單抗注射液(LY01008)用于治療晚期、轉移性或復發性非小細胞肺癌和轉移性結直腸癌,該在研產品已于2020年4月在中國申報上市申請。
根據戰略合作備忘錄,綠葉制藥與阿斯利康將在現有合作基礎上積極探索未來合作的方向,希望在合作的深度和廣度方面能有進一步地提升。在心血管領域,雙方將在目前已有的全球范圍內商業化合作的基礎上,圍繞互聯網醫療及線上渠道拓展探討更多創新推廣模式,進一步提升血脂康®膠囊的患者用藥可及性。在腫瘤領域,雙方將探討如何聯合各自優勢,進一步深化力撲素®在廣闊區域和細分市場的覆蓋,并將就該產品后續的臨床學術研究方面的合作機會加強溝通。此外,雙方還將就綠葉制藥另一大腫瘤在研產品LY01008與阿斯利康抗腫瘤藥物開展臨床聯合用藥研究進行深入探討,并積極探索LY01008在中國以外的各大國際新興市場的合作空間。
“與阿斯利康的再度攜手,標志著我們雙方合作關系的進一步深化。阿斯利康在心血管、腫瘤治療領域深耕多年,擁有廣泛的創新資源和全球網絡,我們期待雙方圍繞這兩大疾病領域建設更為緊密、互惠的合作關系,通過聯合兩家公司的資源與優勢,幫助更多病人及時獲益于有效的治療。”綠葉制藥集團總裁楊榮兵先生表示。
“植根中國20多年來,阿斯利康始終秉持‘以患者為中心’的理念,關注中國需求最迫切的疾病領域,為患者提供優質的創新醫藥資源。我們期待與綠葉制藥能有更多的合作機會,共同為廣大患者提供更多、更好的創新醫療方案。”阿斯利康全球執行副總裁、國際業務及中國總裁王磊先生表示:“一直以來,阿斯利康致力于和中國本土企業的合作,共同推動中國健康產業的創新發展,惠及更多的患者。”
關于血脂康®膠囊
血脂康®膠囊是利用現代工藝發酵特制紅曲制成的純天然調脂藥。血脂康®膠囊有調節異常血脂的作用,可降低血膽固醇、甘油三酯、低密度脂蛋白膽固醇和升高高密度脂蛋白膽固醇;抑制動脈粥樣硬化斑塊的形成,保護血管內皮細胞;抑制脂質在肝臟沉積。該產品已上市20多年,包括中國冠心病二級預防研究(CCSPS)等大型臨床循證醫學研究均證實:血脂康®能夠抑制膽固醇合成,并顯著降低冠心病患者總死亡率、冠心病死亡率以及心血管事件發生率,不良反應少。
關于力撲素®
力撲素®屬于紫杉醇納米制劑,是首個商業化的紫杉醇脂質體制劑,也是目前全球唯一上市的紫杉醇脂質體制劑,用于治療乳腺癌、非小細胞肺癌、卵巢癌。該藥物獨特的腫瘤和淋巴結靶向性以及較長的半衰期,能更好地發揮抗腫瘤作用,同時獲得更好的安全性和耐受性。上市十六年來,力撲素®的患者累計用藥超過200萬人次,其良好的療效和安全性已在長期臨床應用中獲得廣泛認可,并相繼獲得多個權威指南和共識明確推薦。據最新發布的臨床研究結果,力撲素®聯合順鉑對比吉西他濱聯合順鉑一線治療晚期肺鱗癌的療效相當,安全性和依從性更優。
關于貝伐珠單抗注射液(LY01008)
貝伐珠單抗注射液(LY01008)用于治療晚期、轉移性或復發性非小細胞肺癌和轉移性結直腸癌。該產品的上市申請已于2020年4月獲得中國國家藥品監督管理局藥品審評中心受理。
]]>上海2020年11月26日 /美通社/ -- 綠葉制藥集團宣布與菲律賓的全國藥品分銷公司Distribution Solutions Phils., Inc.(Distriphil)達成合作協議,向Distriphil授予中樞神經系統藥物思瑞康®(富馬酸喹硫平,速釋)、以及思瑞康緩釋片®(緩釋制劑)在菲律賓市場的獨家分銷和推廣權。
簽約儀式于11月26日在線上舉行,不僅標志著雙方合作的開始,Distriphil也將參與到綠葉制藥面向亞太地區發起的“關愛精神健康”公益活動中。該項公益活動致力于提升公眾對于精神健康問題的關注和認知,以支持患者、醫生和醫療衛生體系共同應對這一亟待解決的醫療挑戰。在當下新冠肺炎疫情蔓延全球的嚴峻背景下,這一舉措顯得尤為及時。
雙相情感障礙、精神分裂癥、抑郁癥和焦慮癥等各類精神疾病已成為影響全球公眾健康的重大公共衛生問題。世界衛生組織數據顯示[i],全球已有近10億人存在精神障礙,每40秒鐘就有一人自殺身亡。當前新冠肺炎疫情的大流行使全球數十億人受到影響,進一步沖擊著公眾的心理健康。
為了幫助公眾進一步認識到各類精神健康問題的重要性,綠葉制藥攜手各地合作伙伴,于今年6月在亞太區共同發起“關愛精神健康”公益活動,截止目前已在多個國家和地區成功舉辦32場疾病教育活動。今年10月,綠葉制藥還在線上召開第二屆亞太精神科峰會,吸引來自亞太區9個國家和地區的1000多名精神科醫生參會,共同探討精神分裂癥、雙相情感障礙等精神疾病的治療與管理。在此次達成的分銷合作的基礎上,Distriphil亦將與綠葉制藥攜手推動“關愛精神健康”公益活動在菲律賓的開展,雙方將通過舉辦一系列線上及線下公益講座,邀請精神健康領域的專家科普疾病知識,進一步提升當地公眾的精神健康意識。
“精神健康問題是一項嚴峻的全球公共健康挑戰,需要我們所有人團結一致、長期共同應對。‘關愛精神健康’公益活動有助于提升公眾對于各類精神健康問題的了解,為大家提供更多治療選擇和科學建議,并幫助大家意識到早診斷、早治療的重要性。”綠葉制藥(國際)亞太區商務總監蕭幸偉表示,“我們期待與Distriphil的合作,協同各方力量,共同提升公眾的精神健康意識,并為患者帶來更好的關懷和服務。”
“能夠為滿足菲律賓當地公眾日益增長的精神健康需求獻一份力,我們感到十分榮幸。這也正是Distriphil的使命所在:通過提供包括思瑞康在內的高品質藥物,致力于為每一位菲律賓患者提供關懷、改善他們的健康。”Distriphil公司副總裁兼首席運營官Michael Quijano表示,“我們很高興與綠葉制藥達成合作并共同開展‘關愛精神健康’公益活動,期待能為改善菲律賓當地的精神健康問題做出貢獻。”
[i] 世界衛生組織官網:《世界精神衛生日:啟動大規模增加精神衛生投資的機會》https://www.who.int/news/item/27-08-2020-world-mental-health-day-an-opportunity-to-kick-start-a-massive-scale-up-in-investment-in-mental-health |